 化学能与热能第一课时公开课
化学能与热能第一课时公开课


《化学能与热能第一课时公开课》由会员分享,可在线阅读,更多相关《化学能与热能第一课时公开课(22页珍藏版)》请在装配图网上搜索。
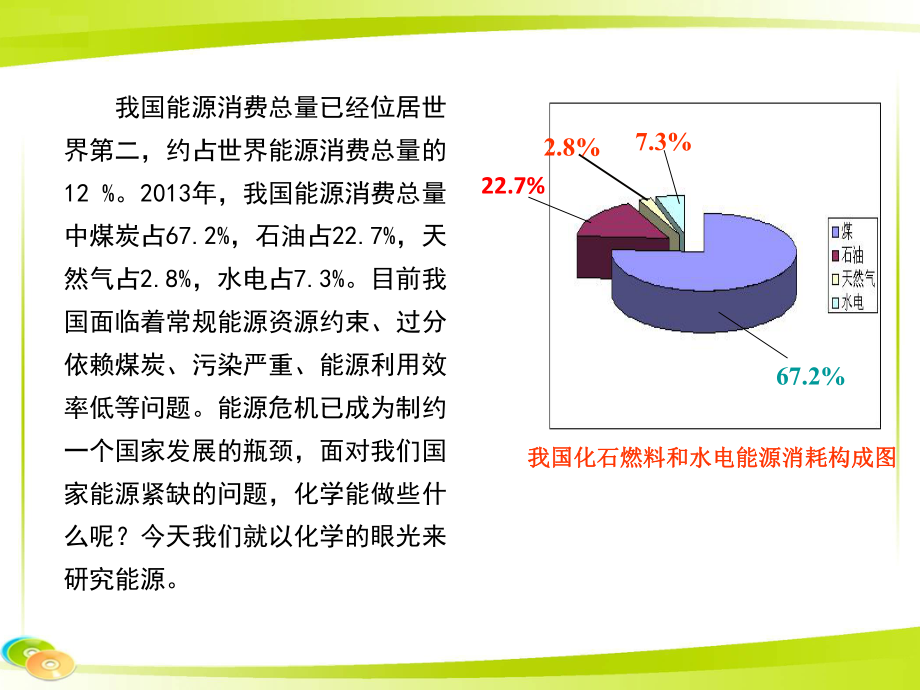
1、2.8%7.3%67.2%我国化石燃料和水电能源消耗构成图我国化石燃料和水电能源消耗构成图22.7%我国能源消费总量已经位居世界第二,约占世界能源消费总量的12%。2013年,我国能源消费总量中煤炭占67.2%,石油占22.7%,天然气占2.8%,水电占7.3%。目前我国面临着常规能源资源约束、过分依赖煤炭、污染严重、能源利用效率低等问题。能源危机已成为制约一个国家发展的瓶颈,面对我们国家能源紧缺的问题,化学能做些什么呢?今天我们就以化学的眼光来研究能源。2-1 2-1 化学能与热能化学能与热能第一课时第一课时 第二章第二章 化学反应与能量化学反应与能量1.1.知道能量变化是化学反应的又一特征
2、。知道能量变化是化学反应的又一特征。2.2.理解化学反应中能量变化的主要原因。理解化学反应中能量变化的主要原因。3.3.了解化学反应中能量变化的形式。了解化学反应中能量变化的形式。魔术:水点火【讨论交流讨论交流】1、你看到了什么现象?、你看到了什么现象?2、由这个现象你能得出什么结论?、由这个现象你能得出什么结论?3、根据你的预习情况解释你的结论。、根据你的预习情况解释你的结论。一个化学反应的过程,本质上就是一个化学反应的过程,本质上就是旧化学键断裂旧化学键断裂和和新化学键形成新化学键形成的过程。的过程。吸收能量吸收能量放出能量放出能量断开断开1mol H-H键要键要吸收吸收的能量为的能量为4
3、36kJ。断开断开1mol Cl-Cl键要键要吸收吸收的能量为的能量为243kJ。形成形成1mol Cl-Cl键键放出放出的能量为的能量为243kJ。例例 如如 在在250C、101KPa的条件下:的条件下:形成形成1mol H-H键键放出放出的能量为的能量为436kJ。形成形成1mol化学键时释放的能量或断裂化学键时释放的能量或断裂1mol化学化学键时吸收的能量。键时吸收的能量。(一)(一)键能:键能:一、化学键与化学反应中能量变化的关系一、化学键与化学反应中能量变化的关系键键键能键能键键键能键能HH436CH415.0ClCl242.7OH462.8BrBr193.7NH390.8II15
4、2.7HCl431.8CC347.7HI298.7某些化学键的键能某些化学键的键能(KJ/mol)键能越大键能越大化学键越牢固化学键越牢固含该键的分子越稳定含该键的分子越稳定该分子具有的能量越低该分子具有的能量越低一、化学键与化学反应中能量变化一、化学键与化学反应中能量变化的关系的关系(二)化学键与能量变化的关系(微观角度)(二)化学键与能量变化的关系(微观角度)思考思考在化学反应中,反应物中化学键的断裂吸收在化学反应中,反应物中化学键的断裂吸收能量,生成物中化学键的形成放出能量,那么,能量,生成物中化学键的形成放出能量,那么,一一个化学反应吸收能量还是放出能量与化学键有何关个化学反应吸收能量
5、还是放出能量与化学键有何关系?系?以氢气在氯气中燃烧为例,用化学键的以氢气在氯气中燃烧为例,用化学键的观点分析反应的本质过程。观点分析反应的本质过程。由反应式:由反应式:H2+Cl2=2HCl 可知可知 破坏破坏1molH-H、1molCl-Cl键键吸收的能量为:吸收的能量为:436.0k J/mol1mol+243kJ/mol1mol =679k J 形成形成2molH-Cl键键放出的能量放出的能量为为 431k J/mol2mol=862kJ 放出的能量放出的能量大于大于吸收的能量吸收的能量,该反应是放热反应,放出,该反应是放热反应,放出的热量为的热量为 862k J 679k J=183
6、k J化学键的断裂和形成化学键的断裂和形成是化学反应中能量变化的主是化学反应中能量变化的主要原因。要原因。1 1、化学反应中能量变化的主要原因是什么?、化学反应中能量变化的主要原因是什么?2 2、化学反应中能量变化与化学键的关系是什么呢?、化学反应中能量变化与化学键的关系是什么呢?化学反应中是吸收能量还是放出能量要看化学反应中是吸收能量还是放出能量要看断键时断键时吸收的能量多还是成键时放出能量得多吸收的能量多还是成键时放出能量得多。在化学反应中在化学反应中:断键吸收的总能量断键吸收的总能量 成键放出的总能量成键放出的总能量化学反应化学反应吸收能量吸收能量从微观角度:从微观角度:即化学键的断裂与
7、形成,能即化学键的断裂与形成,能计算出化学反应中能量的变化。下面我们计算出化学反应中能量的变化。下面我们从宏观角度从宏观角度继续探究化学反应中能量的变继续探究化学反应中能量的变化。化。宏观上:任何物质都储存有化学能,宏观上:任何物质都储存有化学能,不同的物不同的物质由于结构和组成不同,则所含化学能不同。质由于结构和组成不同,则所含化学能不同。因此,因此,反应物的总能量反应物的总能量与与生成物的总能量生成物的总能量不相不相等,导致反应有能量的变化。等,导致反应有能量的变化。先看实例:先看实例:(三)、物质具有的能量与化学反应中能(三)、物质具有的能量与化学反应中能量变化的关系(宏观角度)量变化的
8、关系(宏观角度)思考(1)当反应物具有的总能量比生成物所具当反应物具有的总能量比生成物所具有的总能量多时,反应物变成生成物后,有的总能量多时,反应物变成生成物后,根根据能量守恒原理,据能量守恒原理,多出的能量哪去了?多出的能量哪去了?多出的能量释放出去了多出的能量释放出去了 E 反反应物应物+E 生成生成物物热量热量结论:结论:E E反反EE生,反应为放热反应生,反应为放热反应 E 生生成物成物+E 反应反应物物热量热量思考?思考?(2)当生成物具有的总能量比反应物所具有当生成物具有的总能量比反应物所具有的总能量多时,多出的能量从哪里来?的总能量多时,多出的能量从哪里来?多出的能量从外界吸收进
9、来多出的能量从外界吸收进来结论:结论:E E生生EE反,反应为吸热反应反,反应为吸热反应【课堂过关检测课堂过关检测】看图讨论,并回答问题看图讨论,并回答问题左图表示的化学反应为左图表示的化学反应为 反应(吸热反应(吸热/放热)放热)右图表示的化学反应为右图表示的化学反应为 反应(吸热反应(吸热/放热)放热)放热放热吸热吸热化学反应的过程,可以看成是能量的化学反应的过程,可以看成是能量的“贮存贮存”或或“释放释放”的的过程过程宏观宏观:化学反应中能量变化主要取决于反应物的总能:化学反应中能量变化主要取决于反应物的总能量和生成物的量和生成物的总能量的相对大小总能量的相对大小。微观微观:化学键的断裂和形成是化学反应中能量变化的:化学键的断裂和形成是化学反应中能量变化的主要原因主要原因。断键吸收总能量断键吸收总能量 成键放出总能量成键放出总能量反应物的反应物的总总能量能量 生成物的生成物的总总能量能量反应物的总能量反应物的总能量 0为放热反应为放热反应Q0为吸热反应为吸热反应 本节课学习了哪些知识和学习方法?本节课学习了哪些知识和学习方法?通过本节课的学习你有哪些收获或感想?通过本节课的学习你有哪些收获或感想?资料61页:1、变式训练12、探究:比较放热反应和吸热反应
- 温馨提示:
1: 本站所有资源如无特殊说明,都需要本地电脑安装OFFICE2007和PDF阅读器。图纸软件为CAD,CAXA,PROE,UG,SolidWorks等.压缩文件请下载最新的WinRAR软件解压。
2: 本站的文档不包含任何第三方提供的附件图纸等,如果需要附件,请联系上传者。文件的所有权益归上传用户所有。
3.本站RAR压缩包中若带图纸,网页内容里面会有图纸预览,若没有图纸预览就没有图纸。
4. 未经权益所有人同意不得将文件中的内容挪作商业或盈利用途。
5. 装配图网仅提供信息存储空间,仅对用户上传内容的表现方式做保护处理,对用户上传分享的文档内容本身不做任何修改或编辑,并不能对任何下载内容负责。
6. 下载文件中如有侵权或不适当内容,请与我们联系,我们立即纠正。
7. 本站不保证下载资源的准确性、安全性和完整性, 同时也不承担用户因使用这些下载资源对自己和他人造成任何形式的伤害或损失。
