 高中化学第一章从实验学化学习题
高中化学第一章从实验学化学习题


《高中化学第一章从实验学化学习题》由会员分享,可在线阅读,更多相关《高中化学第一章从实验学化学习题(5页珍藏版)》请在装配图网上搜索。
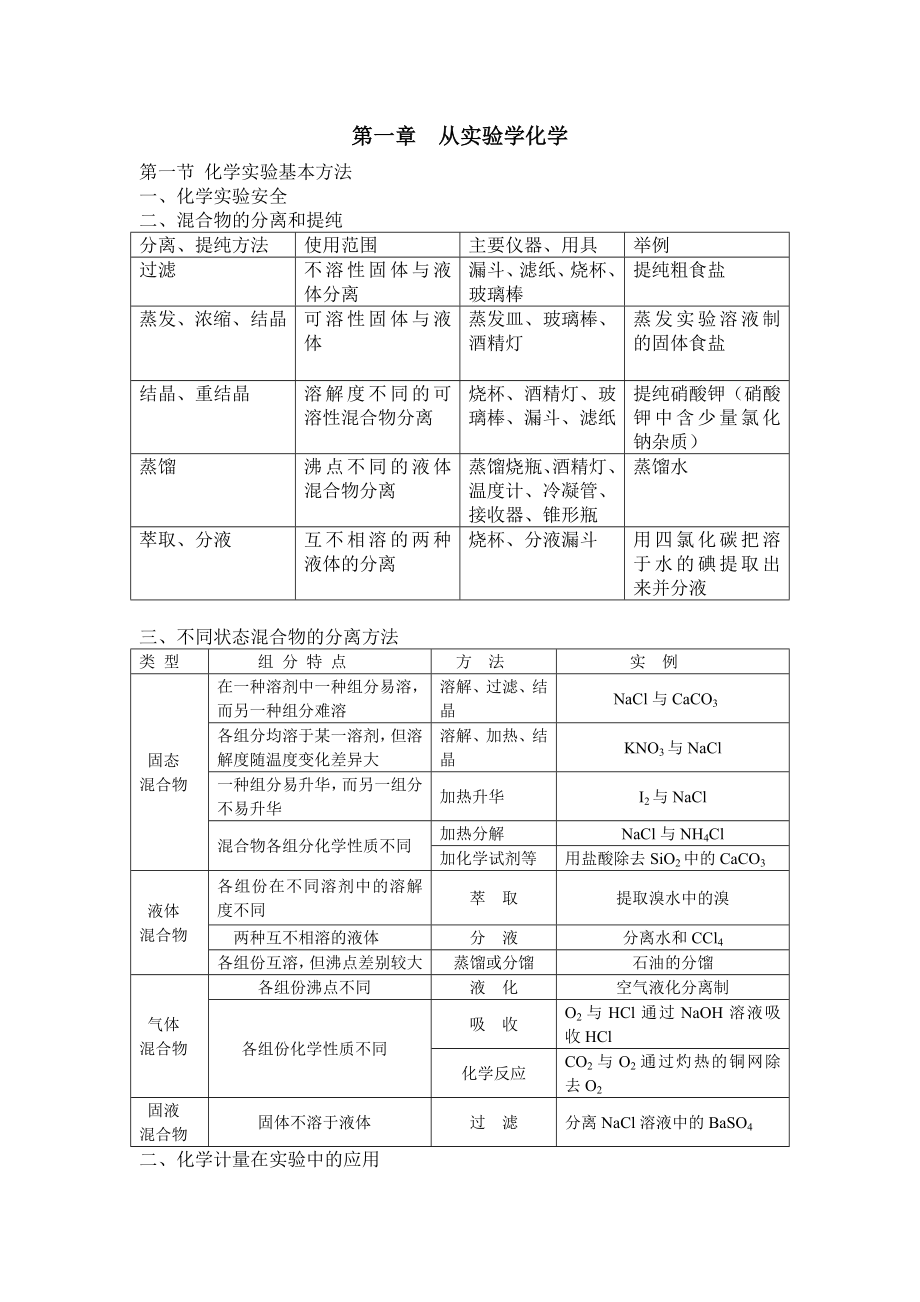
1、第一章 从实验学化学第一节 化学实验基本方法一、 化学实验安全二、 混合物的分离和提纯分离、提纯方法使用范围主要仪器、用具举例过滤不溶性固体与液体分离漏斗、滤纸、烧杯、玻璃棒提纯粗食盐蒸发、浓缩、结晶可溶性固体与液体蒸发皿、玻璃棒、酒精灯蒸发实验溶液制的固体食盐结晶、重结晶溶解度不同的可溶性混合物分离烧杯、酒精灯、玻璃棒、漏斗、滤纸提纯硝酸钾(硝酸钾中含少量氯化钠杂质)蒸馏沸点不同的液体混合物分离蒸馏烧瓶、酒精灯、温度计、冷凝管、接收器、锥形瓶蒸馏水萃取、分液互不相溶的两种液体的分离烧杯、分液漏斗用四氯化碳把溶于水的碘提取出来并分液三、 不同状态混合物的分离方法类 型组 分 特 点方 法实 例
2、固态混合物在一种溶剂中一种组分易溶,而另一种组分难溶溶解、过滤、结晶NaCl与CaCO3各组分均溶于某一溶剂,但溶解度随温度变化差异大溶解、加热、结晶KNO3与NaCl一种组分易升华,而另一组分不易升华加热升华I2与NaCl混合物各组分化学性质不同加热分解NaCl与NH4Cl加化学试剂等用盐酸除去SiO2中的CaCO3液体混合物各组份在不同溶剂中的溶解度不同萃 取提取溴水中的溴两种互不相溶的液体分 液分离水和CCl4各组份互溶,但沸点差别较大蒸馏或分馏石油的分馏气体混合物各组份沸点不同液 化空气液化分离制各组份化学性质不同吸 收O2与HCl通过NaOH溶液吸收HCl化学反应CO2与O2通过灼热
3、的铜网除去O2固液混合物固体不溶于液体过 滤分离NaCl溶液中的BaSO4二、化学计量在实验中的应用1.物质的量:表示含有一定数目粒子的集合体,符号为n,单位为mol。2阿伏加德罗常数NA: 1mol 任何物质含的微粒数目都是6.021023 个;3摩尔质量:单位物质的量的物质所具有的质量,符号为M,单位为g/mol; 4、气体摩尔体积:单位物质的量的气体所占的体积(标准状态下体积为22.4L/mol),符号Vm,单位为L/mol。5、 阿伏加德罗定律:由PV=nRT 可推导出温度、体积、压强、分子数之间的关系。6、 物质的量浓度:单位体积溶液里所含溶质的物质的量,符号CB,数学表达式为 CB
4、=nB/V。7、物质的量浓度CB 与溶质的质量分数=1000 M。8、溶液稀释规律C(浓)V(浓)=C(稀)V(稀)以物质的量为中心。三、一定物质的量浓度溶液的配制配制口诀: 配制过程共六步,第一计算二称量, 第三烧杯中溶解,第四入瓶兼洗涤。第五滴管慢滴水,凹液面与刻度齐,第六倒转摇数次,写贴标签移瓶中。注: 1、只能配制容量瓶上标定容积的溶液;意 2、配前检漏;事 3、不能用容量瓶溶解、稀释或久存溶液,转入容量瓶中的溶液应先使温度恢复至20项 度左右;4、拿容量瓶时,手指应持在瓶颈刻度线以上部分,以免手温影响溶液温度;5、如果加多了水或者洒出了几点溶液都应重配;6、定容好了后在震荡,液面低于
5、刻度线时不要再加水;7、用玻璃棒引流时,玻璃棒下端应在刻度线以下。典型例题:一、选择题(每小题均有一个选项符合题意)如果你家里的食用花生油混有水份,你将采用下列何种方法分离A过滤B蒸馏C分液D萃取下列实验操作均要用玻璃棒,其中玻璃棒作用相同的是 过滤 蒸发 溶解 向容量瓶转移液体A和B和C和D和以下是一些常用的危险品标志,装运乙醇的包装箱应贴的图标是 A B C D实验中的下列操作正确的是A用试管取出试剂瓶中的Na2CO3溶液,发现取量过多,为了不浪费,又把过量的试剂倒入试剂瓶中BBa(NO3)2 溶于水,可将含有Ba(NO3)2 的废液倒入水槽中,再用水冲入下水道C用蒸发方法使NaCl 从溶
6、液中析出时,应将蒸发皿中NaCl 溶液全部加热蒸干D用浓硫酸配制一定物质的量浓度的稀硫酸时,浓硫酸溶于水后,应冷却至室温才能转移到容量瓶中过滤后的食盐水仍含有可溶性的CaCl2、MgCl2、Na2SO4 等杂质,通过如下几个实验步骤,可制得纯净的食盐水: 加入稍过量的Na2CO3溶液; 加入稍过量的NaOH溶液; 加入稍过量的BaCl2 溶液;滴入稀盐酸至无气泡产生; 过滤正确的操作顺序是ABCD下列叙述正确的是A1 mol H2O的质量为18g/molBCH4的摩尔质量为16gC3.011023个SO2分子的质量为32gD标准状况下,1 mol任何物质体积均为22.4L.对下列实验过程的评价
7、,正确的是( )A某固体中加入稀盐酸,产生了无色气体,证明该固体中一定含有碳酸盐B某溶液中滴加BaCl2溶液,生成不溶于水稀HNO3的白色沉淀,证明一定含有SO42-C某无色溶液滴入酚酞试液显红色,该溶液一定是碱溶液D验证烧碱溶液中是否含Cl-,先加稀盐酸除去OH-,再加入AgNO3溶液,有白色沉淀,证明含Cl-过滤后的食盐水仍含有可溶性的CaCl2、MgCl2、Na2SO4 等杂质,通过如下几个实验步骤,可制得纯净的食盐水: 加入稍过量的Na2CO3溶液; 加入稍过量的NaOH溶液; 加入稍过量的BaCl2 溶液;滴入稀盐酸至无气泡产生; 过滤正确的操作顺序是ABCD用NA表示阿伏德罗常数,
8、下列叙述正确的是A标准状况下,22.4LH2O含有的分子数为1 NAB常温常压下,1.06g Na2CO3含有的Na+离子数为0.02 NAC通常状况下,1 NA 个CO2分子占有的体积为22.4LD物质的量浓度为0.5mol/L的MgCl2溶液中,含有Cl- 个数为1 NA欲配制100ml 1.0 mol/L Na2SO4溶液,正确的方法是 将14.2 g Na2SO4 溶于100ml水中 将32.2g Na2SO410H2O溶于少量水中,再用水稀释至100 ml 将20 ml 5.0 mol/L Na2SO4溶液用水稀释至100 mlABCD0.5L 1mol/L FeCl3溶液与0.2L
9、1mol/L KCl溶液中的Cl-的数目之比A5:2B 3:1C15:2D 1:3二、非选择题13.草木灰中主要含有K2C03、KCl、K2S04等钾盐,现欲从草木灰中提取钾盐,填写下列空白(1)此实验操作顺序如下:称量样品,溶解沉淀, 冷却结晶。(2)用天平(托盘天平、指针向上)称量样品时,若指针偏向右边则表示(填代码)A左盘重,样品轻 B左盘轻,砝码重C左盘轻,砝码轻 D右盘轻,样品重(3)在进行第步操作时,有时可能要重复进行,这是由于 在进行第步操作时,要用玻璃棒不断小心地搅动液体,目的是防止 现欲通过实验证明所得钾盐中含有K2S04,则需将晶体溶于水,然后加入 。14海洋植物,如海带、
10、海藻中含有丰富的碘元素,碘元素以碘离子的形式存在。实验室里从海带中提取碘的流程如下:(已知C12+2KI=2KCl+I2)(1)指出提取碘的过程中有关的实验操作名称: , 。(2)提取碘的过程中,可供选择的有机试剂是( ) A苯、酒精 BCCl4、苯 C汽油、乙酸(3)为使海带灰中碘离子转化为碘的有机溶液,实验室里的烧杯、玻璃棒、集气瓶、酒精灯、导管、圆底烧瓶、石棉网以及必要的夹持仪器和物品,仍缺少的玻璃仪器 (4)从含碘的有机溶剂中提取碘和回收有机溶剂,还需要经过蒸馏过程(为防止碘升华,本实验中采用水浴加热)。指出下列蒸馏实验装置中的错误(如下图) , 。15 (1)CCl4和蒸馏水都是无色
11、液体,请按下列要求用实验方法鉴别之(简要地写出实验过程) 只允许用一种试剂 不用任何试剂 (2)NaCl溶液中含有少量的CaCl2,某学生用过量的Na2CO3使Ca2+离子转化为沉淀而除去,确认Na2CO3已过量的实验方法是 16现用质量分数为98、密度为184gcm-3的浓H2SO4来配制500mL、02molL-1的稀H2S04。可供选择的仪器有:玻璃棒烧瓶烧杯胶头滴管量筒容量瓶托盘天平药匙。请回答下列问题:(1)上述仪器中,在配制稀H2S04时用不到的有 (填代号)。(2)经计算,需浓H2S04的体积为 。现有10mL50mL100mL三种 规格的量筒,你选用的量筒是 (填代号)。(3)
12、将浓H2S04加适量蒸馏水稀释后,冷却片刻,随后全部转移到 mL的 容量瓶中,转移时应用玻璃棒 。转移完毕,用少量蒸馏水洗涤烧杯 23次,并将洗涤液全部转移到容量瓶中,再加适量蒸馏水,振荡容量瓶,使溶液混合均匀。然后缓缓地把蒸馏水直接注入容量瓶直到液面接近刻度 处。改用 加蒸馏水到瓶颈刻度的地方,使溶液的 。 振荡、摇匀后,装瓶、贴签。(4)在配制过程中,其他操作都准确,下列操作中: 错误的是 ,能引起误差偏高的有 (填代号)。 洗涤量取浓H2S04后的量筒,并将洗涤液转移到容量瓶中 未等稀释后的H2S04溶液冷却至室温就转移到容量瓶中 将浓H2S04:直接倒人烧杯,再向烧杯中注入蒸馏水来稀释浓H2S04 定容时,加蒸馏水超过标线,又用胶头滴管吸出 转移前,容量瓶中含有少量蒸馏水 定容摇匀后,发现液面低于标线,又用胶头滴管加蒸馏水至标线 定容时,俯视标线16常温下,在27.5g水中溶解12.5g CuSO45H2O,恰好达到饱和,该溶液密度为1.21g /cm3,求: 该溶液中阴阳离子的总物质的量; 该溶液中CuSO4的物质的量浓度; 取出20.0 ml该溶液,配成浓度为1.00 mol/L的稀溶液,则稀释后溶液的体积是多少毫升?
- 温馨提示:
1: 本站所有资源如无特殊说明,都需要本地电脑安装OFFICE2007和PDF阅读器。图纸软件为CAD,CAXA,PROE,UG,SolidWorks等.压缩文件请下载最新的WinRAR软件解压。
2: 本站的文档不包含任何第三方提供的附件图纸等,如果需要附件,请联系上传者。文件的所有权益归上传用户所有。
3.本站RAR压缩包中若带图纸,网页内容里面会有图纸预览,若没有图纸预览就没有图纸。
4. 未经权益所有人同意不得将文件中的内容挪作商业或盈利用途。
5. 装配图网仅提供信息存储空间,仅对用户上传内容的表现方式做保护处理,对用户上传分享的文档内容本身不做任何修改或编辑,并不能对任何下载内容负责。
6. 下载文件中如有侵权或不适当内容,请与我们联系,我们立即纠正。
7. 本站不保证下载资源的准确性、安全性和完整性, 同时也不承担用户因使用这些下载资源对自己和他人造成任何形式的伤害或损失。
