 人教版高一化学教学设计——卤素8
人教版高一化学教学设计——卤素8


《人教版高一化学教学设计——卤素8》由会员分享,可在线阅读,更多相关《人教版高一化学教学设计——卤素8(13页珍藏版)》请在装配图网上搜索。
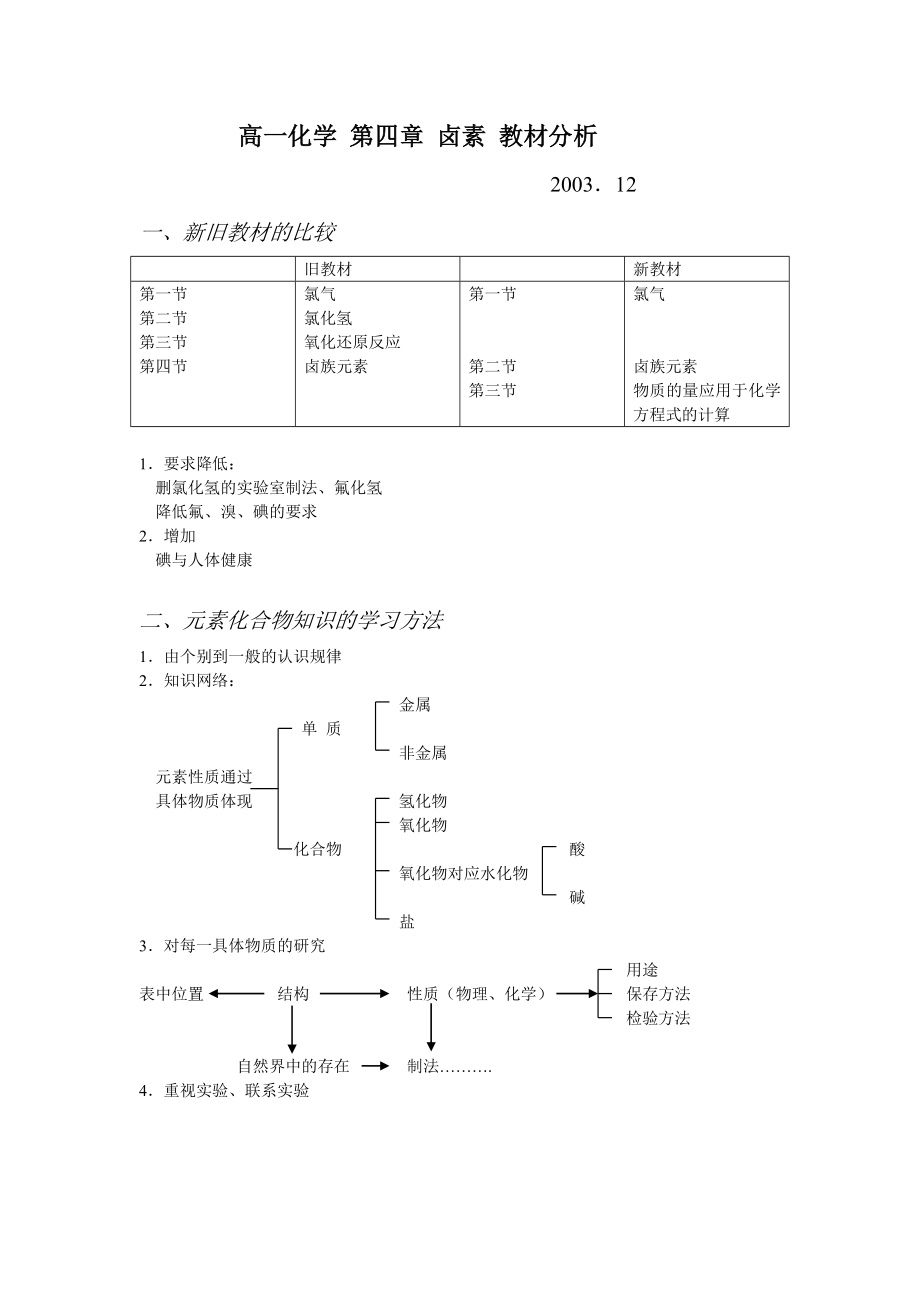
1、高一化学 第四章 卤素 教材分析200312一、新旧教材的比较旧教材新教材第一节第二节第三节第四节氯气氯化氢氧化还原反应卤族元素第一节第二节第三节氯气卤族元素物质的量应用于化学方程式的计算1要求降低:删氯化氢的实验室制法、氟化氢降低氟、溴、碘的要求2增加碘与人体健康二、元素化合物知识的学习方法1由个别到一般的认识规律2知识网络: 金属 单 质 非金属 元素性质通过 具体物质体现 氢化物 氧化物 化合物 酸 氧化物对应水化物 碱 盐3对每一具体物质的研究 用途表中位置 结构 性质(物理、化学) 保存方法 检验方法 自然界中的存在 制法.4重视实验、联系实验 三、教法建议 第一节 氯气一、 结构原
2、子结构示意图、离子结构示意图、电子式、结构式二、物理性质色态气味溶解性,密度熔沸和特性三、化学性质酸碱性、氧-还性、稳定性1.氯气:氯为0价氧化性:与金属钠、铁、铜与非金属氢气、磷与水与碱氢氧化钠、氢氧化钙相互置换2.次氯酸的性质(3点):弱酸性:HClO H+ClO- 不稳定性:2HClO 2HCl+O2强氧化性:是由不稳定性导致的,在溶液中新生成的氧气有特别强的得电子能力,这种能力在化学上叫氧化能力。由于有强氧化性,所以次氯酸可以用于杀菌消毒和漂白。区别干燥氯气液氯新制氯水久置氯水组成成分漂白作用注意对比:次氯酸、过氧化钠、活性炭的漂白性。四、实验室制法原料、原理、装置(发生、收集、尾气处
3、理)、操作第二节 卤族元素编写模式采用科学探究方法的写法事实原子结构分析结构特征推论相似形和差异性实验验证与金属、非金属等反应 结论 推论正确 (直接给出) (说明) (预测) (现象反映) (检验)一、物理性质 水苯或汽油(上层)四氯化碳(下层)溴碘二、化学性质 结 构:最外层电子数=7相似形 化学性质:易失一个电子,强氧化性 结 构:质子数增大,电子层数增大,原子半径增大,氧化性渐弱递变性 与氢气反应的条件 化学性质 气态氢化物的稳定性 最高价氧化物水化物的酸性强弱 相互置换 三、卤化银溶解性、卤离子检验、不稳定性、用途第三节 物质的量应用于化学方程式的计算化学计量数 SI单位为一,符号为
4、1,单位一般不写出化学计量数比规则 各反应物之间相互起反应的物质的量之比等于它们的化学计量数之比 n(A) = (A)n(B) (B)根据化学方程式计算的基本步骤1 根据题意写方程式2 找已知量、未知量3 列比例式4 求解5 答注意事项1 换算纯量代入方程2 上下相同 左右配套 高一化学第四章第二节卤族元素(第一课时)教学目标知识和技能:1、掌握卤素原子结构和化学性质的相似点和递变性2、通过结构和化学性质关系的分析,培养学生的思维能力过程和方法:3、通过对比实验,培养学生的观察能力和科学实验的方法4、通过实验设计,培养学生的合作精神情感价值观:5、通过结构决定性质的分析,对学生进行本质决定现象
5、的辩证唯物主义观点教育6、通过物质的特性,使学生认识矛盾的一般性和特殊性教学重点、难点:卤素的原子结构和化学性质的相似点和递变性教学方法:探究实验、讲解、讨论教学法教学用品1、实验用品:氯气,液溴,固体碘,滴管,氯水,溴水,溴化钠溶液,碘化钾溶液,淀粉试液,蒸馏水2、电教用品:教学过程一、单质物理性质教师活动学生活动设计意图学习了氯气后,我们一起来研究卤族的其它元素板书:第二节卤族元素卤素(以X表示)单质的通式、氢化物的通式如何表示?首先先探究卤素单质的物理性质的变化情况。(1)观察氯气、溴和碘的色态。(2)观察氯水、溴水、碘水的色态指导学生分析现象分析数据学生观察现象、小结规律(1)卤素单质
6、的颜色:氯气 黄绿色,溴 红褐色,碘 紫黑色变化规律:从氟到碘,渐深(2)水溶液颜色:氯水黄绿色,溴水-橙色,碘水-棕色(颜色深浅与浓度有关)学生探究实验(1)各取3-5 ml溴水、碘水,分别加入约2ml汽油,振荡,静置,观察现象。(2)各取3-5ml溴水、碘水,分别加入约2ml四氯化碳(CCl4),振荡,静置,观察现象。(3)稍微加热碘球,观察现象。培养学生的观察能力和总结现象的能力。观察实验,思考讨论指导学生学小结:(1)有机溶液的颜色:溴 汽油 橙色,CCl4橙色碘 汽油 橙色CCl4紫红色(4)卤素单质的熔沸点:渐高(5)溶解性:可溶于水,易溶于有机溶剂。(6)特性:溴易挥发,碘易升华
7、提问什么是升华?(1)描述观察的实验现象.(2)卤素单质的颜色,溶沸点有什么变化规律?(3) 卤素单质的溶解性有什么规律?(4)卤素单质有什么特性?会重点和实验结果归纳。指导学生生阅读。板书二、结构和化学性质投影卤素的原子结构示意图和原子半径(1)卤素的结构:在核电荷数、电子层数、最外层电子数、原子半径四个方面有什么相似点和递变性?学生讨论分析数据培养学生分析归纳总结的能力。板书(2)卤素的结构及其化学性质1、相似点:(1)结构:最外层电子数均为7个,易得1个电子。(2)化合价:最低价-1(3)化学性质:结构决定性质。讨论,小结通过结构决定性质的分析,对学生进行本质决定现象的辩证唯物义义观点教
8、育。复习氯气的化学性质Cl+eCl-思考回忆 和金属反应:Cl2+2Na(点燃)2NaCl 和氢气反应:Cl2+H2(点燃)2HCl 和水反应:Ci2+H2OHCl+ HClO 和NaOH反应:Cl2+2NaOH NaCl+NaClO+H2O复习旧知识,为新知识打基础。小结,板书根据氯气的化学性质,推导卤素单质可能的化学性质板书:X+eX-学生 书写方式:和金属反应:如:X2+2Na-(点燃)2NaX和氢气反应:X2+H2-(点燃) 2HX和水反应:X2+ H2OHX+HXO(除氟外)和NaOH反应:X2+2NaOHNaX+NaXO+H2O(除氟外)指导学生方法,和类比推理能力。板书2、递变性
9、(1)结构:从氟到碘(计算机辅助),核电荷数:递增电子层数:递增原子半径:递增指导学生阅读课本:卤素单质结合氢的能力、和水的反应能力、单质的氧化性有何规律?思考原子得电子能力:递减单质的氧化性:递减思考化学性质:结合氢的能力:递减和水反应能力:递减单质的氧化性:递减培养学生的分析归纳能力培养阅读能力你能设计一个实验来验证卤素单质的氧化性的强弱吗?指导学生用蒸馏水作空白对比实验思考:写出上述反应的化学方程式,这些反应的类型是什么?用氧化还原反应的规律比较分析卤素单质间的氧化性?(分析讲解)讨论实验方案学生探究利用卤素间的置换反应,验证卤素单质的氧化性(1)把少量氯水加入到溴化钠溶液中,观察现象。
10、(2)把少量氯水加入到碘化钾溶液中,观察现象。(3)把少量溴水加入到碘化钾溶液中,观察现象。进行科学研究方法的训练根据氧化还原反应的规律:氧化剂比氧化产物的氧化性强氧化性:Cl2Br2I2讨论,分析卤素单质氧化性强弱的变化规律。Cl2+2NaBr2NaCl+Br2氧化剂:CI2 氧化产物:Br2Cl2+2KI2KCl+I2氧化剂:Cl2 氧化产物:I2Br2+2KI2KBr+I2氧化剂:Br2 氧化产物:I2巩固氧化还原反应的概念,加深对变化规律的理解,为下一章学习作准备。小结卤素原子结构和性质的递变性(从氟到碘)结构:电子层数,递增;原子半径,递增物理性质:颜色:渐深;溶沸点:渐高;化学性质
11、:原子得电子能力:渐弱;阴离子失电子能力;渐强单质氧化性:渐弱;阴离子还原性:渐弱元素的非金属性:渐弱结构决定性质,培养学生的归纳推理能力。3、特殊性:氟(1)2F2+2H2O4HF+O2(2)氟能同稀有气体Xe,Kr形成化合物碘:演示:显色反应:碘+淀粉呈蓝色讨论砹(At)是卤素中原子序数最大的元素,根据卤素单质物理性质、结构和化学性质的变化规律,推导砹可能的结构和性质: (1)砹单质的分子式为At2(2)At2 为白色固体(3)砹的原子半径比碘大(4)HAt很稳定(5)At易溶于有机溶剂培养学生从普遍性到特殊性的认识。2、氯化碘(ICl)的化学性质和氯气相似,预计它和水A. HI 和HCl
12、OB.HCl 和HIOC.HIO和 HClO3D.HClO和 HIO1、甲、乙、丙三种无色溶液各含有一种X-(X-为Cl-、Br-或I-)离子,向甲中加淀粉溶液和氯水,则溶液变为橙色,再加入丙溶液,颜色无明显变经,则甲、乙、丙三种无色溶液依次含有:()A. Br- Cl- I-B. Br- I- Cl-C .I- Br- Cl- D. Cl- I- Br-第一节 氯气教学目标:知识技能:了解氯气的物理性质、用途;认识氯气能溶于水,掌握氯气与水的反应,了解氯水的漂白性和不稳定性;掌握氯气与碱的反应及漂白粉的制法和漂白原理。能力目标:通过对实验方案的方针,培养学生的实验能力、观察能力以及根据实验事
13、实进行分析推理的能力。培养学生搜集信息,处理信息的能力。培养学生理论联系实际的能力。情感目标:通过小组实验、讨论,创设情境激发学生的学习兴趣。培养学生严谨求实,勇于探索的科学态度;对学生进行辩证唯物主义教育和环保教育。教学重点:氯气的化学性质。教学难点:氯气与水反应。教学用具:计算机、实物投影、有关的化学试剂和仪器。教学过程设计教师活动学生活动设计意图引入学生在课下收集有关氯气资料进行展示和交流展示、交流倾听,思考。充分调动学生学习的积极性和主动性,使学生对氯气有一定的感性认识。培养学生搜集信息的能力。提问通过对氯气资料的收集,你们对氯气有了哪些认识?板书一、氯气的物理性质二、氯气的用途从资料
14、中提炼、归纳氯气的物理性质及用途。培养学生加工信息、处理信息的能力。教师活动学生活动设计意图提问你们还想了解与氯气有关的哪些问题?过渡为了解决这些问题,研究氯水的成份和性质是十分必要的。课题用已给出的试剂、仪器,设计实验方案,验证氯水的主要成份和性质。分组实验,组间交流,进行分析和筛选,得出:氯水呈淡黄绿色且有刺激性气味说明氯水中有Cl2加入AgNO3溶液,出现白色沉淀一说明氯水中有Cl-加入石蕊试液,先变红,后褪色说明氯水中有H+和具漂白性质。促进学生之间相互交流,充分发挥学生的主体作用,培养学生勇于探索的科学态度。培养学生实验能力、观察能力和发散思维能力。培养学生根据实验进行分析推理的能理
15、。设问如何用实验的方法研究是氯气有漂白性,还是次氯酸有漂白性,或是二者都有?演示实验将干燥、湿润的红纸分别放入氯气瓶中。点拨次氯酸具有漂白性,这是其强氧化性的表现。讨论、交流方案:取两条蓝色石蕊试纸分别放入装有氯气的大试管和装有氯水的大试管中,观察有无褪现象。观察现象并得出:氯气没有漂白性。次氯酸具有漂白性。培养学生设计实验能力和观察能力。进行透过现象看本质的辩证唯物主义的教育。过渡次氯酸除具有漂白性以外还具有其它特性吗?课件演示次氯酸见光分解观看课件认识次氯酸的不稳定性。投影三、氯气的化学性质1、与水反应Cl2+H2O=HClO+HCl2HClO=2HCl+O2总结氯气、氯水、次氯酸的有关性
16、质听讲、记笔记。知识点落实。发挥教师的主导作用。教师活动学生活动设计意图讨论实验中为什么用氢氧化钠溶液收多余氯气?氢氯化钠溶液为什么能吸收氯气?板书2、氯气与碱反应提问书写Cl2和NaOH反应的化学方程式。投影Cl2+H2O=HClO+HClNaOH +HCl=NaCl+H2O+)HClO+ NaOH =NaClO+H2OCl2+2NaOH=NaCl+NaClO+H2O讨论后,抽象概括:NaOH能中和氯水中HCl、 HClO,因消耗了酸,使得氯气与水的反应趋于完全。书写方程式引出氯气与碱反应。理解氯气与碱反应的原理,便于记忆复杂的化学反应方程式。讨论氯气厂装液氯的钢瓶一旦发生氯气泄漏,可采取哪
17、些及时有效的防毒措施?投影刘伯承元帅在淮海战役时编写的防毒歌。思考、讨论观看,欣赏,思考进行安全教育环保教育。培养学生学以致用,理论联系实际的能力。激发学生的学习兴趣。前后呼应练习书写Cl2和Ca(OH)2反应的化学方程式。投影2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O介绍次氯酸具有漂白作用,但因其不稳定,不易保存和使用,工业上利用Cl2和Ca(OH)2反应原理制取漂白粉。书写方程式巩固氯气与碱反应方程式的书写。教师活动学生活动设计意图阅读课本提问1、漂白粉的主要成份?有效成份?漂白原理?2、游泳池中漂白粉,并未加酸,为何也有消毒作用?3、如何保存漂白粉?投影Ca(Cl
18、O)2+H2O+CO2=CaCO3+2HClO回答:主要成分是CaCl2 和Ca(ClO)2,有效成份是Ca(ClO)2,Ca(ClO)2与较其强的酸反应生成HClO而发挥消毒作用和漂白作用。回答:漂白粉与空气中H2O和CO2作用生成HClO;回答:密闭、避光保存。培养学生自学能力以及运用所学知识分析问题解决问题的能力提问上述反应证明了HClO的什么性质。讨论实验室为何不用氢氧化钙吸收 氯气?工业上为何不用氢氧化钠制漂白粉?次氯酸是比碳酸还弱的酸。从吸收的效率、原料的来源、经济收益等方面进行讨论。巩固HClO的特质。培养学生具体问题具体分析的能力。提问通过这节课的学习你对氯气有了哪些新的认识?
19、氯气能与水、碱等化合物反应,从而认识到氯气是一种化学性质非常活泼的非金属单质。回顾本节课的重点内容。小节正当使用氯气的性质,可以帮助人类,反之则可以毁灭人类。我们应学好化学,为人类造福。听讲教育学生认识问题要一分为二作业记作业巩固本课时重点内容氯气相关资料资料一:“伊普尔毒雾”的挑战在比利时的佛兰德省,有一座名叫伊普尔的城镇,城镇的西南有一块高地。第一次世界大战期间,协约国的联军占据了这块具有战略意义的高地。因此德军发动了多次的猛烈攻势,包括用大炮狂轰滥炸、组织大兵团冲击等,都未能奏效。1915年4月22日下午,德军的大炮又向高地轰击。联军官兵立即跳入战壕,像往常一样,予以有力的回击。90分钟
20、后,德军的炮击停止了,有的士兵打喷嚏,有的咳嗽,有的流眼泪,有的鼻子、喉咙发痒,有的兼有这些症状。还有许多官兵直叫胸闷,并很快倒在阵地上。阵地上一片忙乱。就在这时,德军发起了疯狂的反攻。联军失去了往日的风采,毫无抵抗力,防线崩溃了。原来,德军使用了可以致人于死地的化学毒气氯气。这次“毒袭”的发明者是德国化学家费里茨哈伯.这是人类战争史上第一次林规模地使用化学武器。费里茨.哈伯曾在德国的卡尔斯鲁大学和柏林大学当过教授,在科学研究方面有一定的成果。他曾发明氨的空气合成法,为以后的固定氮工业和氮肥工业奠定了基础。为此,他在1918年获得诺贝尔化学奖。但同时,他也是一名双手沾满鲜血的战犯,他鼓动德军总
21、参谋部实施了使用化学氯气的作战方案,命令士兵在600米长的前线阵地上,每隔40米就构筑一个土台,并在土台上埋没了40个装有氯气的钢瓶。1915年4月22日下午,微风从德军阵地吹向高地。借着风势,德军把毒气放到联军阵地,这就是著名的“伊普尔毒雾”。在这次毒袭中,仅英法联军就有1.5万人中毒,5000人丧生。正是氯气开创了将化学毒物作为武器用于战争的先例。资料二:刘伯承元帅在淮海战役时编写的防毒歌。阵地准备石灰水,肥皂毛巾带身边;发现敌人放毒气,手巾纵横叠六道;上面撒上石灰水,皂水用来更保险;撒好蒙住口与鼻,毒气不能往里钻。资料三:儿童游泳集体氯气中毒事件中新网南昌:南昌发生一起儿童游泳集体氯气中
22、毒中件。5日晚9点05分左右,有40名少儿游泳队员正在南昌市体校游泳馆进行训练,馆内一工作人员操作失误,在泳池内还有队员的情况下,将净化水质的氯气管道打开消毒,当即导致靠近管道的多名小选手出现呕吐、头晕、四肢无力现象。在场工作人员立刻将11名症状较重的儿童送往医院抢救,大部分中毒儿童脱离生命危险。在这些中毒的孩子中,年龄最大的9岁,最小的只有6岁。资料四:温州氯气中毒事件1979年9月7日下午1时55分,温州电化厂液氯工段的工人正在充装作业,一只半吨重充满氯的钢瓶突然爆炸。随着震天的巨响大量液氯气体,形成巨大黄绿色气柱冲天而起,蘑菇状,高达40余米,其它液氯钢瓶被引爆或击穿,大量液氯外泄。时值
23、东北风,氯气迅速呈60度扇形向西北扩散,共有32个居民区和6个生产队受到污染。1208人受到氯气危害,779人中毒,死亡59人(均为重污染区的军民,本厂职工逆风疏散到一高坡上,故无中毒致死者)。中毒患者表为胸闷、咳嗽、呼吸困难、头痛、恶心、呕吐、无力等,严重者可出现大量白色中粉红色泡沫痰、烦躁不安,昏迷,部分患者出现严重的紫绀;少数患者发现时已经死亡。防化、消防人员用大量喷水抑制逸出氯气的扩散,关闭了所有储、管道的阀门。厂区周围人员全部疏散,共有8万人撤离了危险区。根据现场的具体情况及模式似试验,最后证实此次事故是由于氯化石蜡倒入钢瓶内,引起的化学性爆炸。资料五:中毒原理(1)氯气在呼吸道内遇
24、水可生成氯酸和盐酸(HCl)。次氯酸可穿透细胞膜,损伤支气管粘膜,肺胞上皮细胞,使通透性增强,引起呼吸道粘膜损伤、肺水肿、支气管炎或肺炎、高烧、休克等,严重者可昏迷。也可因喉头水肿窒息死亡。(2)次氯酸可与多种含硫氢基的酶起反应,抑制其活性,扰乱机体代谢。(3)氯气刺激呼吸道粘膜感受器,反射性引起支气管平滑肌痉挛。(4)高浓度氯气刺激可引起迷走神经兴奋,导致喉头痉挛或心跳骤停。资料六:氯气用途重要化工原料。大量用于制造有机合成的中间体(如氯苯、氯化萘等)、溶剂(如氯代烷类)、盐酸、漂白粉以及制造药物(如氯胺T等)和农药;在生产塑料聚氯乙烯、合成纤维氯纶、合成橡胶氯丁橡胶等合成材料时也需用多量氯气。氯气液化后压入钢瓶常供纸浆漂白、纺织品漂白、自来水消毒杀菌、制次氯酸钠、从卤水中提炼溴和碘以及某些金属或硅的提纯冶炼等。
- 温馨提示:
1: 本站所有资源如无特殊说明,都需要本地电脑安装OFFICE2007和PDF阅读器。图纸软件为CAD,CAXA,PROE,UG,SolidWorks等.压缩文件请下载最新的WinRAR软件解压。
2: 本站的文档不包含任何第三方提供的附件图纸等,如果需要附件,请联系上传者。文件的所有权益归上传用户所有。
3.本站RAR压缩包中若带图纸,网页内容里面会有图纸预览,若没有图纸预览就没有图纸。
4. 未经权益所有人同意不得将文件中的内容挪作商业或盈利用途。
5. 装配图网仅提供信息存储空间,仅对用户上传内容的表现方式做保护处理,对用户上传分享的文档内容本身不做任何修改或编辑,并不能对任何下载内容负责。
6. 下载文件中如有侵权或不适当内容,请与我们联系,我们立即纠正。
7. 本站不保证下载资源的准确性、安全性和完整性, 同时也不承担用户因使用这些下载资源对自己和他人造成任何形式的伤害或损失。
