 九年级化学第九单元中考知识点网络及常见错误
九年级化学第九单元中考知识点网络及常见错误


《九年级化学第九单元中考知识点网络及常见错误》由会员分享,可在线阅读,更多相关《九年级化学第九单元中考知识点网络及常见错误(6页珍藏版)》请在装配图网上搜索。
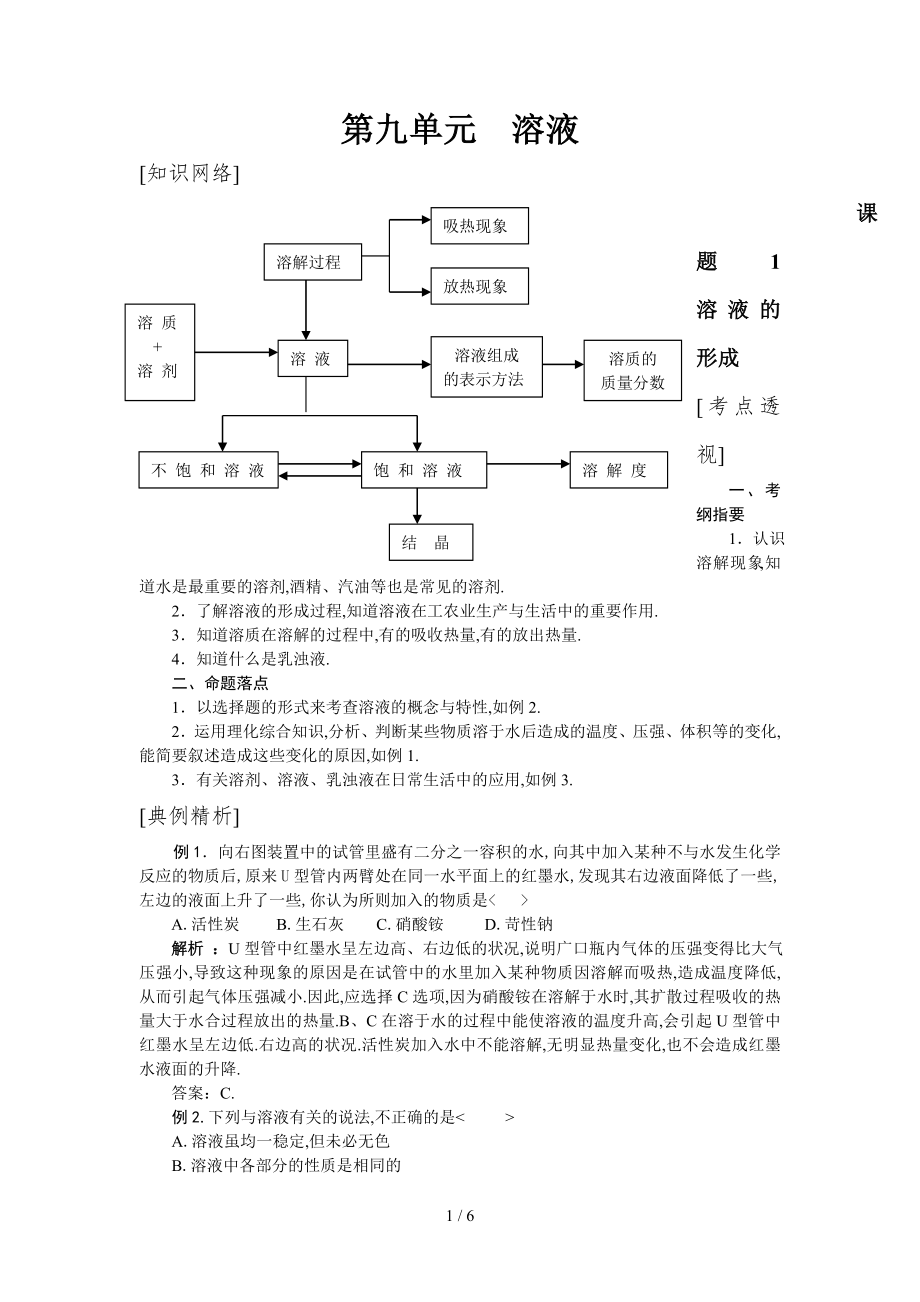
1、第九单元 溶液不 饱 和 溶 液饱 和 溶 液溶 解 度结 晶溶 质+溶 剂溶 液溶液组成的表示方法溶质的质量分数溶解过程放热现象吸热现象知识网络课题1溶液的形成考点透视一、考纲指要1认识溶解现象,知道水是最重要的溶剂,酒精、汽油等也是常见的溶剂.2了解溶液的形成过程,知道溶液在工农业生产与生活中的重要作用.3知道溶质在溶解的过程中,有的吸收热量,有的放出热量.4知道什么是乳浊液.二、命题落点1以选择题的形式来考查溶液的概念与特性,如例2.2运用理化综合知识,分析、判断某些物质溶于水后造成的温度、压强、体积等的变化,能简要叙述造成这些变化的原因,如例1.3有关溶剂、溶液、乳浊液在日常生活中的应
2、用,如例3.典例精析例1向右图装置中的试管里盛有二分之一容积的水,向其中加入某种不与水发生化学反应的物质后,原来U型管内两臂处在同一水平面上的红墨水,发现其右边液面降低了一些,左边的液面上升了一些,你认为所则加入的物质是A.活性炭 B.生石灰 C.硝酸铵 D.苛性钠解析 :U型管中红墨水呈左边高、右边低的状况,说明广口瓶内气体的压强变得比大气压强小,导致这种现象的原因是在试管中的水里加入某种物质因溶解而吸热,造成温度降低,从而引起气体压强减小.因此,应选择C选项,因为硝酸铵在溶解于水时,其扩散过程吸收的热量大于水合过程放出的热量.B、C在溶于水的过程中能使溶液的温度升高,会引起U型管中红墨水呈
3、左边低.右边高的状况.活性炭加入水中不能溶解,无明显热量变化,也不会造成红墨水液面的升降.答案:C.例2.下列与溶液有关的说法,不正确的是A.溶液虽均一稳定,但未必无色 B.溶液中各部分的性质是相同的C.如果温度不变,水不蒸发,食盐溶液久置也不会分离出食盐晶体D.一种溶液中只能含一种溶质解析:溶液具有以下特征:1各部分的组成性质完全相同,外观看起来均匀、透明、澄清,这一特征为均一性.2只要不改变溶液的条件,如温度、压强等,不蒸发水分,溶液长期放置也不会有溶质分离析出,这一特征为稳定性.因此,对于题中有关溶液的叙述,很容易判断出B、C是正确的.溶液是均一、透明的,但不一定无色,如CuSO4溶液就
4、是蓝色的,FeCl3溶液是黄色的,由此可判断A也是正确的.一种溶液可同时溶解多种溶质,形成混合溶液,故D的说法不正确.答案:D.例3生活中的洗涤问题大都与化学知识有关.下列有关说法不正确的是A厨房洗涤剂可使餐具上的油污乳化B汽油可溶解衣服上的油渍C食醋可用来除去热水瓶中的水垢D自来水可溶解掉铁栅栏上的铁锈解析:洗涤离不开溶剂、溶液、乳浊液,本题所考查的正是这些物质的应用是否恰当的问题.生活经验告诉我们,餐具上的油污是完全可以用厨房洗涤剂乳餐洗净来洗掉的,其道理就在于这些洗涤剂能使油污分散成细小的液滴一种乳浊液,这些细小的液滴可随水流走;汽油作为一种有机溶剂,能溶解许多的有机物,衣服上的油渍就完
5、全可以溶解在汽油中,之后随汽油的挥发而被除掉;食醋的主要成分是醋酸,能和热水瓶中的水垢主要成分是碳酸钙发生化学反应,从而形成能溶于水的物质而被除去;铁栅栏上的铁锈成分主要是氧化铁,由于它不溶于水,因此用自来水是不可能将铁锈溶解掉的,这样做,只能进一步加快铁栅栏的锈蚀.答案:D.常见误区1认为溶液一定是液态的物质.根据溶液的概念,清新的空气、有色玻璃等也属于溶液,因为它们都是由一种物质分散到另一种物质里所形成的均一的稳定的混合物.2认为一种溶液中只含有一种溶质.实际上,自然界、实验室里的不少的溶液都是混合溶液,即在溶剂里同时溶解了多种溶质.如例2.3有的同学在分析由于溶质的溶解造成的溶液温度升降
6、的时候,只强调扩散或水合两个过程的其中之一,为我所用,不能全面、客观的进行分析.如硝酸铵溶于水时溶液温度降低,就不能说是由于扩散而吸收了热量,而是因为扩散过程吸收的热量少于水合过程放出的热量,这才造成了溶液温度的降低.如例1.4认为无色透明的、均一的、稳定的液体都是溶液.应注意:溶液不一定没有颜色,其类别一定属于混合物. 基础演练课题2溶解度考点透视一、考纲指要1记住饱和溶液、不饱和溶液的概念,知道饱和溶液与不饱和溶液在一定条件下是可以相互转化的.2了解溶解度的含义,知道溶解度的相对大小与溶解性的关系.3认识溶解度曲线,能利用溶解性表或溶解度曲线查阅有关物质的溶解性或溶解度.4认识影响气体溶解
7、度大小的因素.二、命题落点1以选择、填空等形式考查饱和溶液、不饱和溶液的概念与其相互转化的条件和方法,如例1.2对溶解度概念的理解程度的考查,对影响溶解度因素的分析和认识的考查,如例2.3对于溶解度曲线的认识与利用能力以与看图、识图能力的考查,如例3.4影响气体物质溶解度的因素的分析与以此解释生活中的某些现象,如例4.例1下列有关固态物质饱和溶液的说法正确的是 A.饱和溶液就是不能继续溶解溶质的溶液B.同一溶质的饱和溶液一定比不饱和溶液浓C.将热饱和溶液降温时,一定会析出晶体D.饱和溶液在一定条件下可转化为不饱和溶液解析 :此题主要考查饱和溶液的概念.在理解这个概念时,要注意溶质为固态如下几个
8、关键:一定温度、一定量的溶剂;同种溶质溶解的量不能继续增加但其它溶质可以继续溶解.比较同种溶质的饱和溶液、不饱和溶液的浓稀,一定要在同温下进行比较.如A中未指明一定温度、一定量的溶剂,也未指明是不是同种溶质,故不正确.B中未指明相同温度,也不正确.C中因为并不是所有的物质的溶解度都是随温度的降低而减小的,有些溶质的溶解度如氢氧化钙是随温度升高而减小的,故C不正确.答案:D.例220时食盐的溶解度是36g.根据这一条件与溶解度的含义,判断下列说法哪一种是正确的 A.100g水溶解36g食盐恰好能配成饱和溶液 B.200C时,100g食盐饱和溶液里含有36g食盐 C.200C时,把136g食盐饱和
9、溶液蒸干,可得到36g食盐 D.饱和食盐水溶液中溶质、溶剂、溶液的质量比为36:100:136解析:本题重在考查大家对于溶解度概念的理解.溶解度这一概念有如下四个要点:一定的温度;100溶剂;达到饱和状态;质量单位.根据溶解度的概念并结合题给条件可知,A的说法是不正确的,原因在于没有指明温度这一条件;按照溶解度的含义,在20时将36g食盐溶于100水中恰好达到饱和状态,这时所得到的食盐饱和溶液的质量为136;相反,如果将这136的食盐饱和溶液蒸干,一定就能得到36食盐;同样,由于在136食盐饱和溶液里含有36食盐,那么,在100食盐饱和溶液里就不可能含有36食盐了肯定比36要少.至于饱和食盐水
10、溶液中溶质、溶剂、溶液的质量之比,如果没有温度这一前提条件,就无法进行相应的求算.答案:C.例3 A、B两种固体物质的溶解度曲线如图所示.请回答:1时,A物质的溶解度为g.2时,A、B两种物质的溶解度填相同或不同.3我国有些地区有一种说法:冬天捞碱,夏天晒盐.这里的碱是指Na2CO3,盐是指NaCl.那么,图中填A或B的溶解度曲线与Na2CO3的溶解度曲线相似.人们用上述方法从盐湖中捞得的Na2CO3会含有少量的NaCl.某研究性学习小组称取含NaCl的Na2CO3固体12.5g,将其配制成溶液,再向其中逐滴加入足量的稀盐酸,使气体完全放出,共收集到4.4g CO2气体,则原固体中Na2CO3
11、的质量分数为多少?.解析:本题重在考查大家对于溶解度曲线的认识与利用的能力,同时涉与到根据化学方程式的计算问题.我们知道,溶解度曲线是以实验数据为依据,用纵坐标表示溶解度,横坐标表示温度,绘出的物质的溶解度随温度变化的曲线.利用溶解度曲线,可以查出某物质在不同温度下的溶解度;也可以查出同一温度下不同物质的溶解度;还可以比较不同的物质在同一温度下溶解度的大小;若两条曲线相交,则其交点表示在该温度下这两种物质的溶解度大小相等.当然,根据溶解度曲线还能看出某物质的溶解度受温度变化的影响情况.由所给A、B两种固体物质的溶解度曲线可以看出,时,A物质的溶解度为a g;时,A、B两种物质的溶解度是相同的;
12、既然冬天能捞碱,这就说明碳酸钠的溶解度受温度的影响是比较大的,因此其溶解度曲线应当与A相似;通过根据碳酸钠与盐酸反应的化学方程式不难求得原固体中Na2CO3的质量分数为84.8.例4生活中的下列现象不能说明气体溶解度随温度升高而减小的是 A.烧开水时,沸腾前有气泡逸出B.喝下汽水感到有气体冲出鼻腔C.揭开啤酒瓶盖,有大量的泡沫溢出D.夏季黄昏,池塘里的鱼常浮出水面解析:气体物质在水中的溶解度受温度与压强的影响,温度越高,气体的溶解度越小;压强越大,气体的溶解度越大.根据影响气体物质溶解度的的因素,可以解释生活中的某些现象;反之,通过某些现象也可以说明外界条件对于气体溶解度的影响.对比四个选项不
13、难知道,A、B、D都说明了气体的溶解度是随着温度的升高而减小的,唯有C表明了在压强减小时,气体的溶解度也变小,与题干的要求不符,这正是本题的答案.答案:C.常见误区1忽视饱和溶液、不饱和溶液、溶解度等概念的前提条件,未能真正理解这些概念的含义,从而导致在对某些说法的判断上不能作出正确的选择.如例1、例2.2对溶解度曲线的含义与利用缺少全面的认识,方法上不得要领.要把握住溶解度曲线的交点的意义,知道比较不同物质的溶解度大小需要在相同的温度下进行,理解曲线的陡、缓反映的是受温度影响的情况.如例3.3审题不细,特别是对选择题的要求看得不够认真,如把关于的说法正确的是看成是关于的说法不正确的是,或把不
14、能说明的是看作为能说明的是,如例1、例4等.课题3溶质的质量分数考点透视一、考纲指要1知道溶质的质量分数是是溶质的质量与溶液的质量之比.2能进行有关溶质质量分数的简单计算.3初步学会配制一定溶质质量分数的溶液.二、命题落点1以选择、填空等形式来考查有关溶质质量分数的简单计算.如例1.2联系生活实际,考查溶液知识与其有关计算,如例2.3分析、判断不同溶质溶于水时所引起的溶质质量分数的变化情况,如例3.4依据公式进行溶液配制实验误差的分析,如例4.典例精析例1将一瓶80g 溶质质量分数为10%的NaCl溶液平均分为2等份,每份溶液中溶质的质量分数为;若将其中的一份溶液中溶质的质量分数减小一半,应加
15、水g,若将另一份溶液中溶质的质量分数增大一倍,应加入NaClg.解析:根据溶液的均一性可知,无论将原来的溶液怎么样来分,只要条件不改变,其溶质的质量分数是不会发生变化的.增加溶剂的质量能使溶质的质量变小,加入多少水才能使40原溶液质量的一半10%的NaCl溶液的溶质质量分数减小一半即5呢?显然,所加水的质量应该和对应溶液的质量一样多40;通过加入溶质的方法肯定能使溶液中溶质的质量分数增大,那么,所加入的溶质质量怎样计算呢?很简单:依据溶质质量分数的计算公式.但要注意,加入这部分溶质后,不仅能使溶质的质量增大,同样也使溶液的质量增大.若设加入的溶质质量为,则由题意可得:40104020解之,5.
16、答案:10%;40;5 . 例22003年南京市中考题日常生活中我们要科学地节约用水.现有一件刚用洗涤剂洗过的衣服,拧干后湿衣服上残留的溶液为100g,其中洗涤剂的质量分数为1,则湿衣服上残留的洗涤剂质量为 g.现用5700g清水对这件衣服进行漂洗,有以下两种漂洗方法假设每次拧干后湿衣服仍残留100g溶液: 方法一:用5700g清水漂洗,拧干后残留在衣服上的洗涤剂质量为用分数表示,下同g; 方法二:用5700g清水均匀分成质量相等的三份每份1900g,分三次漂洗: 第1次,用1900g清水漂洗,拧干后残留在衣服上的洗涤剂质量为g; 第2次,用1900g清水漂洗,拧干后残留在衣服上的洗涤剂质量为
17、g; 第3次,用1900g清水漂洗,拧干后残留在衣服上的洗涤剂质量为g. 由以上计算分析,用相同质量的水漂洗衣服,是一次漂洗效果好,还是将水分成三份,分三次漂洗效果好? 解析:这是一道密切联系生活实际的简单计算题.试题旨在通过简单计算,使大家明白并掌握节约用水的一种方法.通过这种方法的介绍,引导我们进一步树立节约水、爱惜水的观念,做到合理地利用水、科学地节约和保护水.其实,该题的实质是关于溶质溶解、溶液稀释的计算.它以日常生活中的小事为背景,将漂洗衣服时为什么要少量多次的科学道理让学生通过计算加以感受,既考查了分析与计算能力,又进行了节约用水的方法教育,真可谓匠心独具,是一道难得的好题.解答时
18、要注意:题中拧干后湿衣服上残留的溶液仍为100g,这就意味着不论用什么方法、进行哪一次漂洗,这100g溶液始终应跟随在计算的过程中.如用方法2进行第一次漂洗,漂洗时所用水的总质量就应当是:1900g100g2000g,拧干后残留在衣服上的洗涤剂质量的质量分数为:100g12000g0.05,因此,残留在衣服上的洗涤剂的质量为:0.05100g1/20 g.例3在t 时,将 10 g某纯净物完全溶解在90 g水中,你认为所得溶液中溶质的质量分数可能出现哪些情况?试举例说明.解析 :解答此题,既要掌握溶质质量分数的计算公式,又要熟悉物质溶于水的三种情况:物质溶解于水后,溶质本身没变,像氯化钠、硝酸
19、钠等,溶质的质量为 10 g,溶质的质量分数:100=10.物质溶于水时,与部分水发生化合反应,溶质不再是加入的物质,而是化合后生成的新物质,这时其质量肯定大于 10 g,因此所得溶液中溶质的质量分数也一定大于 10.如三氧化硫溶于水就是这种情况.结晶水合物溶于水时,结晶水转化为溶剂水,这样一来,溶液中溶质的质量小于 10 g,而溶剂质量却大于90 g,因此,溶质的质量分数必定小于 10.如兰矾CSO45H2O溶于水就是这种情况.例4配制10%的氯化钠溶液时,不会引起溶液中氯化钠的质量分数偏小的是A用量筒量取水时仰视读数 B配制溶液的烧杯用少量蒸馏水润洗C氯化钠晶体不纯 D转移已配好的溶液时,
20、有少量溶液溅出解析:配制一定溶质质量分数的溶液是一个定量实验,所用试剂不当或操作错误都会给实验结果带来一定的影响.影响的结果如何,我们是可以通过溶质质量分数的计算公式来作出判断的.对于A,这样量取的水的体积要比理论上的体积大一些,其质量也相应变大,因此配得的溶液中氯化钠的质量分数将偏小;对于B,此时相当于所用水的质量增大了,会引起溶液中氯化钠的质量分数偏小;当氯化钠晶体不纯时,相当于溶质的质量减小,这样就会引起溶液中氯化钠的质量分数偏小;在将溶液配制完成之后,即便有少量溶液溅出,但不会影响其中氯化钠的质量分数.答案:D.常见误区1认为只要加入溶质就能使溶液中溶质的质量分数变大.仔细想一想,如果溶液本来就是某一定温度下的饱和溶液,再加入溶质后还能继续溶解吗?此时溶质的质量分数还会变大吗?答案是显而易见的.2在计算加入溶质所得溶液的质量分数时,只看到溶质质量的增加,未想到溶液的质量也同样增加,从而导致计算结果的错误.3不能全面考虑物质溶于水时所发生的变化,认为加入水中的物质都是溶质,生搬硬套公式进行计算.如例3.4分析配制一定溶质质量分数的溶液所可能造成的误差时,找不准正确的判断依据,只凭主观想像加以判断.如例4.6 / 6
- 温馨提示:
1: 本站所有资源如无特殊说明,都需要本地电脑安装OFFICE2007和PDF阅读器。图纸软件为CAD,CAXA,PROE,UG,SolidWorks等.压缩文件请下载最新的WinRAR软件解压。
2: 本站的文档不包含任何第三方提供的附件图纸等,如果需要附件,请联系上传者。文件的所有权益归上传用户所有。
3.本站RAR压缩包中若带图纸,网页内容里面会有图纸预览,若没有图纸预览就没有图纸。
4. 未经权益所有人同意不得将文件中的内容挪作商业或盈利用途。
5. 装配图网仅提供信息存储空间,仅对用户上传内容的表现方式做保护处理,对用户上传分享的文档内容本身不做任何修改或编辑,并不能对任何下载内容负责。
6. 下载文件中如有侵权或不适当内容,请与我们联系,我们立即纠正。
7. 本站不保证下载资源的准确性、安全性和完整性, 同时也不承担用户因使用这些下载资源对自己和他人造成任何形式的伤害或损失。
