 生物工程下游技术复习题
生物工程下游技术复习题


《生物工程下游技术复习题》由会员分享,可在线阅读,更多相关《生物工程下游技术复习题(14页珍藏版)》请在装配图网上搜索。
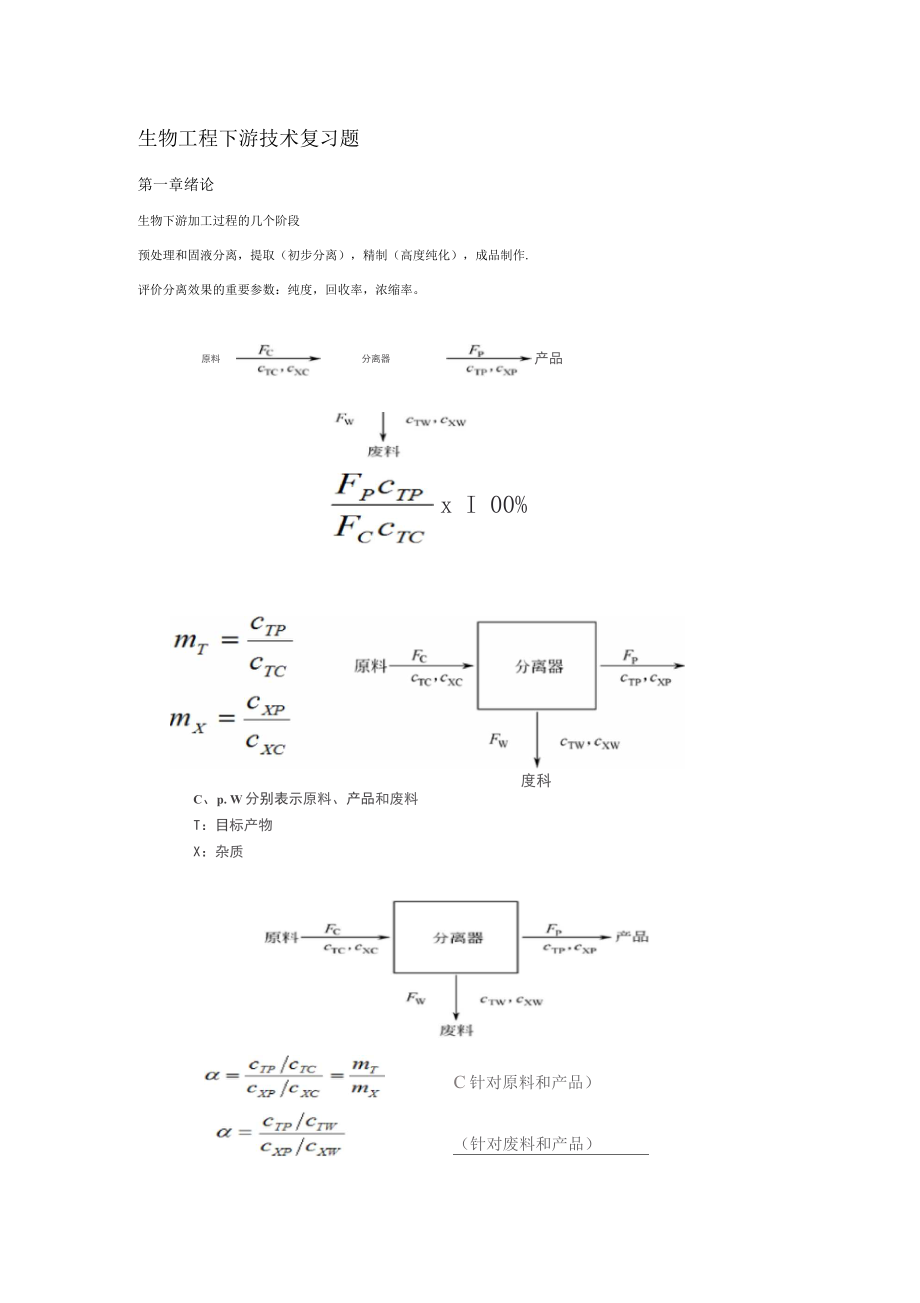
1、生物工程下游技术复习题第一章绪论生物下游加工过程的几个阶段预处理和固液分离,提取(初步分离),精制(高度纯化),成品制作.评价分离效果的重要参数:纯度,回收率,浓缩率。原料分离器产品x I 00%度科C、p. W分别表示原料、产品和废料T:目标产物X:杂质C针对原料和产品)(针对废料和产品)第二章发酵液预处理和固液分离主要名词:凝聚、絮凝凝聚:指在电解质作用下,由于胶粒之间双电层电排斥作用降低,电位下降,而使胶体体系不稳定的现象;絮凝:指在某些高分子絮凝剂存在下,基于桥架作用,使胶粒形成较大絮凝团的过程。1 .改变发酵液过滤特性的方法调酸(等电点),热处理,电解质处理,添加凝聚剂,添加表面活性
2、物质,添加反应剂冷冻解冻,添加助滤剂2 .发酵液的相对纯化(1)高价无机离子的去除方法L Ca2+草酸、草酸钠.f形成草酸钙沉淀(注意回收草酸);三聚磷酸钠,一形成三聚磷酸钠镁可溶性络合物;3. Fe2+黄血盐,f普鲁士兰沉淀3K4Fe(CN)6 + 4F9+ = Fe4Fe(CN)6p + 12K+(2)杂蛋白的去除方法沉淀法,变性法,吸附法。3常用的固液分离方法:重力沉降,浮选,旋液分离,介质过滤,离心。(1)离心离心机种类:碟片式。管式。倾析式。(2)过滤(澄清过滤,滤饼过滤)过滤机种类:按推动力分为 4种重力过滤,加压过滤,真空过滤,离心过滤。板框压滤机,真空转鼓过滤机第三章细胞破碎和
3、包涵体复性细胞破碎的主要方法和适用对象,了解基本机理方法: 珠磨法原理: 进入珠磨机的细胞悬浮液与极细的玻璃小珠、石英砂、 氧化铝等研磨剂(直径小于1mm )一起快速搅拌或研磨,研磨剂、珠子与细胞之间的互相剪切、碰撞,使细胞破碎, 释放出内含物。在珠液分离器的协助下,珠子被滞留在破碎室内,浆液流出从而实现连续操作。高压匀浆法原理: 利用高压使细胞悬浮液通过针形阀, 由于突然减压和高速冲击撞击环使细胞破碎, 细胞悬浮液自高压室针形阀喷出时, 每秒速度高达几百米, 高速喷出的浆液又射到静止的撞击环上, 被迫改变方向从出口管流出。 不适用范围 : 易造成堵塞的团状或丝状真菌,较小的革兰氏阳性菌,含有
4、包含体的基因工程菌(因包含体坚硬,易损伤匀浆阀)珠磨法 固体剪切作用 可达较高破碎率, 可较大规模操作, 大分子目的产物易失活, 浆液分离困难高压匀浆法液体剪切作用性菌超声破碎法液体剪切作用X-press 法固体剪切作用可达较高破碎率, 可大规模操作, 不适合丝状菌和革兰氏阳对酵母菌效果较差, 破碎过程升温剧烈, 不适合大规模操作破碎率高,活性保留率高,对冷冻敏感目的产物不适合酶溶法 酶分解作用 具有高度专一性,条件温和,浆液易分离,溶酶价格高,通用性差化学渗透法 改变细胞膜的渗透性具一定选择性, 浆液易分离, 但释放率较低, 通用性差渗透压法渗透压剧烈改变破碎率较低,常与其他方法结合使用冻结
5、融化法反复冻结-融化破碎率较低,不适合对冷冻敏感目的产物干燥法 改变细胞膜渗透性条件变化剧烈,易引起大分子物质失活第四章 沉淀法1.蛋白质的表面特征蛋白质组成20 种氨基酸构成的两性高分子电解质,包括疏水性氨基酸和亲水性氨基酸蛋白质折叠趋势疏水性氨基酸:向内部折叠的趋势亲水性氨基酸:分布于蛋白质外表面的趋势结果在蛋白质三维结构中仍会有部分疏水性氨基酸残基暴露于表面,在蛋白质表面形成一定的疏水区蛋白质表面由不均匀分布的荷电基团形成荷电区、亲水区和疏水区构成。蛋白质的溶解行为是一个独特的性质,由其组成、构象以及分子周围的环境所决定。一般而言,小分子蛋白质比起在化学上类似的大分子蛋白质更易溶解。2
6、.盐析法的原理和影响因素防止蛋白质凝聚沉淀的屏障蛋白质周围的水化层 可以使蛋白质形成稳定的胶体溶液。蛋白质分子间静电排斥作用。 (存在双电层)盐析类型(Ks盐析、3盐析)定义:蛋白质在高离子强度的溶液中溶解度降低、发生沉淀的现象称为“盐析” 。盐溶 :低盐情况,盐离子强度的增高,蛋白质溶解度增大。盐析 :高盐,盐离子强度增加,蛋白质溶解度减小。盐析法原理:形成离子对,部分中和了蛋白质的电性,排斥作用减弱而能相互靠拢,聚集起来。中性盐的亲水性比蛋白质大,使蛋白质脱去了水化膜,使其沉淀log S= 3 K s I式中S蛋白质的溶解度,g/L;I一离子强度等于1=1/2汇mizi2;mi 离子 i
7、的摩尔浓度;Zi 所带电荷;3常数,与盐的种类无关,但与温度、pH和蛋白质种类有关;Ks 盐析常数,与温度和 PH 无关,但与蛋白质和盐的种类有关。在一定的pH值及温度条件下,改变盐的浓度(即离子强度)达到沉淀的目的,称为“Ks”分级盐析法。(Ks盐析:固定pH,温度,改变盐浓度)在一定的离子强度下,改变溶液的pH值及温度,达到沉淀的目的,称为“3 ”分级盐析法。(3盐析:固定离子强度,改变 pH及温度。)3 .有机溶剂沉淀的基本原理和影响因素定义向水溶液中加入一定量亲水性的有机溶剂, 降低溶质的溶解度, 使其沉淀析出的分离纯化方法。原理 1 )加入有机溶剂后,会使水溶液的介电常数降低 ,导致
8、蛋白质分子之间的静电引力增加,从而使蛋白质发生聚集沉淀。 2 )由于使用的有机溶剂与水互溶,它们在溶解于水的同时从蛋白质分子周围的水化层中夺走了水分子,破坏了蛋白质分子的水膜,因而发生沉淀作用。影响因素:温度,pH值,样品浓度,中性盐浓度,某些金属离子。主要名词:盐溶、盐析、有机溶剂沉淀、等电点沉淀、聚合物沉淀4 .了解其他几种沉淀法第五章萃取主要名词:萃取、浸取、有机溶剂萃取、双水相萃取、反胶团和反胶团萃取、超临界流体和超临界流体萃取1 .萃取相关的几个参数萃取因素EVF 料液体积;Vs 萃取剂的体积;C1 溶质在萃取液的浓度;C2溶质在意?里受力 x 100% = - x 1 ()0% 原
9、始料液中溶质总量 + 1萃余相的浓度;K表观分配系数 萃余率:甲理论收率:IF1 ”1xlOO%-X100%+1E + 1洁霉素在20c和pH10.0时分配系数(丁醇/水)为18。用等量的丁醇萃取料液中的洁霉素, 计算可得理论收率E=18*1/1=18理论收率:94.7%若改用1/3体积丁醇萃取,理论收率:E = 18x = 6 l-(p = 5xlOO% = 85.7% 16 + 12 .工业萃取方式单级萃取多级萃取过程、计算经一级萃取后,经二级萃取后未被萃取的分率。i为经n级萃取后,未被萃取的分率为 S 1)1 -=1-产物收率为:(E + iy(石 + 1) J -1(E +红霉素在pH
10、 9.8时的分配系数(醋酸丁酯/水)为44.5,若用1/2体积的醋酸丁酯进行单级E 44,5 x 7 N 22.25萃取,则:J22 251 9=1x 100% = 95.7%理论收率22.25 + 1若用1/2体积的醋酸丁酯进行二级错流萃取,则1/4l = : = 445x = 11,12511 (P理论收率(11.125+1/ -1一(1L125 +1)(11.125 +1)xlOO% = 99.32%fp 1n级萃取后,萃余率为:-x 1OO%1 - = 1 理论收率为-1xlOO% =xlOO%青霉素在0c和pH2.5时的分配系数(醋酸丁酯/水)为35,若用1/4体积的醋酸丁酯进行二级
11、逆流萃取,1/4 = 35x3 = 8.75则:1n=2,理论收率 、L改为二级错流萃取,第一级用1/4体积的醋酸丁酯,第二级用1/10体积的醋酸丁酯,则i = 35x = 8.75 Q = 35 x = 3.51 11 0 = 1 %f? x 100% = 97.72%(8.75 + 1X3.5 + 1)2 .双水相萃取(1)常用双水相体系(无毒)聚乙二醇-葡聚糖聚乙二醇-无机盐系统(2)影响因素:与相体积无关,只取决于被分离物质本身的表面性质、温度和特定的双水相体系的性质。3 .反胶团萃取构成与机理、应用反胶团:是两性表面活性剂在非极性有机溶剂中亲水性基团自发的向内聚集而成的,内含 微小水
12、滴的,空间尺度仅为纳米级的集合型胶体。萃取机理:三步传质过程: 通过表面液膜扩散,从水相到达相界面;在相界面处溶质进入反胶团;含溶质的反胶团扩散进入有机相。反萃操作中溶质亦经历相似的过程,只是方向相反,在界面处溶质从反胶团释放出来。主要影响因素:水相的 pH值;盐离子的种类和浓度;温度 ;蛋白质的分子量和浓度表面活性剂应用:分离蛋白质或酶;分离氨基酸;分离抗生素;分离核酸;用于蛋白 质复性4 .超临界流体萃取定义:萃取技术,又称压力流体萃取、超临界气体萃取、临界溶剂萃取等,是利用处于临界 压力和临界温度以上的一些溶剂流体所具有特异增加物质溶解能力来进行分离纯化的技术。( 2 )萃取原理:在超临
13、界状态下,超临界流体具有很好的流动性和渗透性,将超临界流体与待分离的物质接触, 使其有选择性地把极性大小、 沸点高低和分子量大小的成分依次萃取出来。然后借助减压、升温的方法使超临界流体变成普通气体,被萃取物质则完全或基本析出,从而达到分离提纯的目的。( 3 ) SC-CO2 萃取的优点:(1)临界条件温和(Tc=31.06C Pc=7.2MPa),可以在3540 c的条件下进行提取,防止热敏 性物质的变质和挥发性物质的逸散。(2)在 CO2 气体笼罩下进行萃取,萃取过程中不发生化学反应;又由于完全隔绝了空气中的氧因此,萃取物不会因氧化或化学变化而变质。(3) 由于 CO2 无味、无臭、无毒、不
14、可燃、价格便宜、纯度高、容易获得 ,使用相对安全。(4) CO2 容易提纯与分离的,因此萃取物几乎无溶剂残留,也避免了溶剂对人体的毒害和对环境的污染。(5) CO2 扩散系数大而粘度小,大大节省了萃取时间,萃取效率高。缺点:设备投资大。第六章 膜分离主要名词:反渗透、水通量、截留率、截断分子量、浓差极化1 .膜的分类:按孔径大小:微滤膜、超滤膜、反渗透膜、纳滤膜按膜结构:对称性膜、不对称膜、复合膜按材料分:合成有机聚合物膜、无机材料膜多孔膜与致密膜:前者微滤膜、超滤膜、纳滤膜,后者反渗透膜、渗透蒸发2 .膜的分离机理孔模型: 以压力为推动力的膜分离技术, 按不同孔径来选择分离溶液中所含的微粒或
15、大分子,比膜孔径小的物质和溶剂(水)一起透过膜而较大的物质则被截留溶解扩散模型: 在推动力作用下, 渗透物质先溶解进入膜的上游侧, 然后扩散至膜的下游侧,扩散是控制步骤。例如气体的渗透分离过程中,推动力是膜两侧渗透物质的分压差优先吸附毛细管流动模型: 由于膜表面对渗透物的优先吸附作用, 在膜的上游侧表面形成一层该物质富集的吸附液体层。 然后, 在压力作用下通过膜的毛细管, 连续进入产品溶液中。3 .膜的性能参数(了解)影响截留率的因素分子形状:线状分子易透过,线 球;吸附作用:溶质吸附于膜孔壁上,降低膜孔有效直径浓差极化:在膜分离操作中,所有溶质均被透过液传送到膜表面上,不能完全透过膜的溶质受
16、到膜的截留作用,在膜表面附近浓度升高。这种在膜表面附近浓度高于主体浓度的现象称为浓度极化或浓差极化4 .膜污染及处理方法:类型:沉淀污染吸附污染生物污染处理:物理方法:等压冲洗;反冲洗;脉冲流动;超声波化学方法:化学清洗剂(稀碱、稀酸、酶、表面活性剂、络合物和氧化剂等)5 .主要的几种膜分离过程和应用微孔过滤(MF)、超滤(UF)、反渗透(RO)、纳滤(NF)、渗析(D)、电渗析(ED)、液膜(LM)及渗 透蒸发(PV)等6 .工业中常用的膜组件类型工业上应用的膜组件主要有中空纤维式、管式、螺旋卷式、板框式等四种型式。管式和中空纤维式组件也可以分为内压式和外压式两种。7 .液膜的组成和机理组成
17、:外相、膜相、内相(1)无载体液膜的分离机理选择性渗透:分离物在液膜中的溶解度差异 化学反应:为提高富集的效果,可使待富集成分在内水相发生化学反应以降低其浓度,促使迁移不断进行。 萃取和吸附(2)有载体液膜的分离机理一一“载体输送”第七章色谱分离1 .色谱分类两相分子的聚集状态分:液相,气相,超临界流体色谱固定相的形状分:柱色谱纸色谱 薄层色谱按分离机制分:分配色谱:利用分配系数的不同吸附色谱:利用物理吸附性能的差异离子交换色谱:利用离子交换原理空间排阻色谱:利用排阻作用力的不同2 .凝胶色谱:分离机理、分配系数的讨论、应用(主要:脱盐、分离、测分子量)定义:以多孔性凝胶填料为固定相,按分子大
18、小顺序分离样品中各个组分的液相色谱方法分离机理: 小分子量的化合物可以进入孔中, 滞留时间长; 大分子量的化合物不能进入孔中,直接随流动相流出。分子大小介于二者之间的分子在流动中部分渗透,渗透的程度取决于它们分子的大小,流出的时间介于二者之间 .分配系数: Ve = Vo + KdViKd = (Ve-Vo) / Vi当分子的Kd = 0时,Ve= Vo即该分子被完全排阻于凝胶颗粒之外,全部分布于流动相里,固定相里分布为零( A);当分子的Kd = 1时,Ve= Vo+Vi即该分子完全不被排阻,均匀的分布在流动相和固定相里,两相比值为 1(C) ;当 0 Kd 流动相固定相- 极性强流动相 (
19、 己烷 , 庚烷 )- 极性弱极性物质后出峰反相 HPLC极性 : 固定相 流动相固定相- 极性弱流动相 ( 甲醇 , 乙腈等 )- 极性强极性小物质后出峰4 .离子交换色谱:离子交换树脂的组成;应用机理: 树脂上可电离离子与流动相中具有相同电荷的离子及被测组分的离子进行可逆交换而分离。组成:骨架功能基团 活性离子(或可交换离子) 应用:软水制备:利用钠型阳离子交换树脂去除水中的钙、镁离子。2RSO3Na+ Ca2+X2RSO3Ca2+Na2X分离纯化一一氨基酸制备猪血粉firrDl/L.HC124h水解液1过滤后)脱色派嚼部A滤波黑篝4置募fAsp(pH3.5) GlpH4.5) Leu(p
20、H4 57 5)佚俄 1 01 mol/L 甄水耳is空HE.肛T .5)L”(pH七 5 T L)?uw/L家水Aig(pM ”72)无盐水制备无盐水制备是利用氢型阳离子交换树脂和羟型阴离子交换树脂的组合以除去水中所有的离子,其反应式如下RSOjH +MeX=RSO3Me + HXROH+HXtRX+H?O6.亲和色谱:影响亲和作用的因素;洗脱方式;了解常用的亲和配基影响因素:离子强度 PH抑制氢键形成的物质 温度 液体离子 螯合剂亲和作用主要源于静电引力,提高离子强度会减弱或完全破坏亲和作用;亲和作用主要源于氢键作用,提高离子强度也会降低或消除氢键作用;当亲和结合作用主要源于疏水性相互作用
21、,增大离子强度则可提高亲和结合作用;亲和作用主要源于静电引力,提高离子强度会减弱或完全破坏亲和作用;亲和作用主要源于氢键作用,提高离子强度也会降低或消除氢键作用;当亲和结合作用主要源于疏水性相互作用,增大离子强度则可提高亲和结合作用;洗脱方式:特异性洗脱:利用洗脱液中的物质与待分离物质或与配体的亲和特性而将待分离物质从亲和 吸附剂上洗脱下来。非特异性洗脱:通过改变洗脱缓冲液pH 、离子强度、温度等条件,降低待分离物质与配体的亲和力而将待分离物质洗脱下来。第八章 电泳1.电泳的分类分离原理:移动界面电泳 区带电泳 稳态电泳支持介质:纸电泳醋酸纤维薄膜电泳琼脂凝胶电泳聚丙烯酰胺凝胶电泳SDS 聚丙
22、烯酰胺凝胶电泳支持介质形状:薄层电泳、板电泳、柱电泳等用途:分析电泳、制备电泳、定量免疫电泳、连续制备电泳等2.SDS-PAGE 的基本原理及测定分子量的方法基本原理:聚丙烯酰胺凝胶系统中加入 SDS, SDS 与蛋白质结合后使蛋白质 SDS 复合物上带有大量的负电荷,使各种蛋白质分子本身的电荷完全被SDS 掩盖。这样就消除了各种蛋白质本身电荷上的差异。蛋白质电泳迁移率取决于其分子量,而与形状及所带电荷无关测定分子量的方法:样品处理:在沸水浴中煮35 min,使SDS与蛋白质充分结合,以使蛋白质完全变性和解聚,并形成棒状结构。短轴一定,长轴长度正比于P 分子量。加样。电泳过程中分子迁移的规律,小分子走在前头,大分子滞后。 染色脱色。在一定的凝胶浓度下, 多肽链分子量的对数与多肽链的相对迁移率成线性关系, 所以可以通过标准曲线求未知多肽链分子量。3.双向电泳的构成原理:第一向进行等电聚焦,蛋白质沿pH 梯度分离,至各自的等电点;随后,再沿垂直的方向进行分子量的分离。 第一向:等电聚焦电泳 第二向: SDS-PAGE双向电泳后的凝胶经染色后蛋白呈现二维分布图:水平方向反映出蛋白在pI 上的差异,垂直方向反映出它们在分子量上的差别。
- 温馨提示:
1: 本站所有资源如无特殊说明,都需要本地电脑安装OFFICE2007和PDF阅读器。图纸软件为CAD,CAXA,PROE,UG,SolidWorks等.压缩文件请下载最新的WinRAR软件解压。
2: 本站的文档不包含任何第三方提供的附件图纸等,如果需要附件,请联系上传者。文件的所有权益归上传用户所有。
3.本站RAR压缩包中若带图纸,网页内容里面会有图纸预览,若没有图纸预览就没有图纸。
4. 未经权益所有人同意不得将文件中的内容挪作商业或盈利用途。
5. 装配图网仅提供信息存储空间,仅对用户上传内容的表现方式做保护处理,对用户上传分享的文档内容本身不做任何修改或编辑,并不能对任何下载内容负责。
6. 下载文件中如有侵权或不适当内容,请与我们联系,我们立即纠正。
7. 本站不保证下载资源的准确性、安全性和完整性, 同时也不承担用户因使用这些下载资源对自己和他人造成任何形式的伤害或损失。
