 ISO13485-2016内部审核检查表(制造部)带填写记录
ISO13485-2016内部审核检查表(制造部)带填写记录


《ISO13485-2016内部审核检查表(制造部)带填写记录》由会员分享,可在线阅读,更多相关《ISO13485-2016内部审核检查表(制造部)带填写记录(6页珍藏版)》请在装配图网上搜索。
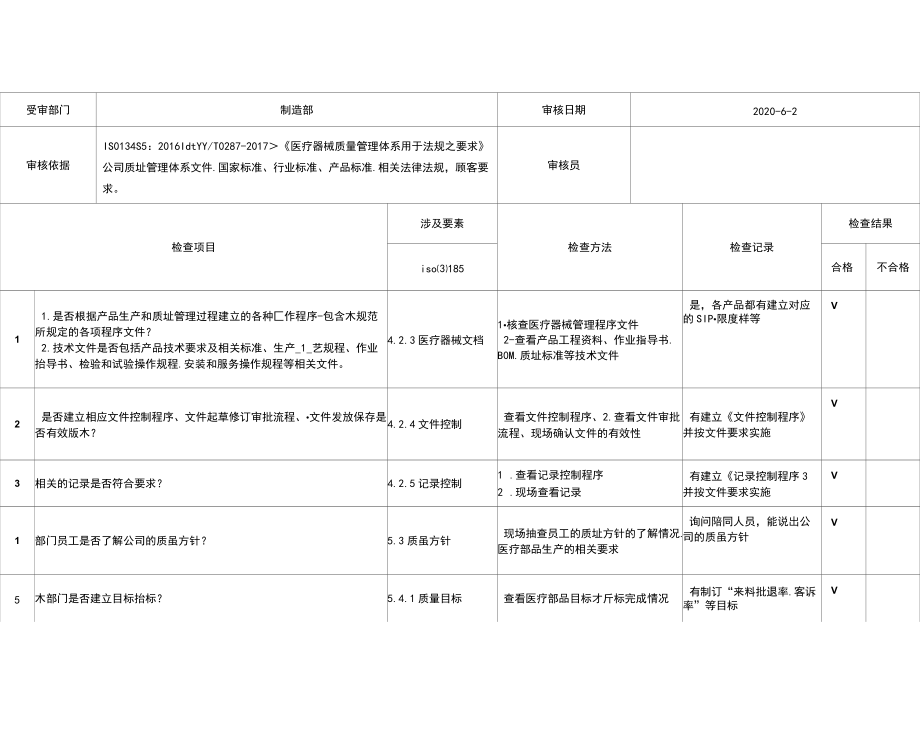
1、受审部门制造部审核日期2020-6-2审核依据IS0134S5:2016IdtYY/T0287-2017医疗器械质量管理体系用于法规之要求公司质址管理体系文件.国家标准、行业标准、产品标准.相关法律法规,顾客要求。审核员检查项目涉及要素检查方法检查记录检查结果iso185合格不合格11 .是否根据产品生产和质址管理过程建立的各种匚作程序-包含木规范所规定的各项程序文件?2 .技术文件是否包括产品技术要求及相关标准、生产_1_艺规程、作业抬导书、检验和试验操作规程.安装和服务操作规程等相关文件。4.2.3医疗器械文档1核查医疗器械管理程序文件2-查看产品工程资料、作业指导书.B0M.质址标准等技
2、术文件是,各产品都有建立对应的SIP限度样等V2是否建立相应文件控制程序、文件起草修订审批流程、文件发放保存是否有效版木?4.2.4文件控制查看文件控制程序、2.查看文件审批流程、现场确认文件的有效性有建立文件控制程序并按文件要求实施V3相关的记录是否符合要求?4.2.5记录控制1 .查看记录控制程序2 .现场查看记录有建立记录控制程序3并按文件要求实施V1部门员工是否了解公司的质虽方针?5.3质虽方针现场抽查员工的质址方针的了解情况.医疗部品生产的相关要求询问陪同人员,能说出公司的质虽方针V5木部门是否建立目标抬标?5.4.1质量目标查看医疗部品目标才斤标完成情况有制订“来料批退率.客诉率”
3、等目标V6是否明确木部门的职责和权限.明确质址管理职能5.5.1职责和权限询问员工是否清楚木岗位的相关要求,作业岗位有无产品上岗前培训询问陪同人员,能说出木岗位的职责-与岗位说明书一致。V7本部门是否制定培训计划?6.2.2培训、总识和能力查看部门培训计划及实施悄况。部门有制订年度培训计划并按计划实施培训,记录由人资行政部保存V81是否配备与所生产产品和规模相匹配的生产设备、工艺装备.应十确保有效运行。2-生产设备的设计、选型、安装、维修和维护是否符合预定用途.便干操作.清洁和维护。6.3基础设施1对照生产工艺流程图-查看设备清单.所列设备是否满足生产需要:核查现场设备是否与设备清。相关内容一
4、致:应洛制定设备管理制度2.查看IQ报告/0Q报告/PQ报告婆求的内容与现状生产的符合性,目的确认生产设备验证记录确认是否满足预定要求。现场查看生产设备是否便于操作、清洁和维护1 .现场的产品有对应的工艺流程图-SOPXSIPH限度样品等作为参考2 .现场有按婴求作业,并保存对应的记录V9是否提供适合产品的工作环境和污染的控制?6.4工作环境查看匚作现场有没有满足医疗部品环境监测与测址控制程序中的要求是,工作场所的环境都满足现阶段的要求-如1:作台.光照度、无尘棚等V10生产前是否对对产品的SOP.SIP.限度样生产设备、检测设备.产品的质址目标等进行点检确保满足要求?7.1产品实现的策划查看
5、现场的SOP、SIP.限度样等是,现场的环境满足婆求、有对应的SOP、SIP等V101 .是否按照建立的质量管理休系进行生产.以保证产品符合强制性标准和经注册或者备案的产品技术耍求?2 .是否编制生产工艺规程、作业抬导书等.明确关键匚序和持殊过程。7.5.1生产和服务提供的控制1.查看生产记录和出厂检验报告等2-查看相关文件:是否明确关键工序和持殊过程,对关键匚序和持殊过程的重耍参数是否做验证或确认的规定。K关键工序都有对应的SOP.有对应的记录表V11是否对在生产过程中需要原材料、中间品等进行清洁处理的,应半明确清洁方法和要求,并对清洁效果进行验证?7.5.2产品清洁查看对原材料、中间品清洁
6、方法和清洁效果验证记录NA12是否制定灭菌过程控制文件保持每一灭菌批的灭菌过程参数记录.火的记录应为可追溯到产品的每一生产批?7.5.5无菌医疗器械的专用要求1查看灭菌过程控制文件-这些文件应包括:灭菌工艺文件:灭菌设备操作规程:灭菌设备的维护、保养规定:适用时应包括环氧乙烷进货及存放控制:灭菌过程的确认和再确认。N/A2.现场查看火菌设备的过程参数和相关记录,是否符合经确认的灭菌匚艺,灭菌设备是否有自动监测及记录装迓,灭菌过程和参数记录是否完整、齐全,有可追溯性。131是否对生产的特殊过程进行确认-并保存记录.包括确认方案确认方法、操作人员、结果评价、再确认等内容。2-每批(台)产品是否均应
7、有生产记录,并满足可追溯的要求?7.5.6生产和服务提供过程的确认1 .查看特殊过程的确认记录2 .查看生产记录(生产日报表LOTNO批次管理.现品票的管理,材料添加记录,成型匚艺卡的变更管理,点检保养记录产品都有对应的批次号管理.有保存记录V14火菌过程是否按照相关标准要求在初次实施前进行确认必要时再确认-并保持火菌过程确认记录?7.5.7火菌过程和无菌屏障系统确认的专用要求N/AV151是否建立产品标识控制程序-用适宜的方法对产品进行标识,以便识别,防止混用和错用?2.是否在生产过程中标识产品的检验状态,防止不合格中间产品流向下道工序?7.5.8标识1 .查看是否对检验状态标识方法作出规定
8、现场查看生产过程中的检验状态标识.是否符合文件规定。2 .查看产品的可追溯性控制程(现品票标识的正确性)查生产过程中标识产品的检验状态-牟间摆放客户产品的放宜场所-没有按文件规定分待检区.合格品区、不合格区,生产现场只有一个成品摆放区NC161.建立产品的可追溯性程序.规定产品追溯范咏程度、标识和必要的记录。2.产品的说明书、标签是否符合相关法律法规及标准耍求。7.5.9可追溯性1 .查看产品的可追溯性控制程序2 .查看说明书和标签是否符合6号令的管理规定产品都有对应的批次号追溯V171 .是否建立不合格品控制程序-规定不合格品控制的部门和人员的职责与权限:2 是否对不合格品进行标识、记录、隔离.评审.根据评审结果-应U对不合格品采取相应的处宜措施:3 是否对上市后的不合格产品进行管控8.3不合格品控制1 .查看不合格品控制程序:2 .现场查看不合格品的标识.隔离是否符合程序文件的规定,抽查不合格品处理记录.是否按文件的规定进行评审:3 .售后发现不合格时的处宜措施.是否召回和销毁等。有建立不合格品控制程序,并按文件要求执行,详见不合格品处理记录VXXXXX有限公司IS013485:2016医疗质管理体系内审检查编制/日期:审核/日期:
- 温馨提示:
1: 本站所有资源如无特殊说明,都需要本地电脑安装OFFICE2007和PDF阅读器。图纸软件为CAD,CAXA,PROE,UG,SolidWorks等.压缩文件请下载最新的WinRAR软件解压。
2: 本站的文档不包含任何第三方提供的附件图纸等,如果需要附件,请联系上传者。文件的所有权益归上传用户所有。
3.本站RAR压缩包中若带图纸,网页内容里面会有图纸预览,若没有图纸预览就没有图纸。
4. 未经权益所有人同意不得将文件中的内容挪作商业或盈利用途。
5. 装配图网仅提供信息存储空间,仅对用户上传内容的表现方式做保护处理,对用户上传分享的文档内容本身不做任何修改或编辑,并不能对任何下载内容负责。
6. 下载文件中如有侵权或不适当内容,请与我们联系,我们立即纠正。
7. 本站不保证下载资源的准确性、安全性和完整性, 同时也不承担用户因使用这些下载资源对自己和他人造成任何形式的伤害或损失。
