 热力学基础计算题-答案
热力学基础计算题-答案


《热力学基础计算题-答案》由会员分享,可在线阅读,更多相关《热力学基础计算题-答案(15页珍藏版)》请在装配图网上搜索。
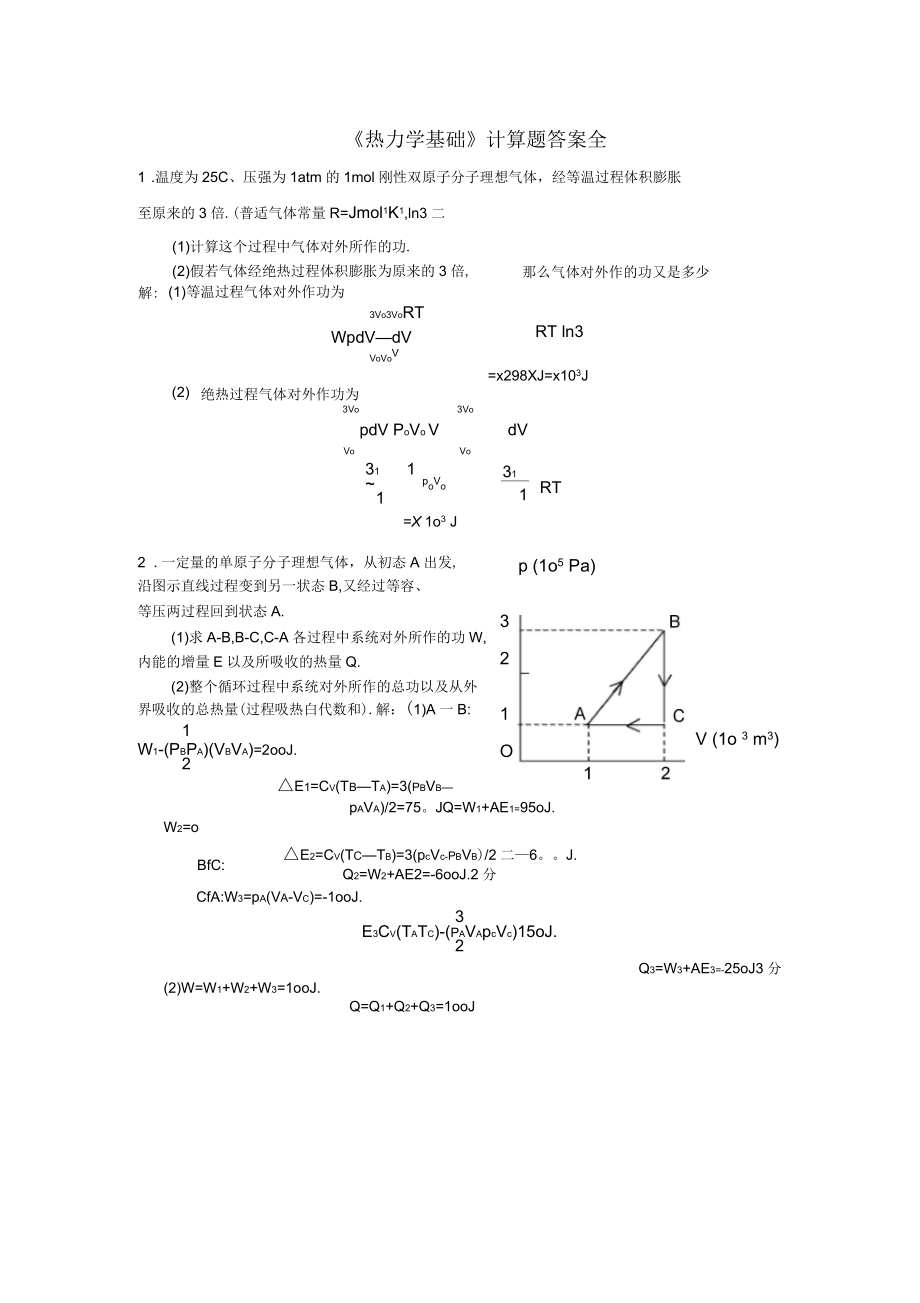
1、热力学基础计算题答案全1 .温度为25C、压强为1atm的1mol刚性双原子分子理想气体,经等温过程体积膨胀至原来的3倍.(普适气体常量R=Jmol1K1,ln3二(1)计算这个过程中气体对外所作的功.那么气体对外作的功又是多少RT ln3(2)假若气体经绝热过程体积膨胀为原来的3倍,解:(1)等温过程气体对外作功为3Vo3VoRTWpdVdVVoVoV=x298XJ=x103J(2)绝热过程气体对外作功为3Vo3VopdV PoVo VVoVo311poVo1=X 1o3 JdV311RTp (1o5 Pa)321OV (1o 3 m3)BfC:2 .一定量的单原子分子理想气体,从初态A出发
2、,沿图示直线过程变到另一状态B,又经过等容、等压两过程回到状态A.(1)求A-B,B-C,C-A各过程中系统对外所作的功W,内能的增量E以及所吸收的热量Q.(2)整个循环过程中系统对外所作的总功以及从外界吸收的总热量(过程吸热白代数和).解:(1)A一B:1W1-(PbPa)(VbVa)=2ooJ.2E1=Cv(TbTa)=3(pbVbpAVA)/2=75。JQ=W1+AE1=95oJ.W2=oE2=Cv(TcTb)=3(pcVc-pbVb)/2二6。J.Q2=W2+AE2=-6ooJ.2分CfA:W3=pA(Va-Vc)=-1ooJ.3E3Cv(TaTc)-(paVapcVc)15oJ.2Q
3、3=W3+AE3=-25oJ3分(2)W=W1+W2+W3=1ooJ.Q=Q1+Q2+Q3=1ooJ3.0.02kg的氨气(视为理想气体),温度由17c升为27c.若在升温过程中,(1)体积保持不变;(2)压强保持不变;(3)不与外界交换热量;试分别求出气体内能的改变、吸收的热量、外界对气体所作的功.1 1(普适气体常量R=JmolK)解:氨气为单原子分子理想气体,i3(1)等体过程,V=常量,W=0据Q=E+W可知QECV(T2T1)=623J3分Mmol(2)定压过程,p=常量,M仆QCp(T2Ti)=xio3jMmolE与(1)相同.W=QE=417J4分(3) Q=0,E与(1)同W=
4、E=623J(负号表示外界作功)3分4.一定量的某单原子分子理想气体装在封闭的汽缸里.此汽缸有可活动的活塞(活塞与气缸壁之间无摩擦且无漏气).已知气体的初压强P1=1atm,体积Vi=1L,现将该气体在等压下加热直到体积为原来的两倍,然后在等体积下加热直到压强为原来的2倍,最后作绝热膨胀,直到温度下降到初温为止,(2) (4) 解: (2)在p-V图上将整个过程表示出来.试求在整个过程中气体内能的改变. 试求在整个过程中气体所吸收的热量. 试求在整个过程中气体所作的功.p V图如右图.T4=TiE= 0七COGTi)2分MiM mol(4)(1 atm = x 105 Pa)p (atm)Pi
5、(2Vi Vi)Cv(T3T2)312V1(2p1Pi)11c一 Wi =x 102 J2W=Q= x 102 J4分2分mol双原子分子理想气体从状态A(p1,V1)沿pV图所示直线变化到状态B(P2,V2),试求:(1)气体的内能增量.(2)气体对外界所作的功.(3)气体吸收的热量.(4)此过程的摩尔热容.(摩尔热容C=Q/T,其中Q表示1mol物质在过程中升高温度T时所吸收的热量.)5,解:(1)ECv(T2Ti)(p2V2P1V1)21(2) W(PiP2)(V2Vi),2W为梯形面积,根据相似三角形有piV2=P2V1,则1W(p2V2P1V1).2(3) Q=AE+W=3(p2V2
6、P1V1).(4)以上计算对于A-B过程中任一微小状态变化均成立,故过程中AQ=3A(pV).由状态方程得故摩尔热容A(pV)=RAT,AQ=3RAT,C=AQ/AT=3R.6. 有1mol刚性多原子分子的理想气体,原来的压强为atm,温度为27C,若经过一绝热过程,使其压强增加到16atm.试求:(1)气体内能的增量;(2)在该过程中气体所作的功;(3)终态时,气体的分子数密度.(1atm=x105Pa,玻尔兹曼常量k=x10-23JK-1,普适气体常量R=Jmol-1K1)解:(1).刚性多原子分子i=6,L_24/31分i1T2T1(p2/p1)600K2分1 3八E(M/Mmol)-i
7、R(T2T1)7,48103J2分2(2)绝热W=-AE=-X10J(外界对气体作功)2分(3)p2=nkT2n=p2/(kT2)=X260个/m33分7.如果一定量的理想气体,其体积和压强依照V a/J6的规律变化,其中 a为已知常量.试求:(1)气体从体积V1膨胀到V2所作的功;(2)气体体积为V1时的温度T1与体积为V2时的温度T2之比.解:(1)dW=pdV=(a2/V2)dVV222211WdW%(a/V)dVa()2分(2)p1V1/T1=p2V2/T2T1/T2=p1V1/(p2V2)由Va/Vp1,V2a/Vp2得p1/p2=(V2/V1)2T1/T2=(V2/V1)2(V1/
8、V2)=V2/V13分8.汽缸内有一种刚性双原子分子的理想气体,若经过准静态绝热膨胀后气体的压强减少了一半,则变化前后气体的内能之比Ei:E2=1解:据(M /Mmoi)RTE(M/Mmoi)1iRT,PV21EliPV2变化前绝热过程1%/E1-iP1V1,2P1V1(V1M)变化后E21%/二1P2V22题设P212P1则(V1/V2)P2V2P2/P11 1 /(2)1 121.229.2 mol氢气(视为理想气体)开始时处于标准状态,后经等温过程从外界吸取了400 JV1/V211、E1/E2iP1V(iP2V2)222的热量,达到末态.求末态的压强.(普适气体常量R=mol-2K-1
9、)解:在等温过程中,AT=0Q=(M/Mmoi)RTln(V2/V1)即末态压强10.热量lV10.0882(M /Mmoi)RTV2/V1 =P2 = (V1 /V2) P1= atm为了使刚性双原子分子理想气体在等压膨胀过程中对外作功2 J,必须传给气体多少解:等压过程W= PAV=(M /Mmoi)RA T内能增量双原子分子1E (M/Mmai)产i 51Q E W -iW21T -iW2夕11 .两端封闭的水平气缸,被一可动活塞平分为左右两室,每室体积均为V。,其中盛有温度相同、压强均为p。的同种理想气体.现保持气体温度不变,用外力缓慢移动活塞(忽略磨擦),使左室气体的体积膨胀为右室的
10、2倍,问外力必须作多少功为了使刚性双原子分子理想气体在等压膨胀过程中对外作功2J,必须传给气体多少热量解:设左、右两室中气体在等温过程中对外作功分别用Wi、W2表示,外力作功用 W 表示.由V。,末态体积各为 4Vo/3和2Vo/3 .题知气缸总体积为2V。,左右两室气体初态体积均为据等温过程理想气体做功:W=(M/Mmol)RTln(V2/Vi)4Vo4WiP0V0InP0V0In3Vo3、,2P0V0 In32Vo得W2p0V0In3Vo现活塞缓慢移动,作用于活塞两边的力应相等,则W+Wi=W2429Vi2poVo(InIn)poVoIn338p (105 Pa)12 .一定量的理想气体,
11、从A态出发,经pV图中所示的过程到达B态,试求在这过程中,该气体吸收的热量.解:由图可得A态:pAVA8X1。5JB态:pBVB8X105JPaVaPbVb,根据理想气体状态方程可知TaTb,E=0根据热力学第一定律得:QWPa(VcVa)Pb(VbVd)1.5106J13 .如图,体积为30L的圆柱形容器内,有一能上下自由滑动的活塞(活塞的质量和厚度可忽略),容器内盛有1摩尔、温度为127c的单原子分子理想气体.若容器外大气压强为1标准大气压,气温为27C,求当容器内气体与周围达到平衡时需向外放热多少(普适气体常量R=Jmol-1K-1)解:开始时气体体积与温度分别为V1=30X103m3,
12、丁1=127+273=400K,气体的压强为P1=RT1/V1=x105Pa大气压po=x105Pa,p1po可见,气体的降温过程分为两个阶段:第一个阶段等体降温,直至气体压强P2=po,此时温度为丁2,放热Q1;第二个阶段等压降温,直至温度T3=To=27+273=300K,放热Q2Q1Cv(T1T2)2R(T1T2)IKQ1=428J5(2)Q2Cp(T2T3)R(T2T3)=1365Jp2,总计放热Q=Q1+Q2=X103J14.一定量的理想气体,由状态a经b到达c.(如图,abc为一直线)求此过程中p(atm)(2)气体对外作的功;气体内能的增量;气体吸收的热量.(1atm=x105P
13、a)解:(1)气体对外作的功等于线段ac下所围的面积W=(1/2)X(1+3)XX10(2)由图看出内能增量PaVa=PcVcE0.2分由热力学第一定律得Q=E+W=J.15.(2)定量的理想气体在标准状态下体积为x102m3,求下列过程中气体吸收的热量:等温膨胀到体积为X102m3;先等体冷却,再等压膨胀到(1)中所到达的终态.已知1atm=x105Pa,并设气体的Cv=5R/2.解:(1)如图,在A-B的等温过程中,Et0,QtWtV2pdVVV2p1Vlp-dVpMln(V2/V1)将p1=x105Pa,代入上式,得V1=x102m3V和V2=x102m3Qt=x10J.A、(2)A-C
14、等体和C-B等压过程中B两态温度相同,区bc=0Qacb=Wacb=Wcb=P2(V2p2=(V1/V2)p1=atmQacb=XX105XX3分Vi)102J=16.(2)将1mol理想气体等压加热,使其温度升高气体所作的功W;气体内能的增量E;比热容比.72K,传给它的热量等于X103J,求:(普适气体常量_11R8.31Jmol1K1)解:(2)CpWpVREQWQ22.2T598J一一一31.00103J11JmolKCVTcR13.9Jmol1KpCp1.6CV17.3m3一定量的某种理想气体,开始时处于压强、体积、To=300K的初态,后经过一等体过程,温度升高到温度分别为p0=x
15、10Pa,Vo=x10T1=450K,再经过一等温过程,压强降到p=P0的末态.已知该理想气体的等压摩尔热容与等体摩尔热容之比Cp/CV=33.求:(1)该理想气体的等压摩尔热容CP和等体摩尔热容Cv.(2)气体从始态变到末态的全过程中从外界吸收的热量.(普适气体常量R=Jmol1K1)一,Cp5解:(1)由和CpCvRCv3p_5_32分2分2分2分可解得J5R和CV-Rp22DoVo(2)该理想气体的摩尔数-4molRTo在全过程中气体内能的改变量为E=Cv(T1T2)=X彳QJ全过程中气体对外作的功为WRT1ln也p。式中p1/po=T1/ToT13则WRT11n16.0610J.To全
16、过程中气体从外界吸的热量为Q=ae+W=x10j.18 .如图所示,AB、DC是绝热过程,CEA是等温过程,BED是任意过程,组成一个循环。若图中EDC所包围的面积为70J,EAB即包围的面积为30J,过程中系统放热100J,求bed过程中系统吸热为多少解:正循环EDCE&围的面积为70J,表示系统对外作正功70JEABE的面积为30J,因图中表示为逆循环,故系统对外作负功,所以整个循环过程系统对外作功为:W=70+(30)=40J1分设CEA过程中吸热Q1,BED过程中吸热Q2,由热一律,W=Q1+Q2=40JQ2=WQ1=40(-100)=140JBED过程中系统从外界吸收140焦耳热.1
17、9 .1mol理想气体在T1=400K的高温热源与T2=300K的低温热源问作卡诺循环(可逆的),在400K的等温线上起始体积为V1=0.001m3,终止体积为V2=0.005m3,试求此气体在每一循环中(1)从高温热源吸收的热量Qi(2)气体所作的净功W(3)气体传给低温热源的热量Q2解:(1)Q1RT11n(V2/V1)5.35103J3分1T20.25.T1,3WQ11.3410J4分3.(3) Q2Q1W4.0110J3分20.一定量的某种理想气体进行如图所示的循环过程.已知气体在状态A的温度为Ta=300K,求(1)气体在状态日C的温度;(2)各过程中气体对外所作的功;(3)经过整个
18、循环过程,气体从外界吸收的总热量(各过程吸热的代数和).解:由图,Pa=300Pa,pB=pc=100Pa;Va=Vc=1m3,Vb=3m3.I) )C-A为等体过程,据方程Pa/T=pc/Tc得Tc=Tapc/pA=100K.B-C为等压过程,据方程Vb/Tb=Vc/Tc得Tb=TCVb/Vc=300K.(2)各过程中气体所作的功分别为.1,A一B:W1(pApB)(VBVc)=400J.2Bfc:W2=pB(VcVb)=200J.C-A:W3=03分(3)整个循环过程中气体所作总功为W=W1+W2+W3=200J.因为循环过程气体内能增量为En。,因此该循环中气体总吸热Q=W+AE=200
19、J) 3分mol氨气作如图所示的可逆循环过程,其中ab和cd是绝热过程,bc和da为等体过程,已知V1=16.4LV2=32.8Lpa=1atm,pb=atm,pc=4atm,pd=atm,试求:(1)在各态氮气的温度.(2)在态氮气的内能.在一循环过程中氮气所作的净功.(1atm=x105Pa)(普适气体常量R=Jmol1K)解:Ta=paV2/R=400KTb=pbVi/R=636KTc=pcVi/R=800K4分2分1分1分2分Td=pdV2/R=504K(2) Ec=(i/2)RTC=X103Jbc等体吸热Qi=Cv(TcTb)=X103Jd-a等体放热Q2=CV(TdTa)=X103
20、JW=QiQ2=x103JP(Pa)22.比热容比=的理想气体进行如图所示的循环.已知状态A的温度为300K.求:(1)状态B、C的温度;(2)每一过程中气体所吸收的净热量.解:由图得= 100 Pa,(普适气体常量R=Jmol1K1)Pa=400Pa,pB=pCVa=Vb=2m3,Vc=6m3.(1)C-A为等体过程,据方程pA/Ta=pC/Tc得Tc=Tapc/pA=75K1分B-C为等压过程,据方程Vb/Tb=VcTc得Tb=TcVb/Vc=225K1分(2)根据理想气体状态方程求出气体的物质的量(即摩尔数)为pAVARTAmol5_7由=知该气体为双原子分子气体,CV-R,CP7R22
21、B-C等压过程吸热Q27R(TcTb)1400J.一5C-A等体过程吸热Q3R(TaTc)1500J.2循环过程4E=0,整个循环过程净吸热八1QW2(PAPc)(VbVc)600J.1-A-B过程净吸热:Q1=QQ2Q3=500J23 .一卡诺热机逆的),当高温热源的温度为127C、低温热源温度为27c时,其每次循环对外作净功8000J.今维持低温热源的温度不变,提高高温热源温度,使其每次循环对外作7功10000J.若两个卡诺循环都工作在相同的两条绝热线之间,试求:(1)第二个循环的热机效率;(2)第二个循环的高温热源的温度.解:WQiQ2TiT2QiTiTi T2Q2 = T2 Qi/Ti
22、TiQ2Q由于第二循环吸热(2)Q2TiTi T2Qi WT2WTiQ2 WW /QiT2 =24000 JTi T2Q2( .Q2%425 KQ2)4分3分 i分2分p (atm)24 .气缸内贮有36g水蒸汽(视为刚性分子理想气体),经abcda循环过程如图所示.其中a-b、cd为等体过程,bc为等温过程,d-a为等压过程.试求:(1) d-a过程中水蒸气作的功Wda(2) a-b过程中水蒸气内能的增量ab(3)循环过程水蒸汽作的净功W(4)循环效率(注:循环效率=W/Qi,W为循环过程水蒸汽对外作的净功,Qi为循环过程水蒸汽吸收的热量,iatm=xi05Pa)解:水蒸汽的质量M=36xi
23、0-3kg水蒸汽的摩尔质量Mmoi=i8Xi0-3kg,i=6(1) Wda=pa(Va-Vd)=-Xi0J(2) Eab=(M/Mmol)(i/2)RTbTa)=(i/2)Va(pbpa)=Xi04JTbpbVa9i4K(M/Mmol)RWbc=(M/Mmoi)RTbln(Vc/Vb)=X410净功W=Wbc+Wda=xi03J(4)Qi=Qab+Qbc=AEab+Wbc=X4J刀=W/Q=i3%2分mol的理想气体,完成了由两个等体过程和两个等压过程构成的循环过程(如图),已知状态i的温度为Ti,状态3的温度为T3,且状态2和4在同一条等温线上.试求气体在这一循环过程中作的功.解:设状态“
24、2”和“4”的温度为TWW4iW23R(T3T)R(TiT)R(TiT3)2RTPl=p4,p2=p3,Vl=V2,V3=V4而PiViRTi,p3V3RT3,P2V2RT,P4V4RT2T1T3p1V1P3V3/R,_2_2Tp2V2P4V4/R.得T2T1T3,即T(TiT3)1/2K1/2WRTiT32(T/3)k3分26 .一卡诺循环的热机,高温热源温度是400K.每一循环从此热源吸进100J热量并向一低温热源放出80J热量.求:(1)低温热源温度;(2)这循环的热机效率.解:(1)对卡诺循环有:Ti/T2=Q1/Q2T2=T1Q2/Q1=320K即:低温热源的温度为320K.3分Q2
25、(2)热机效率:120%2分Q127 .如图所示,有一定量的理想气体,从初状态a(P1,V1)开始,经过一个等体过程达到压强为P1/4的b态,再经过一个等压过程达到状态c,最后经等温过程而完成一个循环.求该循环过程中系统对外作的功W和所吸的热量Q.解:设c状态的体积为V2,则由于a,c两状态的温度相同,p1V1=P1V2/4循环过程而在a-b等体过程中功 在b-c等压过程中功V2=4V1E=0,Q=W.W1=0.W2=p1(V2V1)/4=P1(4V1V1)/4=3P1V1/4在c-a等温过程中功W3=p1V1ln(V2/V1)=p1V1ln4W=W1+W2+W3=(34)ln4P1V1Q=W
26、=(3/4)-ln4p1V128.比热容比的理想气体,进行如图所示的ABCA循环,状态 A的温度为300 K.(1)求状态B、C的温度;(2)计算各过程中气体所吸收的热量、气体所作的P (Pa)A 400功和气体内能的增量.(普适气体常量 R-一118.31 J mol K )解:(1) C- A等体过程有Pa/Ta = pc/TcpcTc Ta产)Pa75A300200100BC6O 2V (m3)B一 C等压过程有Vb/Vb=Vc/ TcTb(2)气体的摩尔数为VBTc(VB)M225由Y =可知气体为双原子分子气体,CVC- A等体吸热过程BfC等压压缩过程A- B膨胀过程29.气缸内盛
27、有M molPaVa rt10.3212R , cpWCA=0Qca = A Eca = v CV (Ta Tc ) =1500 JWbc=Pb(Vc Vb) =-400 JA Ebc= v C/ (Tc- Tb) =- 1000 JQbc= A Ebc+ Wbc = 1400 J1WAB-(400 100) (6 2) J 1000 J2AEab = vC/ (TbTa) =500 JQab = AEab+ Wab =500 J定量的单原子理想气体.若绝热压缩使其体积减半,问气体分子的平均速率为原来的几倍解:设绝热压缩前气体的体积为V1,温度为T1;压缩后的体积为=V1/2,温度为T2;气体
28、的比热比为由绝热方程得:V1丁V21T2T2=T1(V1/V2)t-1=2t-1T12分设绝热压缩前后,气体分子的平均速率分别为v1和v2,v乐二v2/v13T2/T1将关系式T2/T1=2-1代入上式,得心/712(1)/21分单原子理想气体=5/3-,1分故72/爪1=1分30.一定量的氨气(理想气体),原来的压强为pi=1atm,温度为Ti=300K,若经过一绝热过程,使其压强增加到p2=32atm.求:(1)末态时气体的温度T2.(2)末态时气体分子数密度n.(玻尔兹曼常量k=X1023JK1,1atm=xi0Pa)解:(1)根据绝热过程方程p1TC有T2(匹)(1)/T1P1T2T1(匹)(1)/P1氨为单原子分子,33T2=1200K3分(2)n型1.961026m32分kT2
- 温馨提示:
1: 本站所有资源如无特殊说明,都需要本地电脑安装OFFICE2007和PDF阅读器。图纸软件为CAD,CAXA,PROE,UG,SolidWorks等.压缩文件请下载最新的WinRAR软件解压。
2: 本站的文档不包含任何第三方提供的附件图纸等,如果需要附件,请联系上传者。文件的所有权益归上传用户所有。
3.本站RAR压缩包中若带图纸,网页内容里面会有图纸预览,若没有图纸预览就没有图纸。
4. 未经权益所有人同意不得将文件中的内容挪作商业或盈利用途。
5. 装配图网仅提供信息存储空间,仅对用户上传内容的表现方式做保护处理,对用户上传分享的文档内容本身不做任何修改或编辑,并不能对任何下载内容负责。
6. 下载文件中如有侵权或不适当内容,请与我们联系,我们立即纠正。
7. 本站不保证下载资源的准确性、安全性和完整性, 同时也不承担用户因使用这些下载资源对自己和他人造成任何形式的伤害或损失。
