 核外电子排布
核外电子排布


《核外电子排布》由会员分享,可在线阅读,更多相关《核外电子排布(38页珍藏版)》请在装配图网上搜索。
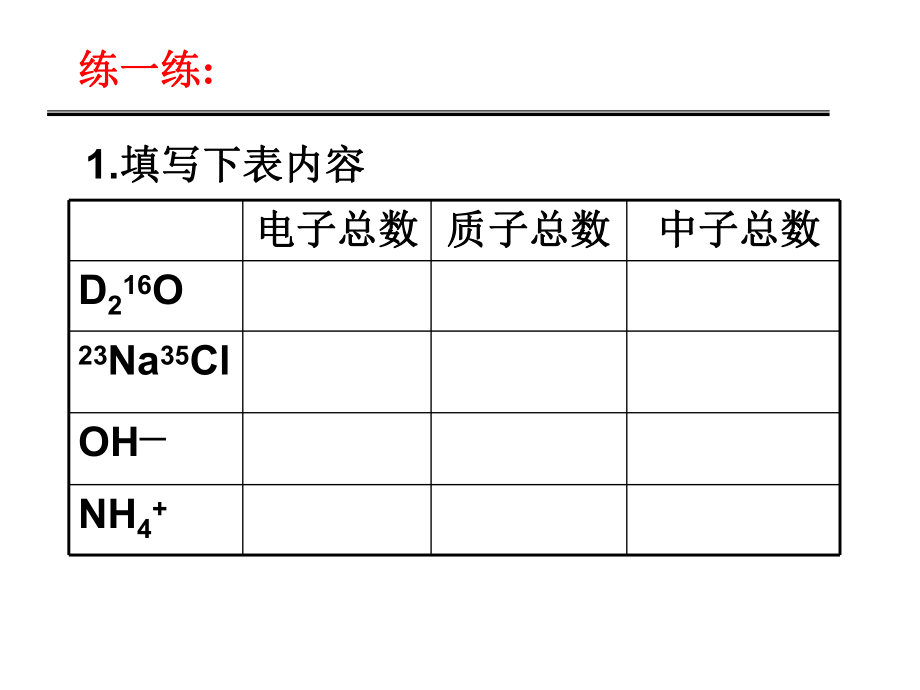
1、电子总数电子总数 质子总数质子总数 中子总数中子总数 D216O 23Na35Cl OH NH4+ 练一练练一练: 1.填写下表内容填写下表内容同位素同位素质子数相同而中子数不同的质子数相同而中子数不同的同一元素的不同一元素的不 同原子同原子互称为同位素;互称为同位素;注意:注意:1、同种元素,可以有若干种不同的核素。同种元素,可以有若干种不同的核素。同位素在周期表里占据同一位置。同位素在周期表里占据同一位置。 2、同位素原子的质量数不同,核外电子层结构同位素原子的质量数不同,核外电子层结构相同,其原子、单质及其构成的化合物相同,其原子、单质及其构成的化合物化学性质化学性质几乎完全相同几乎完全
2、相同,只是某些物理性质,只是某些物理性质略有差异略有差异。 3.天然存在的某种元素,不论是游离态,还是化合态,天然存在的某种元素,不论是游离态,还是化合态,其各种同位素所占的原子个数百分比一般不变。其各种同位素所占的原子个数百分比一般不变。4、相对原子质量、相对原子质量(1)核素的相对原子质量)核素的相对原子质量1个原子的质量个原子的质量1个个12C原子的质量原子的质量612核素的近似相对原子质量质量数核素的近似相对原子质量质量数()元素的相对原子质量等于各同位素的相()元素的相对原子质量等于各同位素的相对原子质量的平均值:对原子质量的平均值:元素的相对原子质量元素的相对原子质量Aa%Bb%C
3、c% 元素的近似相对原子质量等于各同位素的质元素的近似相对原子质量等于各同位素的质量数的平均值。量数的平均值。元素的近似相对原子质量元素的近似相对原子质量Aa%Bb%Cc%符符 号号 同位素的原子量同位素的原子量在自然界中各同位素原子在自然界中各同位素原子 的含量的含量 (丰度)(丰度) 34.969 36.966 24.23 % 75.77 %Cl 35 17 氯元素的相对原子量(平均原子量)氯元素的相对原子量(平均原子量)= 34.9690.757736.9660.2423 = 35.453Cl 37 17 练习 硼元素的平均原子量为硼元素的平均原子量为10.8,则自然界中,则自然界中10
4、B 和和 11B的原子个数比为多少?的原子个数比为多少? 解法一:解法一: 设设10B的丰度是的丰度是X%, 则则11B的丰度是的丰度是1-X% 10X% + 11(1-X%) =10.8解得解得 X% = 20%故故10B和和11B的原子个数比为的原子个数比为 1 :4551-X% = 80%练习 硼元素的平均原子量为硼元素的平均原子量为10.8,则自然界中,则自然界中10B 和和 11B的原子个数比为多少?的原子个数比为多少? 解法二:解法二: 十字交叉法十字交叉法11B5510B111010.8 0.80.24110B和和11B的原子个数比为的原子个数比为 1 :4原子核外电子的排布原子
5、核外电子的排布学习目标:学习目标: 1、理解解核外电子是分层排布的理解解核外电子是分层排布的,不同不同电子层中的电子具有不同的能量。电子层中的电子具有不同的能量。 2、掌握核外电子排布的初步规律掌握核外电子排布的初步规律,并能并能据此规律画出常见原子的结构示意图。据此规律画出常见原子的结构示意图。一、原子核外电子一、原子核外电子的的排布排布1、核外电子运动的特点:、核外电子运动的特点: (1)高速运动高速运动(运动的速度接近光速,约为(运动的速度接近光速,约为108m/s);); (2)运动运动没有确定的轨道没有确定的轨道,不能精确测定或计算,不能精确测定或计算电子在任一时刻所在的位置,也不能
6、描绘出其电子在任一时刻所在的位置,也不能描绘出其运动轨迹。运动轨迹。 (3)多电子的原子里,电子的多电子的原子里,电子的能量不同能量不同。有些电。有些电子能量较低,在离核较近的子能量较低,在离核较近的区域区域里运动;有些里运动;有些电子能量较高,在离核较远的电子能量较高,在离核较远的区域区域里运动。里运动。2 2、电子层电子层: :能量不同能量不同的电子的运动的电子的运动区域区域(即不连续的壳层(即不连续的壳层该电子层模型称洋葱式结构)该电子层模型称洋葱式结构)哪个区域能量最高,电子最哪个区域能量最高,电子最活泼,最易参与化学反应?活泼,最易参与化学反应?电子层电子层(n)1234567字母表
7、示字母表示 能量能量K L M N O P Q低低高高172 8 7Cl 仔细观察,说说各个符号分别表示什么意思?资料资料1:118号元素的原子结构示意图号元素的原子结构示意图观察观察1-18号元素的原子结构示意图,你能归纳号元素的原子结构示意图,你能归纳出核外电子排布有哪些规律?出核外电子排布有哪些规律?资料资料2:稀有气体元素的原子核外电子排布:稀有气体元素的原子核外电子排布元素元素各电子层的电子数各电子层的电子数KLMNOP2He(氦)(氦)210Ne(氖)(氖)2818Ar (氩)(氩)28836Kr (氪)(氪)2818854Xe (氙)(氙)281818886Rn (氡)(氡)28
8、1832188原子核外电子排布原子核外电子排布阅读课本阅读课本P3表表1-1,思考:,思考:K、L、M、N电子层最多可容纳的电子数依次是多少?电子层最多可容纳的电子数依次是多少?与电子层数与电子层数n之间有何关系?之间有何关系?电子层电子层 K L M N 电子层上最多电子层上最多容纳的电子数容纳的电子数2818 32 212 222 232 242 (1)各电子层最多容纳的电子数为)各电子层最多容纳的电子数为2n2个。个。原子核外电子排布规律原子核外电子排布规律分析分析P3表表1-1,各稀有气体元素原子的最外层,各稀有气体元素原子的最外层最多能容纳的电子数是多少?次外层呢?最多能容纳的电子数
9、是多少?次外层呢?(1)各电子层最多容纳的电子数为)各电子层最多容纳的电子数为2n2个。个。(2)最外层电子数不超过)最外层电子数不超过8个(个(K层为最外层层为最外层不超过不超过2个),次外层不超过个),次外层不超过18个(个(K为次外层为次外层为为2个个,倒数第三层最多容纳倒数第三层最多容纳32个电子个电子)(3)核外电子排布时,按能量由低到高排布,)核外电子排布时,按能量由低到高排布, 先排满内层,再依次排向外层。先排满内层,再依次排向外层。注注:原子的核外电子排布需要同时原子的核外电子排布需要同时满足上述的条件满足上述的条件巩固练习巩固练习: :依据原子核外电子的排布规律依据原子核外电
10、子的排布规律,请完请完成成19、20号元素的原子结构示意图号元素的原子结构示意图.思考思考5:分析下图三个不同区域中,各元素分析下图三个不同区域中,各元素的最外层电子数和元素的分类有何关系?的最外层电子数和元素的分类有何关系?氢(H) 氦(He) 锂(Li) 铍(Be) 硼(B) 碳(C) 氮(N) 氧(O) 氟(F) 氖(Ne )钠(Na) 镁(Mg) 铝(Al) 硅(Si) 磷(P) 硫(S) 氯(Cl) 氩(Ar)元素分类元素分类最外层电子数最外层电子数得失电子趋势得失电子趋势稀有气体稀有气体金属元素金属元素非金属元素非金属元素8(He为2 )少于少于4个个4个以上个以上稳定结构稳定结构
11、易易失失电子电子 易易得得电子电子稳定结构:稳定结构:最外层电子数为最外层电子数为8(He为为2)的电子的电子层结构,通常不容易得失电子。层结构,通常不容易得失电子。化学性质稳定、不活泼。化学性质稳定、不活泼。小结小结2 6+8原子结构示意图原子结构示意图核外电子排布规律核外电子排布规律能量最低能量最低原理原理:先排先排K层,排满层,排满K层后再排层后再排L层层.每个电子层最多只能容纳每个电子层最多只能容纳2n2个电子。个电子。最外层最多容纳最外层最多容纳8个电子(个电子(K为最外层为为最外层为2个)个)次外层最多容纳次外层最多容纳18个电子(个电子(K为次外层为为次外层为2个个倒数第三层最多
12、容纳倒数第三层最多容纳32个电子个电子)习习 题题 巩巩 固固2 2、某元素的原子核外有某元素的原子核外有3个电子层,最外层个电子层,最外层有有4个电子,该原子核内的质子数为个电子,该原子核内的质子数为 ( ) A.14 B.15 C.16 D.17练习练习1 :下列原子结构示意图是否正确?:下列原子结构示意图是否正确?+192 8 9+33+202 8 2+10 2 8 1A3.根据下列叙述根据下列叙述,写出元素名称并画出原写出元素名称并画出原子结构示意图。子结构示意图。 (1)A元素原子核外元素原子核外M层电子数是层电子数是L层电子数的层电子数的1/2;_ (2)B元素原子的最外层电子数是
13、次元素原子的最外层电子数是次外层电子数的外层电子数的1.5倍;倍;_ (3)C元素的次外层电子数是最外层元素的次外层电子数是最外层电子数的电子数的1/4;_ 硅硅硼硼氖氖习习 题题 巩巩 固固习习 题题 巩巩 固固4:在118号元素中,用元素符号回答1)最外层只有1个电子的原子2)最外层只有2个电子的原子3)L层有5个电子的原子 M层有5个电子的原子4)最外层电子数是次外层电子数2倍的原子5)M层电子数是L层电子数0.5倍的原子H Li Na He Be MgN P C Si 3+含有含有10个电子的粒子有:个电子的粒子有:1、分子:、分子:HF、H2O、NH3、CH42、原子:、原子:Ne3
14、、阳离子:、阳离子:Na+、Mg2+、Al3+、NH4+、H3O+4、阴离子:、阴离子:N3、O2、F、OH、NH2含有含有18个电子的粒子有:个电子的粒子有:SiH4、PH3、H2S、HCl、F2、Ar、S2、Cl、K+、Ca2+、HS含有含有2个电子的粒子有:个电子的粒子有:H、He、Li+、Be2+具有具有2、8结构的粒子:结构的粒子:N3、O2、F (Ne)Na+、Mg2+、Al3+具有具有2、8、8结构的粒子:结构的粒子: S2 Cl (Ar)K+ Ca2+ 注意这些原子(或离子)在周期表中注意这些原子(或离子)在周期表中的位置和排列规律以及半径大小。的位置和排列规律以及半径大小。3
15、.写出核外电子总数为写出核外电子总数为10的微粒的微粒:1)单核阳离子单核阳离子:_2)单核阴离子单核阴离子:_3)单核原子单核原子:_4)多核阳离子多核阳离子:_5)多核阴离子多核阴离子:_6)多核分子多核分子:_练一练练一练: 自然界有一个普遍的规律,那就是“能量越低越稳定能量越低越稳定”。 电子总是优先占据能量较低的区域,这样能使整个原子体系的能量处于最低,从而促使原子的稳定存在。 所以电子总是尽可能地先从内层排起,当一层充满后再填充下一层。规 118号元素原子结构的特殊规律:最外层电子数等于次外层电子数 的元素: Be、Ar最外层电子数是次外层电子数的 2倍的元素:C最外层电子数是次外
16、层电子数的 3倍的元素:O电子层数与最外层电子数相等的 元素:H、Be、Al原子核内无中子的原子:原子核内无中子的原子: H最外层电子数是最外层电子数是1的原子:的原子: H Li Na 最外层电子数是最外层电子数是2的原子:的原子:He Be Mg 次外层电子数是最外层电子数 2倍的元素:Li、Si应用各层的电子数推断元素:应用各层的电子数推断元素:某元素的某元素的M层上的电子数是层上的电子数是K层的层的3倍倍,则该元素是则该元素是( ).某元素的最外层上的电子数是某元素的最外层上的电子数是次外层层电子数的一半次外层层电子数的一半,是倒数第是倒数第三层的三层的2倍倍,则该元素是则该元素是(
17、). 某元素的最外层上的电子数是次某元素的最外层上的电子数是次外层层电子数的外层层电子数的2倍倍,则该元素是则该元素是 SSiC2、下列有几种元素的核电荷数,其中最外层电子数目最多的是 A、8 B、14 C、18 D、20CC3、某元素原子的最外层的电子数目为次外层的电子数目的3倍,则该元素的原子核内质子数为 A、3 B、7 C、8 D、10练习练习: :8(20018(2001、上海)、上海)X X、Y Y、Z Z和和R R分别代表分别代表四种元素四种元素: :a aX Xm m+ + 、 b bY Yn n+ + c cZ Zn n- - d dR Rm m- -四四种离子的核外电子排布相
18、同,且种离子的核外电子排布相同,且m mn n。则下列关系正确的是(则下列关系正确的是( )A A a-c=m-n B b-d=m+na-c=m-n B b-d=m+nC Ca ab bd dc D ac D ab bc cd dBDBD练习练习: :9(20049(2004、济南)科学家最近制造出第、济南)科学家最近制造出第112112号新元素,其原子的质量数为号新元素,其原子的质量数为277277,这是迄今为止已知元素中最重的原子。这是迄今为止已知元素中最重的原子。则下列关于新元素的叙述正确的是则下列关于新元素的叙述正确的是( )A A 其原子核内中子数和质子数都是其原子核内中子数和质子数
19、都是112112。BDBDB B 其原子核内中子数为其原子核内中子数为165165,核外电子数是,核外电子数是112112。C C 其原子质量是其原子质量是1212C C原子质量的原子质量的277277倍。倍。D D 其原子质量与其原子质量与1212C C原子质量之比为原子质量之比为277277:1212 (1) r(Cl-)r(Cl),r(Na+)r(Na); (2)电子层结构相同时,核电荷数越大,微粒半径电子层结构相同时,核电荷数越大,微粒半径越小。越小。 如如: r(F )r Na+)r(Mg2+)r(Al3+); (3)同周期元素原子半径随原子序数递增逐渐减小。同周期元素原子半径随原子
20、序数递增逐渐减小。 同主族元素原子和离子半径随原子序数递增逐同主族元素原子和离子半径随原子序数递增逐渐增大。渐增大。2.有有X,Y,Z三种元素三种元素,X原子核内无中子原子核内无中子,Y原原子的第三个电子层上有子的第三个电子层上有3个电子个电子,Z原子最原子最外层电子数是其电子层数的外层电子数是其电子层数的3倍倍.试判断试判断X_,Y_,Z_. 并画出其原子结构并画出其原子结构示意图示意图_, _, _.这三种元素这三种元素所组成的化合物的化学式为所组成的化合物的化学式为_.练一练练一练: 练一练练一练: 4.下列说法不正确的是(下列说法不正确的是( )质子数相同的粒子一定属于同种元素质子数相
21、同的粒子一定属于同种元素同位素的化学性质几乎完全相同同位素的化学性质几乎完全相同质子数相同,电子数也相同的粒子,不可能质子数相同,电子数也相同的粒子,不可能是一种分子和一种离子是一种分子和一种离子电子数相同的粒子不一定是同一种元素电子数相同的粒子不一定是同一种元素一种元素只能有一种质量数一种元素只能有一种质量数A、 B、C、 D、在原子序数在原子序数1 11818号元素范围内,按要求号元素范围内,按要求回答下列问题:回答下列问题:最外层电子数为最外层电子数为1 1的原子有的原子有_最外层电子数是次外层电子数最外层电子数是次外层电子数2 2倍的原倍的原子是子是_最外层电子数是次外层电子数最外层电子数是次外层电子数3 3倍的原倍的原子是子是_最外层电子数是次外层电子数最外层电子数是次外层电子数4 4倍的原倍的原子是子是_课前课前3分钟分钟:次外层电子数是最外层电子数次外层电子数是最外层电子数2倍的原子倍的原子有有_内层电子总数是最外层电子数内层电子总数是最外层电子数2倍的原子倍的原子有有_电子层数与最外层电子数相等的原子有电子层数与最外层电子数相等的原子有_最外层电子数是电子层数最外层电子数是电子层数2倍的原子有倍的原子有_最外层电子数是电子层数最外层电子数是电子层数3倍的原子是倍的原子是_在原子序数在原子序数118号元素范围内,按要求号元素范围内,按要求回答下列问题:回答下列问题:
- 温馨提示:
1: 本站所有资源如无特殊说明,都需要本地电脑安装OFFICE2007和PDF阅读器。图纸软件为CAD,CAXA,PROE,UG,SolidWorks等.压缩文件请下载最新的WinRAR软件解压。
2: 本站的文档不包含任何第三方提供的附件图纸等,如果需要附件,请联系上传者。文件的所有权益归上传用户所有。
3.本站RAR压缩包中若带图纸,网页内容里面会有图纸预览,若没有图纸预览就没有图纸。
4. 未经权益所有人同意不得将文件中的内容挪作商业或盈利用途。
5. 装配图网仅提供信息存储空间,仅对用户上传内容的表现方式做保护处理,对用户上传分享的文档内容本身不做任何修改或编辑,并不能对任何下载内容负责。
6. 下载文件中如有侵权或不适当内容,请与我们联系,我们立即纠正。
7. 本站不保证下载资源的准确性、安全性和完整性, 同时也不承担用户因使用这些下载资源对自己和他人造成任何形式的伤害或损失。
