 江苏省怀仁中学高三化学复习《实验》大题练习(六)
江苏省怀仁中学高三化学复习《实验》大题练习(六)


《江苏省怀仁中学高三化学复习《实验》大题练习(六)》由会员分享,可在线阅读,更多相关《江苏省怀仁中学高三化学复习《实验》大题练习(六)(7页珍藏版)》请在装配图网上搜索。
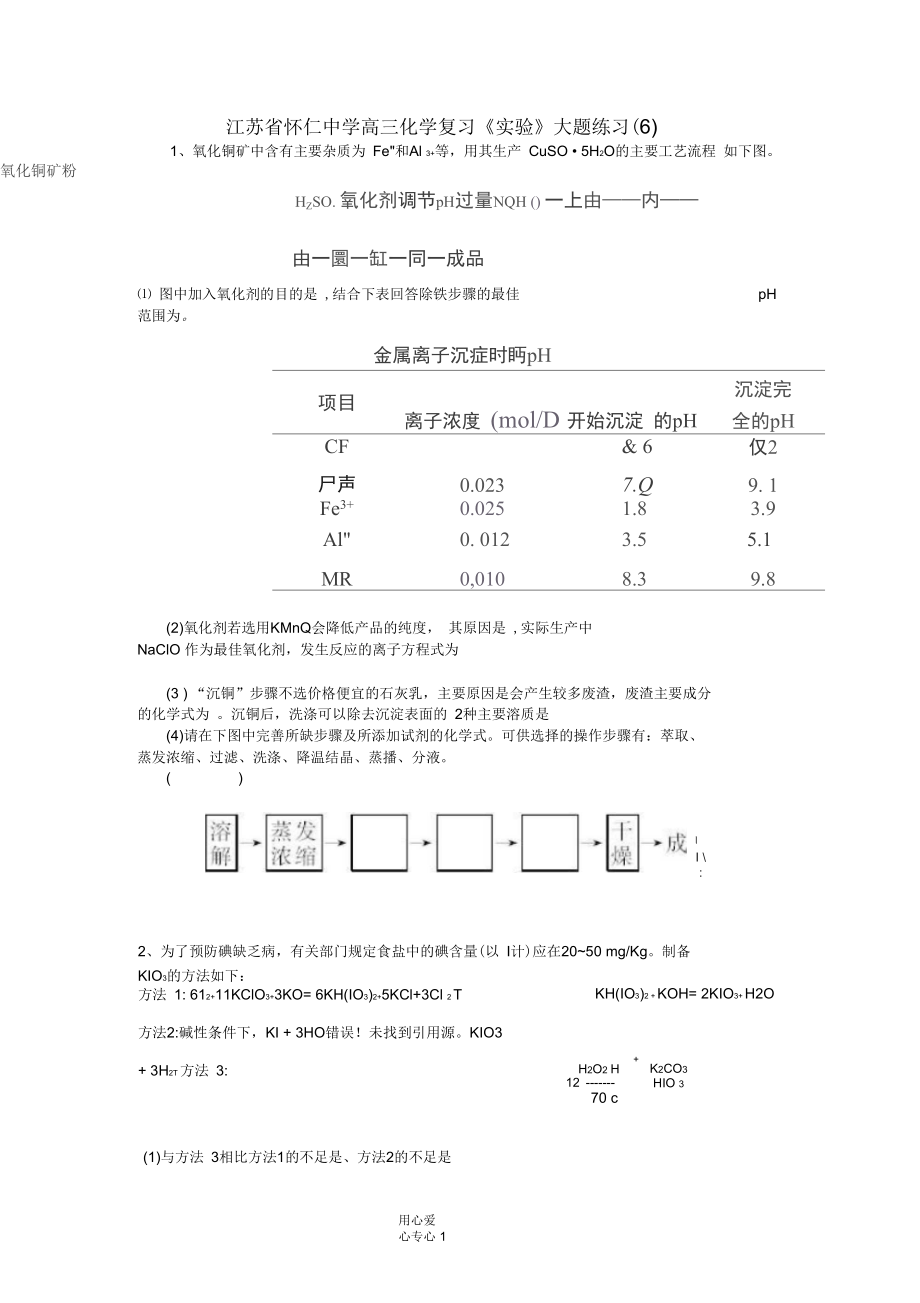
1、江苏省怀仁中学高三化学复习实验大题练习(6)1、氧化铜矿中含有主要杂质为 Fe和Al 3+等,用其生产 CuSO 5H2O的主要工艺流程 如下图。氧化铜矿粉HZSO. 氧化剂调节pH过量NQH () 一上由内由一圜一缸一同一成品 图中加入氧化剂的目的是 ,结合下表回答除铁步骤的最佳pH范围为。金属离子沉症时眄pH项目离子浓度 (mol/D开始沉淀 的pH沉淀完 全的pHCF& 6仅2尸声0.0237.Q9. 1Fe3+0.0251.83.9Al0. 0123.55.1MR0,0108.39.8(2)氧化剂若选用KMnQ会降低产品的纯度, 其原因是 ,实际生产中NaClO 作为最佳氧化剂,发生反
2、应的离子方程式为(3 ) “沉铜”步骤不选价格便宜的石灰乳,主要原因是会产生较多废渣,废渣主要成分的化学式为 。沉铜后,洗涤可以除去沉淀表面的 2种主要溶质是 (4)请在下图中完善所缺步骤及所添加试剂的化学式。可供选择的操作步骤有:萃取、蒸发浓缩、过滤、洗涤、降温结晶、蒸播、分液。()用心爱心专心5I :2、为了预防碘缺乏病,有关部门规定食盐中的碘含量(以 I计)应在2050 mg/Kg。制备KIO3的方法如下:方法 1: 612+11KClO3+3KO= 6KH(IO3)2+5KCl+3Cl 2 T方法2:碱性条件下,KI + 3HO错误!未找到引用源。KIO3+ 3H2T 方法 3:KH(
3、IO3)2 + KOH= 2KIO3+ H2O+H2O2 H12 70 cK2CO3HIO 3,KIO 3(1)与方法 3相比方法1的不足是、方法2的不足是(2)方法2选用的电极是惰性电极,则其阳极反应式是 。(3)方法3反应温度控制在70c左右.,不采用更高温度的主要原因是 。(4)制备纯净KIO3的实验步骤中,最后需将所得晶体最好使用 洗涤2-3次,干 燥后得产品。(5)已知:KIQ+5KI+3屋SO=3K2SO+312+3屋O; I 2+2S2Q2=21 一 + 3Q2,为测定加碘食盐中碘的含量,设计的方案如下。请完善实验步骤并计算测定结果:a.准确称取wg食盐于锥形瓶中,再加适量蒸储水
4、使其完全溶解。b.。c.向锥形瓶中滴加2.0 X 1 0 3 mol/L Na 2S2O3标准溶液至终点。d.重复上述实验两次。三次实验的数据记录如右表。则所测加碘食盐样品中的碘元素含量是mg/kg滴定次数盛标推Na:S;a溶液的读数滴定前刻度(mL)潘定后刻度( tqL)LL.02L1 0372.0011m10.2010.20(以含w的代数式表示)3、食盐是日常生活的必需品,也是重要的化工原料。(1)粗食盐常含有少量 K+、Cs2+、Md+、Fe3+、SO2-等杂质离子,实验室提纯 NaCl的流程 如下:提供的试剂:饱和 N&CO溶液饱和K2CO溶液 NaOH溶液 BaCl 2溶液洗/除去K
5、:)朋匚雇嬴v ) 2L , 原 因 是欲除去溶液I中的Cs2+、Mj、Fe3+、SO2-离子,选出a所代表的试剂,按滴加顺序依次为 (填化学式);滤液中滴加盐酸调PH=4-5的目的是,选用75叱醇洗涤除去 NaCl晶体表面附带的少量KCl,检验NaCl是否洗净的方法(2)用提纯的NaCl配制480mL 4.00 mol L-1NaCl溶液,需要称取的质量为g所用仪器除药匙、玻璃棒、烧杯外还有 (填 仪器名称);(3)电解饱和食盐水的装置如图所示,若收集的H2为2L,则同样条件下收集的Cl2 (填“”、“=”或4、馍电池广泛应用于混合动力汽车系统,电极材料由Ni(OH)2、碳粉、氧化铁等涂覆在
6、铝箔上制成。由于电池使用后电极材料对环境有危害。某兴趣小组对该电池电极材料进行资源回收研究,设计实验流程如下:Ni(OH)3已知:NiCl 2易溶于水,Fe不能氧化Ni。已知实验温度时的溶解度:NiC2C4 NiCzQ H 2。 NiC2。 2H2O某温度下一些金属氢氧化物的心及沉淀析出的理论 pH如下表所示:M(OH)KSp开始沉淀pH沉淀完全pHAl(CH) 31.9 X 10 233.44.2Fe(CH)33.8 x 10 382.52.9Ni(CH)21.6 x 10 147.69.8回答下列问题:(1)用NiC调节溶液的pH,依次析出沉淀I 和沉淀H ,(填化学式)。(2)写出加入N
7、aGQ溶液的反应的化学方程式: 。(3)检验电解滤液时阳极产生的气体的方法: 。(4)写出“氧化”反应的离子方程式: 。(5)如何检验 Ni(CH)3已洗涤干净? 。5、2011年8月12日,网上传云南曲靖市越州镇有总量5000余吨的重毒化工废料铭渣由于非法丢放,毒水被直接排放南盘江中。I :某工厂对制革工业污泥中Cr(III)回收与再利用工艺如下(硫酸浸取液中金属离子主要It33+t .1t_3+_ . 3+22+n . 2 +、是 Cr ,其次是 Fe、Al 、Ca、Mg ):4.3 mil L”部分阳离子常温下以氢氧化物形式沉淀时溶液的pH见下表:阳离子L 3 +FeL 2 +FeMcj
8、 +Al3+Cu2+Cr3+开始沉淀时的pH1.97.04.7沉淀完全时的pH3.29.011.186.79(9 溶解)(1)实验室用18.4 mol L一的浓硫酸配制250 mL 4.8 mol L的硫酸溶液,所用的玻璃仪器除烧杯、玻璃棒和吸量管 (一种能精确量取一定体积液体的仪器)外,还需(2)酸浸时,为了提高浸取率可采取的措施是 (至少答一点)。加入H2Q的作用是。调节溶液的pH= 8是为了除去 离子。(4)钠离子交换树脂的原理为:Mn+ + nNaR - MR+ nNa+ ,被交换的的杂质离子 (5)还原过程发生以下反应(请配平):Na 2C2Q+ SO 2+ = Cr(OH)(H 2
9、O)5SO+ Na 2SO;n: (1)工业废水中常含有一定量的C2。 步骤2中控制生成的硫酸亚铁中不含硫酸铁的方法是 在0-60C范围内,从硫酸亚铁和硫酸钱的混合溶液中可获得硫酸亚铁俊晶体的原 因是 。 为了从步骤3所得溶液中获得硫酸亚铁俊晶体,操作是 测定硫酸亚铁钱晶体中 Fe2+含量的步骤如下:步骤1:准确称取硫酸亚铁俊晶体样品ag(约为0. 5 g),并配制成100 mL溶液;步骤2:准确移取25.0 mL硫酸亚铁钱溶液于 250 mL锥形瓶中;步骤3:立即用浓度约为 0.1 mol L -1KMnO溶液滴定至溶液呈稳定的粉红色,即为终仃 八、步骤4:将实验步骤l3重复2次。步骤1中配
10、制100 mL溶液需要的玻璃仪器是 和CrQ2,它们会对人类及生态系统产生很大损害,必须进行处理。其中一种处理方法为电解法:该法用 Fe做电极,电解含 C2Q2的酸性废水,随着电解进行,阴极附近溶液 pH升高,产生Cr(OH)3沉淀。阳极的电极反应式为。在阴极附近溶液 pH升高的原因是(用电极反应方程 式解释)。(2)含铭废水国家排放标准为 错误!未找到引用源。含量W 0.1000mg/L。取上述电解后的废水200.00mL,调节pH= 1后置于锥形瓶中,用浓度为 0.0001mol/L的KI溶液滴定,至滴定 终点时,用去KI溶液9.00mL。已知酸性条件下,被Cr2。2一氧化的产物为I 2。
11、用计算所得数据说明上述电解法处理后的废水是否符合国家排放标准。6、实验室用硫酸钱、硫酸和废铁屑剖备硫酸亚铁钱晶体的方法如下:步骤1:将废铁屑依次用热的碳酸钠溶液、蒸储水洗涤。步骤2:向盛有洁净铁屑的烧杯中稀HSQ溶液,水浴加热,使铁屑与稀硫酸反应至基本不再冒 出气泡为止。趁热过滤。步骤3:向滤液中加入一定量的(NH4)2SO固体表1硫酸亚铁晶体、磁甄A硫酸亚铁俊晶体的溶解度 (g/1 00 g H 2O)物质0C10C20C30 c40 c50 c60 cFeSO 7 H2O15.620.526.532.940.248.6/(NH4) 2SQ70.673.075.478.081.0/88.0(NH4) 2SQ - FeSO - 6H2012.517.221.028.133.040.044.6为获得样品中Fe2+的含量,还需补充的实验是用心 爱心 专心6用心 爱心 专心
- 温馨提示:
1: 本站所有资源如无特殊说明,都需要本地电脑安装OFFICE2007和PDF阅读器。图纸软件为CAD,CAXA,PROE,UG,SolidWorks等.压缩文件请下载最新的WinRAR软件解压。
2: 本站的文档不包含任何第三方提供的附件图纸等,如果需要附件,请联系上传者。文件的所有权益归上传用户所有。
3.本站RAR压缩包中若带图纸,网页内容里面会有图纸预览,若没有图纸预览就没有图纸。
4. 未经权益所有人同意不得将文件中的内容挪作商业或盈利用途。
5. 装配图网仅提供信息存储空间,仅对用户上传内容的表现方式做保护处理,对用户上传分享的文档内容本身不做任何修改或编辑,并不能对任何下载内容负责。
6. 下载文件中如有侵权或不适当内容,请与我们联系,我们立即纠正。
7. 本站不保证下载资源的准确性、安全性和完整性, 同时也不承担用户因使用这些下载资源对自己和他人造成任何形式的伤害或损失。
