 蛋白质含量的测定方法
蛋白质含量的测定方法


《蛋白质含量的测定方法》由会员分享,可在线阅读,更多相关《蛋白质含量的测定方法(3页珍藏版)》请在装配图网上搜索。
1、蛋白质的测定方法-凯氏微量法有手工滴定定氮和自动定氮仪定氮,实验者可根据经济条件设备而定。1.原理 蛋白质是含氮的有机化合物。食品与硫酸和催化剂一同加热消化,使蛋白质分解,分解的氨与硫酸 结合生成硫酸铵。然后碱化蒸馏使氨游离,用过量硼酸吸收后再以硫酸或盐酸标准溶液滴定,根据酸的 消耗量乘以换算系数,即为蛋白质含量。2NH(CH 1COOH+13H SO (NH XSO+6CO+12SO+16H O2 2 2 2 4 4 2 4 2 2 2(NH4)2SO4+2NaOH2NH3+2H2O+Na2SO42.方法本法参照 GB 5009.5 -85,适用于各类食品及饲料中蛋白质的测定。3.试剂所有试
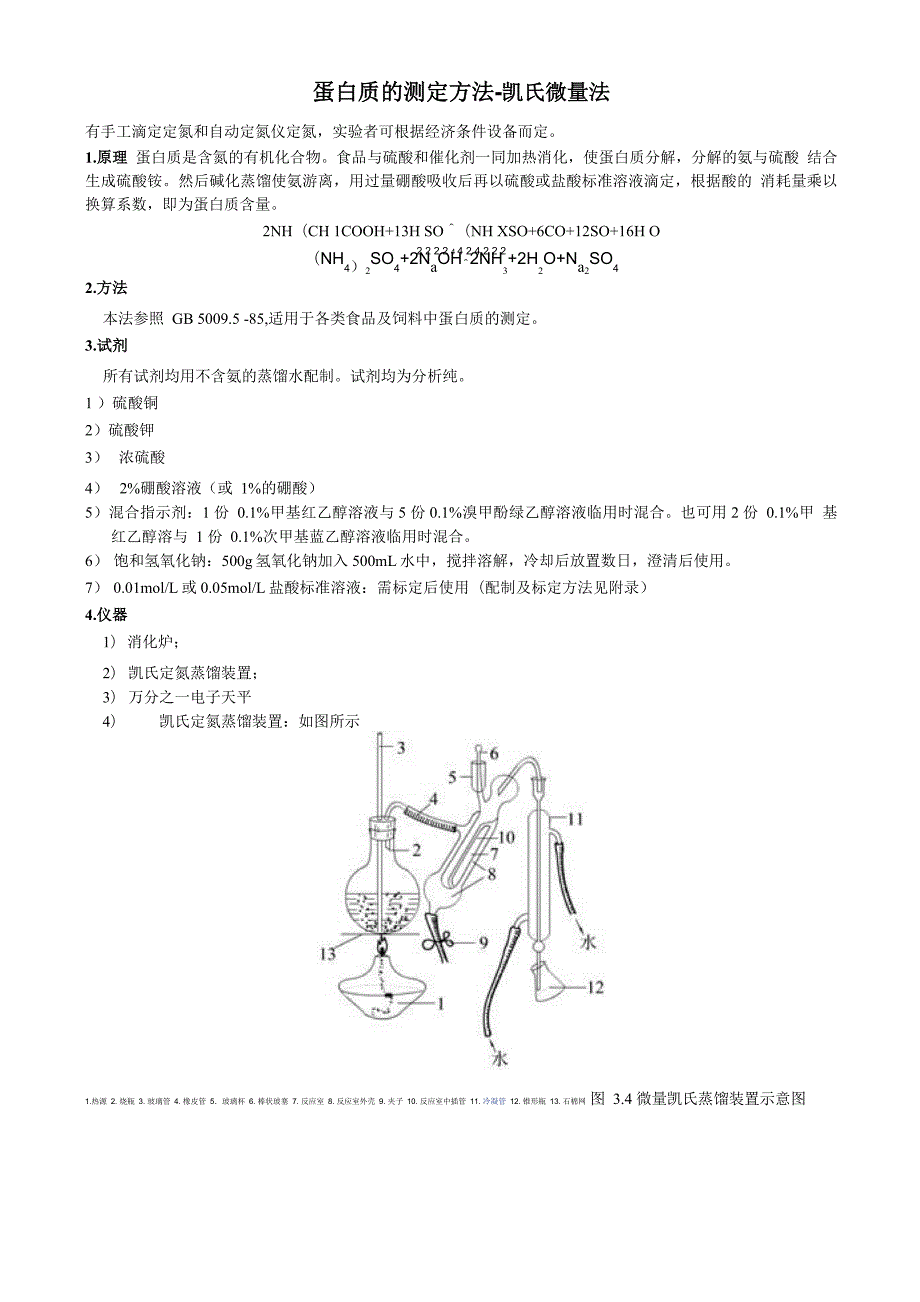
2、剂均用不含氨的蒸馏水配制。试剂均为分析纯。1 )硫酸铜2)硫酸钾3)浓硫酸4)2%硼酸溶液(或 1%的硼酸)5)混合指示剂:1 份 0.1%甲基红乙醇溶液与5 份0.1%溴甲酚绿乙醇溶液临用时混合。也可用2 份 0.1%甲 基红乙醇溶与 1 份 0.1%次甲基蓝乙醇溶液临用时混合。6)饱和氢氧化钠:500g氢氧化钠加入500mL水中,搅拌溶解,冷却后放置数日,澄清后使用。7)0.01mol/L或0.05mol/L盐酸标准溶液:需标定后使用(配制及标定方法见附录)4.仪器1)消化炉;2)凯氏定氮蒸馏装置;3)万分之一电子天平4)凯氏定氮蒸馏装置:如图所示1.热源 2. 烧瓶 3. 玻璃管 4.
3、橡皮管 5玻璃杯 6. 棒状玻塞 7. 反应室 8. 反应室外壳 9. 夹子 10. 反应室中插管 11. 冷凝管 12. 锥形瓶 13. 石棉网 图 3.4 微量凯氏蒸馏装置示意图消化装讹常暈IM氏定氣消化.蒸诩装首1水刀抽气徐2 水比头3饰宙的十燦怙1 注L氏境版5、7 电炉8 蒸倔烧帳6、9 级之柴 1O址申羊漏订12 按收版5. 操作步骤1 样品处理:精密称取 0.12.0g 固体样品或 25g 半固体样品或吸取液体样品 520mL ,放入 100mL 或 500mL凯氏烧瓶中,加入0.2g硫酸铜,0.3g硫酸钾及320mL浓硫酸,放置过夜后小心加热,待内容 物全部炭化,泡沫完全停止后
4、,加强火力,并保持瓶内液体微沸,至液体呈蓝绿色澄清透明后,取下 放冷后用约210mL蒸馏水冲洗瓶壁,混匀后继续加热至液体呈蓝绿透明,取下放冷,小心加1020mL 水混匀,放冷后,移入100mL容量瓶中,并用少量水洗定氮瓶,洗液并入容量瓶中,再加水至刻度, 混匀备用。取与处理样品相同量的硫酸铜、硫酸钾、硫酸按同一方法做试剂空白实验。2按图装好定氮装置,于水蒸气发生瓶内装水至约2/3处,加甲基红指示液数滴及数毫升硫酸,以保持 水呈酸性,加入数粒玻璃 珠以防暴沸,加热煮沸水蒸气发生瓶内的水。3向接收瓶内加入10mL ,12%硼酸溶液及混合指示液1滴,并使冷凝管的下端插入液面下,吸取10mL 样品消化
5、稀释液由小玻璃杯流入反应室,并以10mL水洗涤小烧杯使之流入反应室内,塞紧小玻璃杯的 棒状玻璃塞。将 310mL 饱和氢氧化钠溶液倒入小玻璃杯中,提起玻璃塞使其缓缓流入反应室,立即 将玻璃塞盖紧,并加水于小玻璃杯中以防漏气。加紧螺旋夹,开始蒸馏。蒸气通入反应室使氨通过冷 凝管而进入接收瓶内,蒸馏2min,移动接收瓶,使冷凝管下端离开液面,然后用少量中性水冲洗冷凝 管下端外部,再蒸馏1min取下接收瓶,以0.01或0.05mol/L盐酸标准溶液滴定至灰色或蓝紫色为终点。同时吸取10mL试剂空白消化液按5.3操作。6. 计算X =(V-V0)xCx 0.014x B/m x100x F式中:x样品
6、中蛋白质含量,g / 100g;0V样品消耗盐酸标准液的体积,mL ;V0空白消化液消耗盐酸标准液体积,mL;C盐酸标准液摩尔浓度,mol/L;0.0141mol/L盐酸标准液1 mL相当氮克数;B定容体积/取液量;m一样品的质量,g;F氮换算为蛋白质计算因子。蛋白质的氮素含量不同,故换算因子不同。详见下表。蛋白质计算因子 食物计算因子:蛋,鱼,肉及制品,禽类,玉米,高粱,豆类,水果和蔬菜类 6.25; 乳及乳制品 6.38;大米 5.95;小麦面 普通粉 5.70;全麦,大麦,燕麦,裸麦,小米,小麦面全麦 5.83; 小麦 5.80;黄豆 5.71;花生 5.46;芝麻、向日葵、核桃和榛子
7、5.30;麸皮 6.317. 举例设取样品0.1000g,消化后稀释至100 mL。取10 mL样品稀释液,标准盐酸为0.01 mol/L,空白滴 定为0.12 mL,样品滴定用去的标准盐酸为3.21 mL,测得样品中蛋白质百分率为: (3.21-0.12) x0.01x0.014x10/ 0.01x 100x 6.25 = (3.21-0.12) x8.75 = 27.0%8. 附录:(1)标准HC1溶液(0.1 mol/L HC1)配制及标定:配制:量取9毫升HC1,加适量水稀释至1000毫升。标定:精确称取约0.15克左右在270300C干燥至恒重的基准无水碳酸钠,加50毫升水使之溶解,
8、 加10滴溴甲酚绿-甲基红混合指示液,(量取30mL 0.2%溴甲酚绿乙醇溶液,加入20mL 0.1% 甲基红乙醇溶液,混匀)用配制的盐酸滴定至溶液由绿色变紫红色,煮沸2min,冷却至室温, 继续滴定至溶液由绿色变为暗紫色。同时做试剂空白实验。( 2)计算:C = m(V-V0)x0.0530CHCl标准滴定溶液的实际浓度,mol/L;m一基准无水碳酸钠的质量,g; V HCl标准滴定溶液用量,mL; V0试剂空白HC1标准滴定溶液用量,mL;0.05301.00 mL HCl标准滴定溶液C (HCl) =1mol/L相当基准无水碳酸钠g。0. 01mol/L HCl:精确吸取标定过的0.1m
9、ol/L HCl 10 mL,准确稀释至100毫升。必要时重新标定浓度。9.注意事项:1) 干样用称量纸称重连纸一同消化,空白管同样放称量纸消化。2) 含糖量高和油脂高的样品消化时容易溢出,加热要缓慢。3) 稀释样品时消化液过热,加水反应猛烈使样品损失;消化液 过冷,加水后盐析不溶解。食品中脂肪的测定方法 GB 5009.6-85 酸水解法1 原理:样品经酸水解后用乙醚提取,除去溶剂即得游离及结合脂肪总量。2 试剂:1. 盐酸2.95%乙醇。3. 乙醚。4. 石油醚。3 仪器 100mL 具塞刻度量筒。4 操作方法1. 样品处理1) 固体样品:精密称取约2g,置于50mL大试管内,加8mL水,
10、混匀后再加10mL盐酸。2) 液体样品:称取10.0g,置于50mL大试管内,加10mL盐酸。2. 将试管放入7080C水浴中,每隔510min以玻璃棒搅拌一次,至样品消化完全为止,约4050min。3. 取出试管,加入10mL乙醇,混合。冷却后将混合物移于100mL具塞量筒中,以25mL乙醚分次洗试 管,一并倒入量筒中。待乙醚全部倒入量筒后,加塞振摇1min,小心开塞,放出气体,再塞好,静置 12min,小心开塞,并用石油醚乙醚等量混合液冲洗塞及筒口附着的脂肪。静置1020min,待上部液 体清晰,吸出上清液于已恒量的锥形瓶内,再加5mL乙醚于具塞量筒内,振摇,静置后,仍将上层乙 醚吸出,放入原锥形瓶内。将锥形瓶置水浴上蒸干,置95105C烘箱中干燥2h,取出放干燥器内冷却 0.5h 后称量。
- 温馨提示:
1: 本站所有资源如无特殊说明,都需要本地电脑安装OFFICE2007和PDF阅读器。图纸软件为CAD,CAXA,PROE,UG,SolidWorks等.压缩文件请下载最新的WinRAR软件解压。
2: 本站的文档不包含任何第三方提供的附件图纸等,如果需要附件,请联系上传者。文件的所有权益归上传用户所有。
3.本站RAR压缩包中若带图纸,网页内容里面会有图纸预览,若没有图纸预览就没有图纸。
4. 未经权益所有人同意不得将文件中的内容挪作商业或盈利用途。
5. 装配图网仅提供信息存储空间,仅对用户上传内容的表现方式做保护处理,对用户上传分享的文档内容本身不做任何修改或编辑,并不能对任何下载内容负责。
6. 下载文件中如有侵权或不适当内容,请与我们联系,我们立即纠正。
7. 本站不保证下载资源的准确性、安全性和完整性, 同时也不承担用户因使用这些下载资源对自己和他人造成任何形式的伤害或损失。
