 过渡金属配合物的电子光谱
过渡金属配合物的电子光谱


《过渡金属配合物的电子光谱》由会员分享,可在线阅读,更多相关《过渡金属配合物的电子光谱(37页珍藏版)》请在装配图网上搜索。
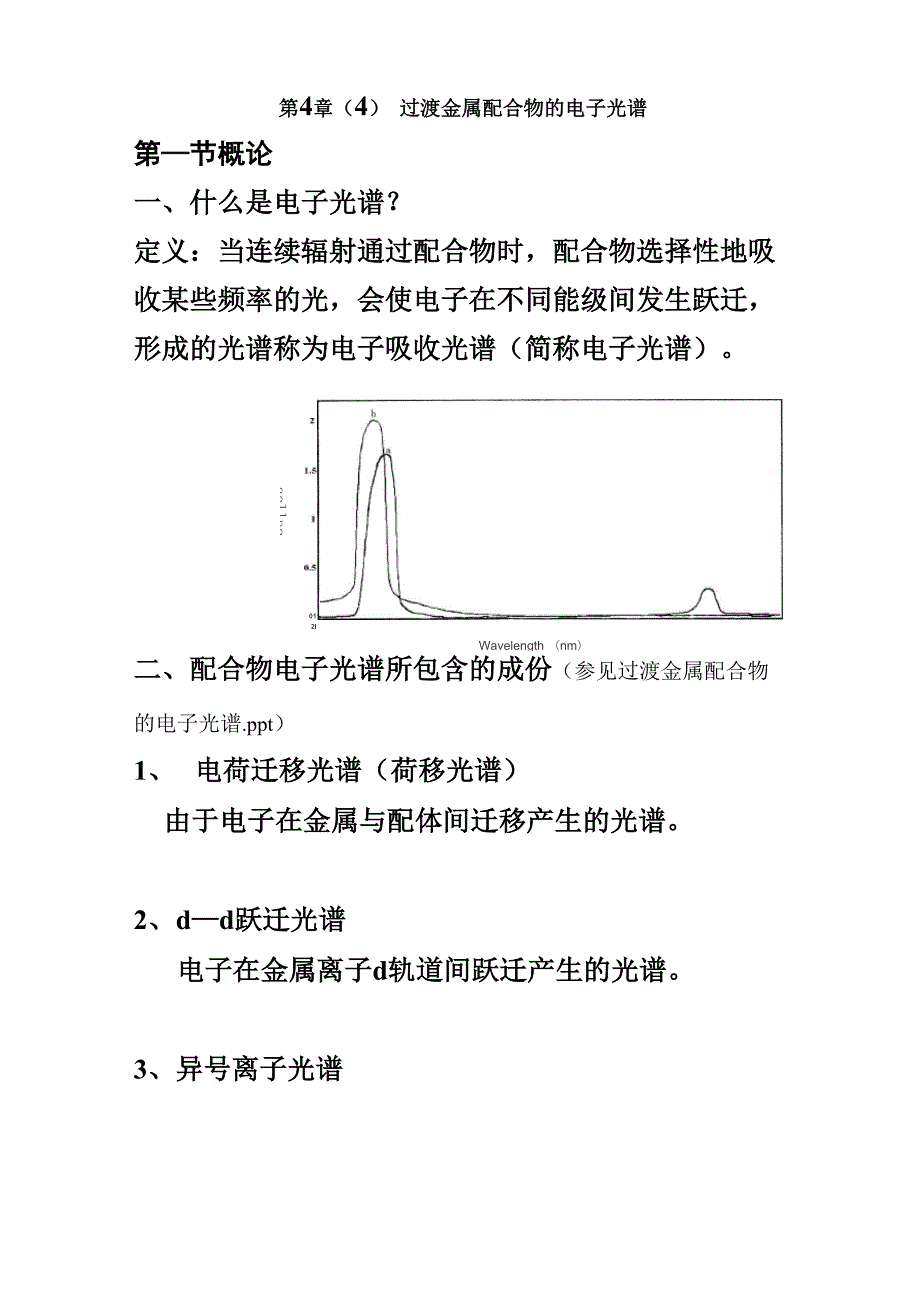
1、第4章(4) 过渡金属配合物的电子光谱第节概论一、什么是电子光谱?定义:当连续辐射通过配合物时,配合物选择性地吸 收某些频率的光,会使电子在不同能级间发生跃迁, 形成的光谱称为电子吸收光谱(简称电子光谱)。aollnqcIKql01 2IH 主1 .州0 .视 I -UHU颂 颇 成 0750300Wavelength (nm)二、配合物电子光谱所包含的成份(参见过渡金属配合物的电子光谱.ppt)1、电荷迁移光谱(荷移光谱)由于电子在金属与配体间迁移产生的光谱。2、dd跃迁光谱电子在金属离子d轨道间跃迁产生的光谱。3、异号离子光谱外界抗衡离子的吸收光谱。如Cu(NH3)4(NO3)2中NO3-
2、的吸收。4、配体光谱配体本身的吸收光谱。如Ti(H2O)63+中H2O的吸 收。第二节电荷迁移光谱异号离子光谱及配体光谱一、电荷迁移光谱1、L-M的跃迁以MCl6n-为例,分子轨道能级图:eg*VV3低能充满配体 t契t2g n群轨道egeg、t2g主要成份为配体轨道;而t2g*、eg*主要成份为 金属离子轨道。四种跃迁:v 1 = t1 2g2g=e3 ege *gL*2ge *g2、M-L的跃迁%*/配体高能空轨道/f2gt2g、eg*主要为金属离子轨道成份,而t2g*主要为配 体轨道。例:Co(CN)63-, ML 跃迁,v 1=4950000-1一、异号离子光谱可分为三种情况:1、在紫
3、外区有吸收,如NO厂,NO,-;322、在可见区有吸收,如CrO42-、MnO4-;3、无吸收,如 Cl-、SO42-、ClO4-。由于ClO4-既无吸收,配位能力又差。因此测定 水合离子的光谱时,为防止水解现象,常加入HClO4。 如测定Ti(H2O)63+的光谱时,若在HCl中进行,则吸 收峰移向长波方向。三、配体光谱=1配体如水、有机分子通常在紫外区有吸收。形成配 合物后,这些谱带仍保留在配合物的光谱中,吸收峰 位置有可能发生移动。第三节dd跃迁光谱一、概论不考虑d电子间相互作用时,d2组态的能态分析:基态激发态1激发态2二、d电子间相互作用(谱项与基谱项;又称光谱项、 光谱支项)原子光
4、谱的光谱项符号是:2S+1L或2s+1 L其构 J量量成方法为:(1)用字母表示总轨道为动量量子数L的值,对应规则是L=0,1, 2,3, 4,-S,P,D,F,G,;(2)用数字表示光谱项的多重性2S+1, 其中S为原子的总自旋角动量量子数;(3)谱项的支 项用右下标的J值加以区分;原子总角量子J的取 值为L + S,L + S -1,L - S)。一个原子 的一定的电子组态存在多个能级,相应就可以有多个 原子光谱项;每个光谱项可有多个光谱支项,代表精 细的能级;每个光谱支项还对应有2J +1个量子态, 说明精细能级在外磁场中会进一步分裂。1、单电子运动的描述运动: 自旋运动轨道运动描述:自
5、旋角动量s轨道角动量lI s | =s(s+1)i/2(h/2n) I l I =l(l+1) i/2(h/2 n )自旋角量子数s=1/2i =虹&轨道角量子数l=JI三m注*矢量用黑体字母表示。*角动量:就是质量乘以角速度(单位 角度/秒)。自旋角动量: 角动量是由物体自旋产生的,而不是外力给它的。轨道角动量:角动量是由轨道运动产生的2、电子间相互作用在多电子体系中,4与I.主要是通过电性相互作用;而札与1.或s.之间则主要通过磁性作用。Si A sj对轻元素(原子序数30),电子间偶合强于电子内偶 合,即:11. Js.Sj的作用要大于s.1.的作用。此时电子间相互作用,可用L-S偶合方
6、案处理:(参见LS偶合方案.pdf)SiL (总轨道角动量)I三I三三S (总自旋角动量)I三I三三即可用L、S描述多电子体系的状态。I S | =S(S+1)i/2(h/2 n )| L |=L(L+1) i/2(h/2 丸)S总自旋角量子数L总轨道角量子数如何求S、L见“物质结构气3、dn组态金属离子的谱项多电子体系的能量状态可用谱项符号表示:2S+1L L012345符号SPDFGH(2S+1)为谱项的自旋多重度。如S=1/2, L=2时,为 2D谱项。组态 谱 项3F, 3P, 1G, 1D, 1Sd1 d92Dd2 d84F, 4P, 2H, 2G, 2F, 2X2D, 2P 5D,
7、 3H, 3G, 2X3F, 3D, 2X3P, 1I,d3 d7d4 d62xiG, 1F, 2xiD, 2xiSd56S, 4G, 4F, 4D, 4P, 2I, 2H, 2X2G,2x2G,2xF, 3x2D, 2P, 2S* dn体系,不考虑电子间作用时,只有一种能量状态。 考虑电子间作用后,产生多个能量状态(谱项)。di 体系除外,因其只含一个电子。1)定义:能量最低的谱项称为基态谱项(基谱项)。i=j4、基态谱项1) 如何确定基谱项?A、同一电子组态的各谱项中,自旋多重度最大量最者能量最低。8、在自旋多重度最大的各谱项中,轨道角量子数最大者能量最低。例:d2组态:3F (基)、3P
8、、1G、1D、1SC、根据上述原则,可用下述方法求基谱项(对d轨道l = 2):轨道磁量子数(S基谱项210-ms)2S+1L233202333Fd92D1/2 * 中2 E)、-S (I)三、自由离子谱项在配体场中的分裂1、研究谱项分裂的两种方法1)弱场方法适用条件:d电子间作用配体场与d电子的作用 方法:先考虑电子间作用得到谱项;再考虑配体场 对电子的作用得到配体场谱项。2)强场方法适用条件:d电子间作用 配体场与d电子的作 用方法:先考虑配体场对电子的作用得到强场组态; 再考虑电子间作用得到配体场谱项。2、弱场方法的处理1)谱项分裂的两条规则A、 不论谱项由哪个dn组态产生,相同配体场,
9、 对给定L的谱项分裂后得到的配体场谱项的数目 和类型是相同的。1=B、 如果忽略化学环境对电子自旋的影响,则一个 谱项被配体场分裂后产生的配体场谱项与原谱项 具有相同的自旋多重度。2)用群论方法讨论谱项的分裂由于单电子轨道波函数和谱项波函数在空间的分 布状况分别依赖于量子数l和L,若L=l,则该谱项波 函数在空间的分布状况类似于该单电子轨道波函数。 因此谱项波函数分裂的结果与单电子轨道波函数的分 裂结果相同。*下标g、u的用法:A、单电子轨道波函数,如果配体场无对称中心,则 不用这两个下标;若有对称中心,则l为偶数的轨道(s、d、g)用下标g,l为奇数的轨道(p、f)用下标u。B、对于谱项波函
10、数,如果配体场无对称中心,则不 用这两个下标;若有对称中心,则用g或u,取决于 产生这个谱项的电子组态中各个电子的单电子轨道波 函数的本质。我们感兴趣的来自dn组态的那些谱项,它们在中心对称场中全部是g特征状态。单电子轨道波函数的分裂轨道OhTdD4hsa.a.a.1g11gpt1ut1a2u+eue +t.g 2ge+t2a +b +b, +e1g 1g 2g gfa +t +to2u 1u 2ua +b +b +2e2u 1u 2u ua +e +L +t1g g 1g 2g2a +a +b +b +2e1g 2g 1g 2g gheu+2t1u+t2ua +2a +b +b +3e1u
11、2u 1u 2u ua1g+a2g+eg+t1g+2t2g2a1g+a2g+2b1g+2b2g+3egd2组态谱项波函数分裂的结果谱项OhTd1S1A1g1A13P3T1g3T11D1E +1T.ga2+t1+t2ai+e+t1+t2e+2t1+t2、+为+用1+2弓D4hA 1g3A2g+3Eg1E+1T,21A1g+1B1g+1B2g+1Eg3F3A2g+3Tig+3T2g3A2+3T1+3T23A2g+3B1g+3B2g+23Eg1G1A1Eg+1T1g+1T2g1A1+1E+1T1+1T221A1g+1A2g+1B1B2g+21Eg3、d1-d9组态离子基谱项在八面体场中的分裂由上述可
12、见,dn与d10-n产生的谱项的密切对应关 系,这种对应关系是电子与空穴互易的结果。4、欧格尔(Orgel)图I=JI三mi=JI三三1)定义:确定配体场分裂的大小和各能级的顺序 要做量子化学计算。将计算出的结果以图表示,图的 纵坐标为能量,横坐标为配体场强度,这种形式的图 就是著名的Orgel图。八面体场中d2金属离子的Orgel图如下:A o(cm-1)在图的最左端Ao=0处,是自由离子的谱项。这些 谱项在配体场中,随配体场强度增大,分裂亦越来越 大。2)不相交规则可以看出Orgel图中,有些线是直的,而有些是弯 曲的。其弯曲是由于相同标记的谱项相互排斥引起的。不相交规则:相同标记的谱项的
13、能量变化曲线永不i=jI三三相交,而且相互排斥,即它们相互弯曲开来。5、能量相关图1)能量相关图将配合物的弱场谱项与强场谱项间的关系用图表 示,即得到能量相关图。两条规则:A、弱场谱项与强场谱项间存在一一对 应关系。这是因为在配体场强度变化的过程中,其对 称性保持不变,因此每一种状态的数目必然是相同的; B、配体场强度变化过程中,各配体场谱项的能量变 化曲线遵守不相交规则。以d2组态金属离子八面体配合物为例:egt2gieg1谱项弱场谱项 强场组态中等场强场谱项2)强场谱项的推导4数目与类型当d电子轨道分裂到最大限度时,有如下三种强 场组态:%2、心、eg21=再约化为:Alg+Eg+Tlg+
14、T2g 再约化为:T2; 再约化为:A +A +E1g 2g g当开始减小环境同离子间的作用,使电子感受到彼 此之间相互作用时,它们开始偶合,产生了一组属于 整个组态的状态,这些状态的对称性质决定于单电子 表示的直积。t/。2户2;)5 (t2gXeg)eg2:(egXeg)这些就是由电子间相互作用产生的轨道状态波函数 的对称性。8、自旋多重度通过降低对称性将多维表示过渡到一维表示,先求出低对称性时状态的自旋多重度。由于对称性降低 后,自旋多重度保持不变,从而可由低对称性的自旋 多重度推出高对称性时状态的自旋多重度。Oh群的相关表该表指出当对称性降低时,Oh群的表示如何改变或分解为它的子群表示
15、。OhTdD-h 4hC4vD3C2hA igA1A igA1A1A gA&2gA2Bi igB1A2B gE gEA1g+B1gA1+B1EAg+BgT 1gT1A2g+EgA2+EA2+EAg+2BgT 2gT2B2g+EgB2+EA1+E2Ag+BgA 1uA2A 1uA2A1A uA, 2uA1B1uB2A2B uE uEA1u+B1uA2+B2EAu+BuT 1uT2A2u+EuA1+EA2+EAu+2BuT 2uT1B2u+EuB1+EA1+E例:eg2: A1g +A2g+ Eg将Oh对称性降低为D4hOuDnh4hAA1g1gA,B,2g1gE gA +B 1g1g,表示均过渡
16、到一维表示。2Au+BuOh现在要求出D4h中各谱项的自旋多重度。Oh中的 eg二重简并轨道在D4h中解除简并:D4h一划b1g组态 多重度谱项(直积)可能的自旋a1g2a1g1b1g1 3B 1gb 21g1A 1gA1A1g1gB1B ,1g1g7A1g后倒推出Oh中谱项的自旋多重度:Oh1A1g3Ao2g1EgD4h1A1g3B 1g1A1g+1B1g,例:t2g2: A1g+ Eg+T1g+T2g将Oh对称性降低为C2h,表示均过渡到一维表示。OhA1gEgC2hA gAg+BgT igT, 2gAg+2Bg2A+Bg g现在要求出c2h中各谱项的自旋多重度 2ht2g三重简并轨道在c
17、2h中解除简并:OC2hl %t2g 二ag(2)b.-g。Oh中的组态 旋多重度谱项(直积)可能的自%(1)2AgiAgag(2)2A giAgb 2AiAgggag(1)1bg13Bg,B giB,g,ag(2)1bg13Bg,B giB , g/ag(1)1ag(2)1A giA, g注意自旋多重度为3的谱项,即可倒推出Oh中谱项的自旋多重度:O.h2h1A.1AiggiEiA +iBggg3T3A +23B1gg!iT, 2g2iAg+iBgg再例:t2giegi:T1g+ T2g将Oh对称性降低为C2h,表示均过渡到一维表示。Ohlg2gC2hAg+2Bg2A+Bg gOh现在要求出
18、C2h中各谱项的自旋多重度。Oh中的t2g 及eg简并轨道在C2h中解除简并:2h一 bg(e)ag(e)a(t1) g、2g =二二ag(t2)_)组态 谱项(直积)旋多重度ag(t1)iag(e)1Ag3A gag(t1)1bg(e)1Bg3Bg,可能的自1Ag,1Bg,ag(t2)1ag(e)1Ag3Agag(t2)1bg(e)1Bg3Bg,bg(t)1ag(e)1Bg3Bgbg(t)1bg(e)1A,3Ag,1Bg,1Bg,总共:31Ag + 33Ag + 31Bg + 33Bg倒推出Oh中谱项的自旋多重度:h1g iT,2gC2h iAg+2iBg 2iAg+iBg3T1g3T2g3
19、Ag+23Bg 23Ag+3Bg四、光谱选律电子跃迁不可能发生在任意两个能级之间,根据量 子力学计算可得出电子跃迁所遵守的规则,即光谱选 律。1、跃迁选律1)自旋规则AS=0允许;AS0 禁阻即自旋多重度(2S+1)相同的谱项间的跃迁是允 许的。2)Laporte 规则具有相同对称性(g或u)的谱项间的跃迁是禁阻 的。2、破坏跃迁选律的机制如果严格遵循上述跃迁选律,则八面体配合物不会 出现d-d跃迁。1)对于ASO0的禁阻跃迁,可通过旋一轨偶合作用 实现跃迁。随着旋一轨偶合常数增大,其跃迁强度增 大,不过总的来说强度还是很弱。2)对于Laporte规则中心对称配合物:可通过“电子一振动偶合”机
20、制, 即电子波函数与振动波函数的偶合,获得跃迁强度。对于非中心对称配合物:可通过p-d轨道混合获得 跃迁强度。3、群表示理论对跃迁选律的解释 1)基本原理与选择定则2)“电子一振动偶合”机制3)电子一振动的偏振作用五、d-d跃迁光谱1、di和d9。自旋多重度为2的谱项只有一个:2D (基)ooTi(H2O)63+u =20300cm-iCu(H2O)62+u =12600cm-i4、d2和d8。自旋多重度为3的谱项有:3F (基)3PM oAoV(H2O)63+3A 一2g Ni(H2O)62+3T1g(F) 3T2g=17200cm-i =8700cm-i3T1g(P)=25600cm-13
21、T1g(F) =14500cm-13T1g(P) =25300cm-13、d3和d7。自旋多重度为4的谱项有:4F (基)4P4咿)oCrF63-Co(H2O)62+-4T1g(F)4A2g 一4%=14900皿14T =8000cm-i2g4T1g(F)=22700cm-i4A =16000cm-12g4T1g(P)=34400cm-14T1g(P)=19400cm-14、d4和d6。自旋多重度为5的谱项只有一个:5D (基)oCr(H2O)62+CoF63-u=?4的较低能量激发态有弱的跃迁。i=jI三mu =14000cm-i5、d5基态谱项自旋多重度为6,从基态到自旋多重度为Et6S6A1g4Eg(D) 4T2g(D)4纣四 4Eg(G) 4T2g(G) 4T 1g6A 1gA oMn(H2O)62+_4T = 18900cm-1 k1g4T2g(G) =23100cm-14Eg(G) = 24970cm-14A1g(G)=25300cm-14T2g(D) = 28000cm-i4Eg(D) = 29700cm-i六、谱带宽度实验发现电子吸收光谱并非线状光谱,吸收峰宽度约为 10003000cm-i。原因:电子跃迁的同时伴随振动的激发,即振动=i能级改变。振动时,配体场强度随配体平均位置而变动。例:
- 温馨提示:
1: 本站所有资源如无特殊说明,都需要本地电脑安装OFFICE2007和PDF阅读器。图纸软件为CAD,CAXA,PROE,UG,SolidWorks等.压缩文件请下载最新的WinRAR软件解压。
2: 本站的文档不包含任何第三方提供的附件图纸等,如果需要附件,请联系上传者。文件的所有权益归上传用户所有。
3.本站RAR压缩包中若带图纸,网页内容里面会有图纸预览,若没有图纸预览就没有图纸。
4. 未经权益所有人同意不得将文件中的内容挪作商业或盈利用途。
5. 装配图网仅提供信息存储空间,仅对用户上传内容的表现方式做保护处理,对用户上传分享的文档内容本身不做任何修改或编辑,并不能对任何下载内容负责。
6. 下载文件中如有侵权或不适当内容,请与我们联系,我们立即纠正。
7. 本站不保证下载资源的准确性、安全性和完整性, 同时也不承担用户因使用这些下载资源对自己和他人造成任何形式的伤害或损失。
最新文档
- 《认识角》ppt教学讲解课件
- 《从数据谈节水》数据的收集、整理与描述优秀教学ppt课件
- 人员配置-公司组织架构与人员配置计划课件
- 《认识分式》ppt课件
- 《从百草园到三味书屋》第一课时ppt课件
- 公路工程概预算三课件
- 中考物理专题突破-综合能力题教学课件
- 《创新设计》高考英语二轮复习(江苏专用)ppt课件:第二部分-基础语法巧学巧练-专题八-非谓语动词
- 中考物理专题复习课件:滑轮及滑轮组
- CIM安全标识统一规划课件
- 中考物理专题复习教学课件-质量和密度
- 《处理民族关系的原则平等团结共同繁荣》ppt课件
- 中考物理专题复习之物理实验和探究题复习指导教学课件
- 《十二人人都会有挫折》初中心理健康教育闽教版《中学生心理健康》七级课件
- Cisco无线网络-安全-Brief课件
