 元素周期律元素周期表基础知识
元素周期律元素周期表基础知识


《元素周期律元素周期表基础知识》由会员分享,可在线阅读,更多相关《元素周期律元素周期表基础知识(6页珍藏版)》请在装配图网上搜索。
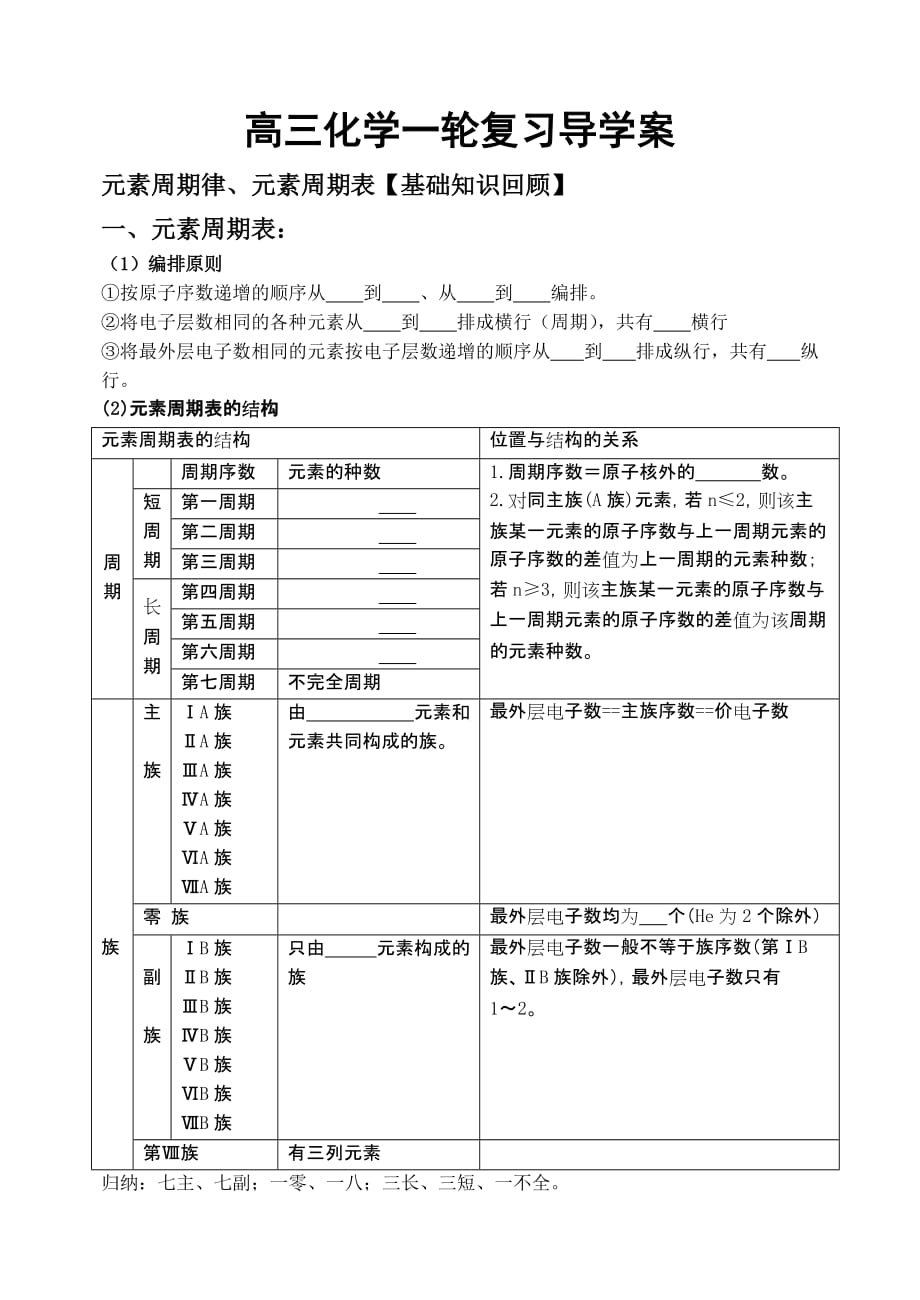
1、高三化学一轮复习导学案元素周期律、元素周期表【基础知识回顾】一、元素周期表:(1)编排原则按原子序数递增的顺序从 到 、从 到 编排。将电子层数相同的各种元素从 到 排成横行(周期),共有 横行将最外层电子数相同的元素按电子层数递增的顺序从 到 排成纵行,共有 纵行。(2)元素周期表的结构元素周期表的结构位置与结构的关系周期周期序数元素的种数1.周期序数原子核外的 数。2.对同主族(A族)元素,若n2,则该主族某一元素的原子序数与上一周期元素的原子序数的差值为上一周期的元素种数;若n3,则该主族某一元素的原子序数与上一周期元素的原子序数的差值为该周期的元素种数。短周期第一周期 第二周期 第三周
2、期 长周期第四周期 第五周期 第六周期 第七周期不完全周期族主族A族A族A族A族A族A族A族由 元素和 元素共同构成的族。最外层电子数=主族序数=价电子数零 族最外层电子数均为 个(He为2个除外)副族B族B族B族B族B族B族B族只由 元素构成的族最外层电子数一般不等于族序数(第B族、B族除外),最外层电子数只有12。第族有三列元素归纳:七主、七副;一零、一八;三长、三短、一不全。(3)相互关系原子序数_数_数核外_数。问题思考1(1)最外层电子数是2的元素都是第A族吗?(2)同周期第A和第A族元素的原子序数一定相差1吗? 问题思考2.观察元素周期表,确认每一纵行各代表哪一族,如:按从左 右的
3、顺序排列,第3纵列是_族,第15纵行是_族,第9纵列是_族,B族在第_纵列,A族处于_纵列等。右的顺序排列,第3纵列是_族,第15纵行是_族,第9纵列是_族,B族在第_纵列,A族处于_纵列等。3若某离子最外层电子数与次外层电子数相同,则它位于元素周期表的什么位置? 4电子层结构相同的离子,它们一定位于同一周期吗? 二、元素的性质与原子结构1、碱金属元素名称和符号锂(Li)钠(Na)钾(K)铷(Rb)铯Cs结构原子序数311193755原子结构简图主要化合价+1+1+1+1+1相同点不同点原子半径离子半径金属活动性单质还原性阳离子氧化性物性颜色和状态_固体(_略有金色光泽)化学性质跟氧气反应2L
4、i+O2=2LiO4Na+O2=2Na2O2Na+O2Na2O2生成更复杂的氧化物生成更复杂的氧化物生成更复杂的氧化物跟卤素反应2M+X2=2M X(M、X2表示碱金属、卤素,以下同)与水反应2M+2H2O=2MOH+H2反应剧烈程度:_与酸反应2M+2H+=2M+H2与盐溶液反应(如CuSO4溶液)2M+2H2O+CuSO4=M2SO4+Cu(OH)2+H2制法2MCl2M+Cl2【小结归纳】通过上述图表分析可知:碱金属元素随着原子核电荷数的递增,在_和_方面,均表现出一定的_和_。但一般之中有特殊。由此可见同一主族元素性质具有一定的_和_。2.卤族元素:元素名称和符号原子结构原子序数917
5、3553结构示意图主要化合价-1-1,+1,+3,+5,+7-1,+1,+3,+5,+7-1,+1,+3,+5,+7相同点最外层电子数相同,都是 个电子不同点原子核外_不同,依次增大原子半径阴离子半径非金属活动性原子氧化能力阴离子还原能力物理性质颜色和状态 气体 气体 色 体易 色 体易 水中溶解性分解水依次递减有机溶剂分解溶剂溶解性依次增大化学反应与金属反应nX2+2M=2MXn 与大多数金属反应 反应快慢 与H2反应X2+H2=2HX 反应剧烈程度 与H2O反应2H2O+2F2=4HF+ O2Cl2+H2O= (反应较慢)Br2+H2O= (反应很慢)I2+H2O=HI+HIO(反应不明显
6、)与NaOH反应2F2+4NaOH=4NaF+O2+2H2OX2+2NaOH=NaX+NaXO+H2O(XCl,Br,I)置换反应先和溶液中的水反应X2+2Y-=2X-+Y2 (YCl,Br,I)置换能力(_)【小结归纳】a氟、氯、溴、碘四种非金属元素的非金属性强弱:b四种卤素单质的氧化性强弱:c卤化氢的稳定性强弱:三、元素周期律内容同周期元素(从左到右)同主族元素(从上到下)原子结构核电荷数电子层数最外层电子数原子半径元素性质主要化合价最高价氧化物对应水化物的酸碱性非金属的气态氢化物稳定性与形成难易还原性水溶液酸性单质的氧化性或还原性元素的金属性和非金属性元素周期律、元素周期表基础知识回顾答
7、案一、元素周期表:(1)编排原则左 右 上下左 右 七上 下 18(2)元素周期表的结构周期:2 8 8 18 18 32 电子层 族:长周期 短周期 长周期(3)质子核电荷电子问题思考1(1)不是,如0族的He,副族中很多元素最外层电子数也是2。(2)不一定,第二、三周期中相差1;第四、五周期中相差11(加副族和第族的10个纵行);第六周期相差25(因为有镧系)。2BA5133若为阴离子,则它位于第三周期,若为阳离子,则它位于第四周期。4不一定,若电性相同,则位于同一周期,若电性相反,则阳离子位于阴离子的下一周期。二、元素的性质与原子结构1、碱金属元素 相同点:最外层电子数相同,都是1个电子
8、原子核外电子层数不同,依次增多依次递增 依次递增 依次递增 依次递增 依次递减银白色 铯 LiNaKRbCs小结归纳:物理性质 化学性质 相似性 递变性 相似性 递变性2.卤族元素:氟(F) 氯(Cl)溴(Br)碘(I) 7 电子层数依次递增 依次递增 依次递减 依次递减 依次递增浅黄绿色 黄绿色 深红棕色 液 挥发 紫黑色固 升华F2、Cl2、Br2、I2 F2、Cl2、Br2、I2HCl +HClO HBr+HBrOCl2Br2I2小结归纳:FClBrI F2Cl2Br2I2 HFHClHBrHI三、内容同周期元素(从左到右)同主族元素(从上到下)原子结构核电荷数递增增大电子层数相同增多最外层电子数增多相同原子半径逐渐减小(1e8 e)逐渐增大元素性质主要化合价最高正价由17最低负价由41最高正价=族序数(O、F除外)非金属负价=-(8-族序数)最高价氧化物对应水化物的酸碱性碱性减弱酸性增强碱性增强酸性减弱非金属的气态氢化物稳定性与形成难易增强;难易减弱;易难还原性逐渐减弱逐渐增强水溶液酸性酸性逐渐增强酸性逐渐增强单质的氧化性或还原性还原性减弱氧化性增强还原性增强氧化性减弱元素的金属性和非金属性金属性逐渐减弱,非金属性逐渐增强金属性逐渐增强,非金属性逐渐减弱
- 温馨提示:
1: 本站所有资源如无特殊说明,都需要本地电脑安装OFFICE2007和PDF阅读器。图纸软件为CAD,CAXA,PROE,UG,SolidWorks等.压缩文件请下载最新的WinRAR软件解压。
2: 本站的文档不包含任何第三方提供的附件图纸等,如果需要附件,请联系上传者。文件的所有权益归上传用户所有。
3.本站RAR压缩包中若带图纸,网页内容里面会有图纸预览,若没有图纸预览就没有图纸。
4. 未经权益所有人同意不得将文件中的内容挪作商业或盈利用途。
5. 装配图网仅提供信息存储空间,仅对用户上传内容的表现方式做保护处理,对用户上传分享的文档内容本身不做任何修改或编辑,并不能对任何下载内容负责。
6. 下载文件中如有侵权或不适当内容,请与我们联系,我们立即纠正。
7. 本站不保证下载资源的准确性、安全性和完整性, 同时也不承担用户因使用这些下载资源对自己和他人造成任何形式的伤害或损失。
