 偏差管理规程GMP2010
偏差管理规程GMP2010
上传人:干***
文档编号:164274947
上传时间:2022-10-24
格式:DOCX
页数:2
大小:150.27KB
收藏
版权申诉
举报
下载


第1页 / 共2页

第2页 / 共2页
资源描述:
《偏差管理规程GMP2010》由会员分享,可在线阅读,更多相关《偏差管理规程GMP2010(2页珍藏版)》请在装配图网上搜索。
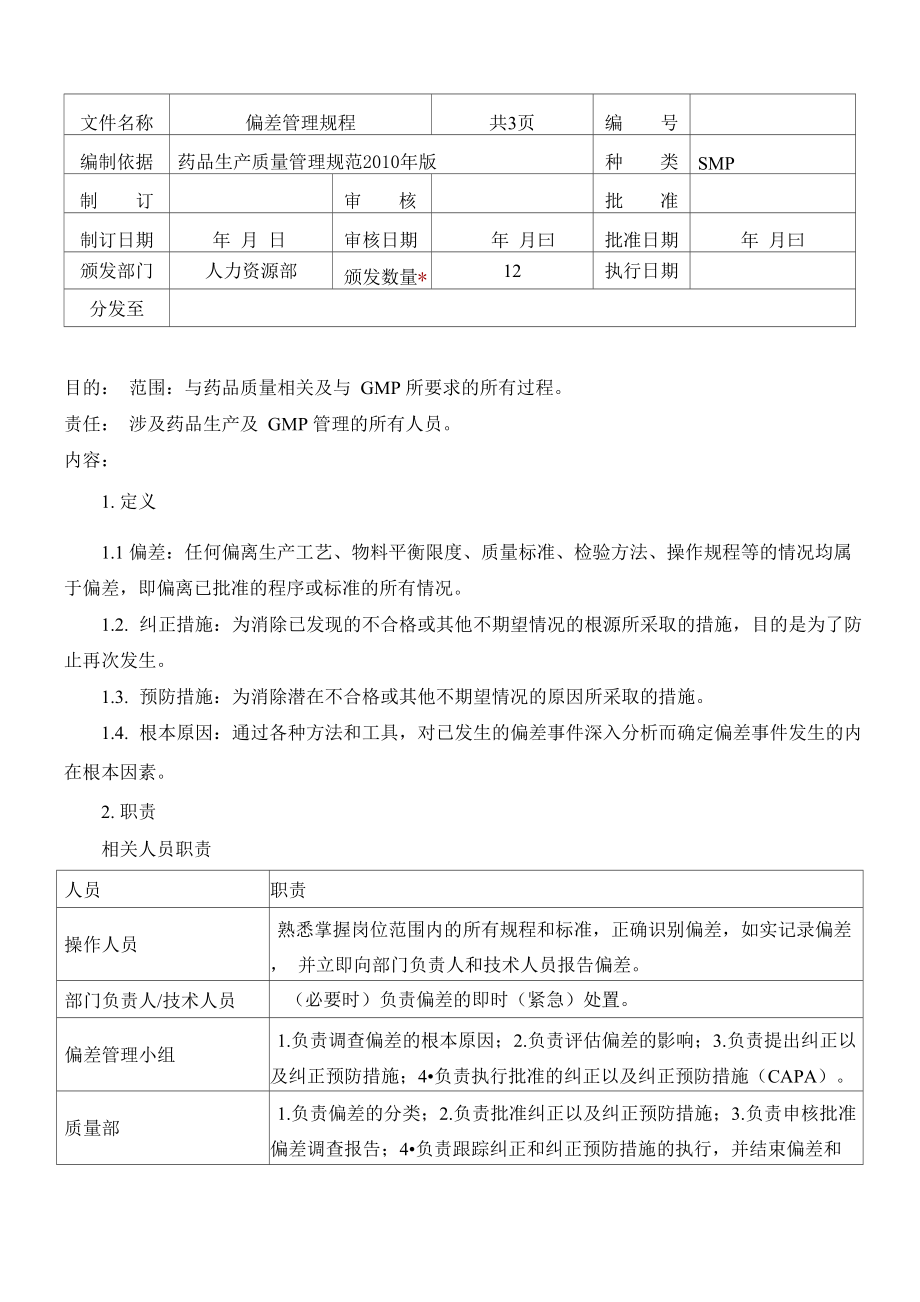
1、文件名称偏差管理规程共3页编号编制依据药品生产质量管理规范2010年版种类SMP制订审核批准制订日期年 月 日审核日期年 月曰批准日期年 月曰颁发部门人力资源部颁发数量*12执行日期分发至目的: 范围:与药品质量相关及与 GMP 所要求的所有过程。责任: 涉及药品生产及 GMP 管理的所有人员。内容:1. 定义1.1 偏差:任何偏离生产工艺、物料平衡限度、质量标准、检验方法、操作规程等的情况均属 于偏差,即偏离已批准的程序或标准的所有情况。1.2. 纠正措施:为消除已发现的不合格或其他不期望情况的根源所采取的措施,目的是为了防 止再次发生。1.3. 预防措施:为消除潜在不合格或其他不期望情况的
2、原因所采取的措施。1.4. 根本原因:通过各种方法和工具,对已发生的偏差事件深入分析而确定偏差事件发生的内在根本因素。2. 职责相关人员职责人员职责操作人员熟悉掌握岗位范围内的所有规程和标准,正确识别偏差,如实记录偏差, 并立即向部门负责人和技术人员报告偏差。部门负责人/技术人员(必要时)负责偏差的即时(紧急)处置。偏差管理小组1.负责调查偏差的根本原因;2.负责评估偏差的影响;3.负责提出纠正以 及纠正预防措施;4负责执行批准的纠正以及纠正预防措施(CAPA)。质量部1.负责偏差的分类;2.负责批准纠正以及纠正预防措施;3.负责申核批准 偏差调查报告;4负责跟踪纠正和纠正预防措施的执行,并结束偏差和
展开阅读全文
- 温馨提示:
1: 本站所有资源如无特殊说明,都需要本地电脑安装OFFICE2007和PDF阅读器。图纸软件为CAD,CAXA,PROE,UG,SolidWorks等.压缩文件请下载最新的WinRAR软件解压。
2: 本站的文档不包含任何第三方提供的附件图纸等,如果需要附件,请联系上传者。文件的所有权益归上传用户所有。
3.本站RAR压缩包中若带图纸,网页内容里面会有图纸预览,若没有图纸预览就没有图纸。
4. 未经权益所有人同意不得将文件中的内容挪作商业或盈利用途。
5. 装配图网仅提供信息存储空间,仅对用户上传内容的表现方式做保护处理,对用户上传分享的文档内容本身不做任何修改或编辑,并不能对任何下载内容负责。
6. 下载文件中如有侵权或不适当内容,请与我们联系,我们立即纠正。
7. 本站不保证下载资源的准确性、安全性和完整性, 同时也不承担用户因使用这些下载资源对自己和他人造成任何形式的伤害或损失。
