 化学计量在实验中的应用2
化学计量在实验中的应用2


《化学计量在实验中的应用2》由会员分享,可在线阅读,更多相关《化学计量在实验中的应用2(33页珍藏版)》请在装配图网上搜索。
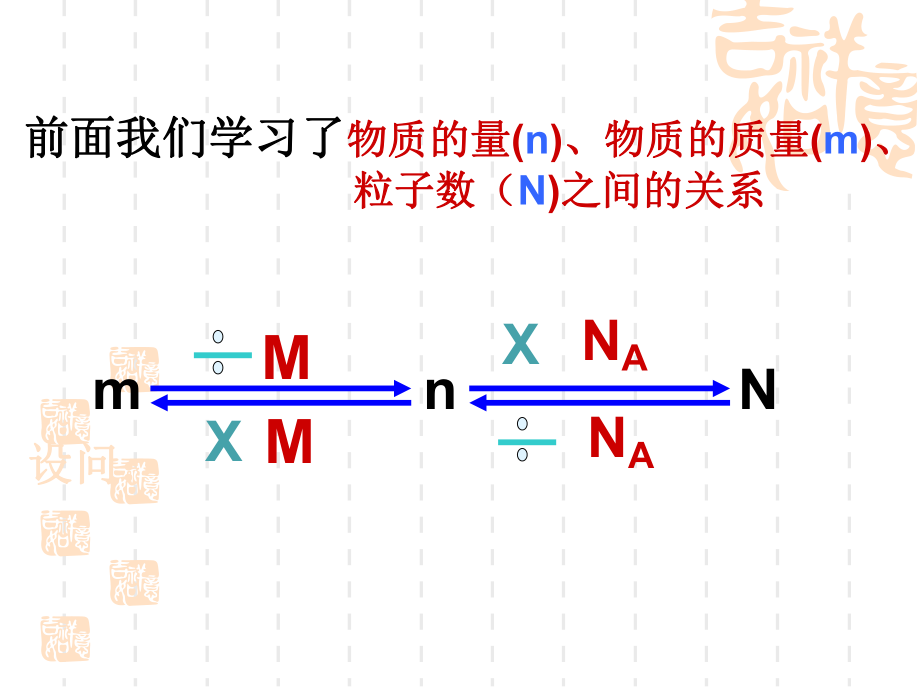
1、 前面我们学习了前面我们学习了物质的量物质的量(n)、物质的质量、物质的质量(m)、粒子数(粒子数(N)之间的关系之间的关系m n NMMXX NANA设问:设问:温故而知新1.8gH2O含有的氢原子数与gCH4 中含有的氢原子数相等。1.21.2化学计量在实验中的应用化学计量在实验中的应用第三课时第三课时 气体摩尔体积气体摩尔体积化学式化学式物质的量物质的量存在存在状态状态不同条件下的体积不同条件下的体积0、101KPa20、101KPa0、202KPaFe1mol固态固态7.2cm3NaCl1mol固态固态27.0cm3H2O1mol液态液态18.0cm3C2H5OH1mol液态液态58.
2、3cm3H21mol气态气态22.4L24.0L11.2LO21mol气态气态22.4L24.0L11.2LCO21mol气态气态22.4L23.9L11.2L结论结论:在相同温度和压强下,在相同温度和压强下,1mol1mol不同的固态或液态物质的体积不同的固态或液态物质的体积()而)而1 mol1 mol任何气体的体积(任何气体的体积()。)。各不相同各不相同几乎相同几乎相同 2、在同温同压下在同温同压下,1,1摩尔任何气体的体积基本相同摩尔任何气体的体积基本相同.3.标准状况标准状况(0、1.01105 Pa)下,下,1摩尔摩尔任何气体的体积约为任何气体的体积约为22.4L。1、在同温同压
3、下(在同温同压下(0、1.01105 Pa),),1 1摩尔摩尔固体和液体的体积各不相同。固体和液体的体积各不相同。由上表的体积数据结合物质状态你得出由上表的体积数据结合物质状态你得出什么结论什么结论?4.气体的体积与微粒种类无关。气体的体积与微粒种类无关。(2)为何为何1mol固体、液体的体积不同,而固体、液体的体积不同,而1mol气体的体积却基本相同呢?从微观角度分析气体的体积却基本相同呢?从微观角度分析,物质的体积由哪些因素决定物质的体积由哪些因素决定?(1)在相同条件下在相同条件下,为什么为什么1mol气体所占的体气体所占的体积比积比1mol固体或液体所占的体积大得多?固体或液体所占的
4、体积大得多?23456789 10气态物质分子平均距离是分子直径的气态物质分子平均距离是分子直径的10倍左右倍左右气体很容易被压缩气体很容易被压缩气态物质气态物质气态物质结构微粒间的距离很大气态物质结构微粒间的距离很大固态和液态物质结构微粒间的距离很小固态和液态物质结构微粒间的距离很小固体和液体是很难被压缩固体和液体是很难被压缩固态物质固态物质液态物质液态物质 因素因素状态状态粒子数目粒子数目粒子大小粒子大小粒子间平均粒子间平均距离距离固体和固体和 液液 体体 气气 体体1mol主要因素主要因素1mol次要因素次要因素主要因素主要因素从微观角度分析从微观角度分析,决定物质体积的三个因素决定物质
5、体积的三个因素次要因素次要因素忽忽 略略忽忽 略略回应质疑回应质疑 在相同的条件下,在相同的条件下,1mol1mol(即粒子数相同时)(即粒子数相同时)固体或液体的体积取决于固体或液体的体积取决于 粒子的大小粒子的大小1.1.在相同状况下,为什么在相同状况下,为什么1mol1mol的固态或的固态或液态物质体积不同?液态物质体积不同?答答:因为构成不同固体或液体物质的因为构成不同固体或液体物质的粒子大小不同粒子大小不同 在相同的条件下在相同的条件下,1mol(,1mol(即分子数相同时)即分子数相同时)气体的体积取决于气体的体积取决于分子间的平均距离分子间的平均距离2.2.相同状况下相同状况下1
6、mol1mol不同气体的体积为什么会不同气体的体积为什么会几乎相同呢?几乎相同呢?(请讨论后面的三个问题请讨论后面的三个问题)讨论讨论dn取决于取决于V气气dT Pd解决质疑解决质疑标况标况(STP):温度(:温度(0即即273k)、压强()、压强(101kPa)(V气气.L)T.P相同相同d相同相同相同相同气体分子间的气体分子间的平均距离平均距离与与分子种类分子种类基本基本无关无关。2.2.为什么在为什么在标况标况下下1mol1mol任何气体任何气体所占的体积都相所占的体积都相同呢?同呢?1.1.分子数相同的情况下,气体分子间的分子数相同的情况下,气体分子间的平均距离平均距离的受哪些的受哪些
7、条件条件影响?是怎样影响的影响?是怎样影响的?标况下气体摩尔体积标况下气体摩尔体积(Vm=22.4L/mol)理解理解要点:要点:标况标况1摩尔摩尔气体气体22.4升升Td,Pd,二者对分子间,二者对分子间平均距离平均距离的的影响可能影响可能相互抵消相互抵消,故可能为,故可能为22.4L。3.3.非标况下,非标况下,1mol气体的体积有没有可能等气体的体积有没有可能等于于22.4L呢?呢?1 1摩尔固体摩尔固体或液体的体积或液体的体积物质的体物质的体积积1 1摩尔气体摩尔气体的体积的体积微粒间微粒间的距离的距离决定于决定于主要决定于主要决定于主要决定于主要决定于微粒的微粒的多少多少微粒的微粒的
8、大小大小归纳与整理归纳与整理气体摩尔体积气体摩尔体积定义:单位物质的量气体所占的体积。定义:单位物质的量气体所占的体积。符号符号:Vm单位单位:L/mol(Lmol-1)和和m3/mol。公式:公式:Vm=Vn气体摩尔体积气体摩尔体积气体的体积气体的体积气体的物质的量气体的物质的量数值:数值:标准状况下标准状况下,气体摩尔体积约为气体摩尔体积约为22.4L/mol变形公式变形公式n=V/VmV=nVm22.4L(标准状况)标准状况)6.021023分子分子 0.282m标准状况下的气体摩标准状况下的气体摩尔体积示意图尔体积示意图标准状况下的气体摩尔体积标准状况下的气体摩尔体积理解要点理解要点:
9、条条 件:标准状况件:标准状况0、1.01105 Pa 对对 象:象:任何任何气体气体物质的量:物质的量:1mol结论结论体积体积约为约为22.4L特别注意:特别注意:(1)气体摩尔体积的数值不是固定不气体摩尔体积的数值不是固定不变的,它决定于气体所处的条件。变的,它决定于气体所处的条件。(2)在标准状况下在标准状况下,Vm22.4L/mol。(3)气体摩尔体积的对象只限于气体气体摩尔体积的对象只限于气体(纯净气体、混合气体均可使用)(纯净气体、混合气体均可使用)1.标准状况下,标准状况下,1mol1mol任何物质的体积都约是任何物质的体积都约是22.4L。(错,物质应是气体)(错,物质应是气
10、体)2.1mol气体的体积约为气体的体积约为22.4L。(错,应标明条件为标准状况)(错,应标明条件为标准状况)3.标准状况下,标准状况下,1molO2和和N2混合气体的体积约为混合气体的体积约为22.4L。(对,气体体积与分子种类无关)(对,气体体积与分子种类无关)4 4.22.4L气体所含分子数一定大于气体所含分子数一定大于11.2L气体所含的分子数。气体所含的分子数。(错,未指明相同条件下)(错,未指明相同条件下)5.标准状况下,气体的摩尔体积都是标准状况下,气体的摩尔体积都是22.4L。(错,(错,“约为约为”;单位应为;单位应为L/molL/mol)6.只有在标准状况下,气体的摩尔体
11、积才可能约为只有在标准状况下,气体的摩尔体积才可能约为22.4L/mol。(错,不一定)(错,不一定)随堂练习随堂练习:在标准状况下在标准状况下,2.2g CO2 的体积是多少?的体积是多少?n(CO2)=m(CO2)M(CO2)=2.2g44 g mol 1=0.05molV(CO2)=n(CO2)Vm=0.05 mol 22.4 L/mol=1.12L解:解:答答:-:-。随堂练习随堂练习2、标准状况下,、标准状况下,11.2L的的O2质量是多少质量是多少g?3、标准状况下,、标准状况下,10gH2的体积有多少的体积有多少L?1、标准状况下,标准状况下,672L的的O2物质的量是多少物质的
12、量是多少mol?4、标准状况下,、标准状况下,5.6升升O2中有多少个中有多少个O2分子?分子?30mol16g112L1.51023个个【例题【例题2】在标准状况下,测得】在标准状况下,测得1.92g某气体的体积某气体的体积为为672mL。计算此气体的相对分子质量。计算此气体的相对分子质量。14gH2与与22.4L(标准状况)(标准状况)CO2相比,所含分相比,所含分子数目多的是子数目多的是_;各;各1.5mol上述两种气体相比上述两种气体相比较,质量大的是较,质量大的是_。64H2CO22计算下列气体在标准状况下的体积。计算下列气体在标准状况下的体积。(1)2.8gCO (2)44gCO2
13、(3)64gSO2 (4)34gNH3 (5)含含1.204x1023个分子的个分子的HCl.3计算下列气体在标准状况下的密度。计算下列气体在标准状况下的密度。(1)H2 (2)O2(3)NH3 (4)CO2 相同条件下(同温同压),相同体积的任何气体相同条件下(同温同压),相同体积的任何气体都含有相同数目的粒子都含有相同数目的粒子由上述计算过程你能得出什么结论?由上述计算过程你能得出什么结论?=N1N2n1n2V1V2=推推 论论阿伏加德罗定阿伏加德罗定律律1、同温同压下,任何气体的体积之比等于、同温同压下,任何气体的体积之比等于物质的量之比,也等于粒子数之比。物质的量之比,也等于粒子数之比
14、。2、同温同压下,气体的、同温同压下,气体的 密度与其相密度与其相对分子质量成正比。对分子质量成正比。=M1M2d1d23、同温同体积的气体,压强与其分子数成正比。=n1n2P1p23.相同物质的量的相同物质的量的Fe和和Al分别与足量的稀盐酸反应,分别与足量的稀盐酸反应,生成的氢气在相同条件下的体积之比为多少?生成的氢气在相同条件下的体积之比为多少?1.在相同条件下,在相同条件下,0.5L的的H2与与1L的的O2所含的分子所含的分子个数比为多少,物质的量之比为多少?个数比为多少,物质的量之比为多少?2.在相同条件下,物质的量之比为在相同条件下,物质的量之比为1:4的的H2与与O2所所含的分子
15、个数比为多少,体积数之比为多少?含的分子个数比为多少,体积数之比为多少?随堂练习随堂练习1:21:42:301 mol H2O(18 mL)1001 mol H2O (g)(3.06104 mL)(体积扩大体积扩大1700倍倍)液态水变成水蒸气时,影响物质体积因素中,液态水变成水蒸气时,影响物质体积因素中,哪个变?哪个不变?决定因素是否发生变化?哪个变?哪个不变?决定因素是否发生变化?素材素材2P不变不变,T升高升高 分子间平均距离增大分子间平均距离增大气体体积变大气体体积变大T不变不变,P增大增大分子间平均距离减小分子间平均距离减小气体体积变小气体体积变小一定量的气体,当温度一定量的气体,当
16、温度或或压强发生变化时,气压强发生变化时,气体体积将如何变化?体体积将如何变化?PV=nRT理想气体状态方程:理想气体状态方程:注注R:常数,值约为常数,值约为8.314J/(molK)练习:练习:在同温同压下,同质量的下列气体占有的在同温同压下,同质量的下列气体占有的体积由大到小的顺序是体积由大到小的顺序是ClCl2 2 N N2 2 H H2 2 COCO2 2 O O2 2同温同压同体积同分子数即同物质的量同温同压同体积同分子数即同物质的量混合气体平均相对分子质量的求混合气体平均相对分子质量的求算算物质的相对分子质量在数值上与其摩尔质量物质的相对分子质量在数值上与其摩尔质量相等,故只要求
17、出混合气体的平均摩尔质量相等,故只要求出混合气体的平均摩尔质量即可。即可。1.已知标准状况下气体密度已知标准状况下气体密度,M M=22.4L/mol.2.根据摩尔质量定义法,用混合气体总质量根据摩尔质量定义法,用混合气体总质量除以总物质的量除以总物质的量 =m(总总)/n(总)(总).MM【例4】按体积比为1:2:3所组成的N2、O2、CO2混合气体100g,在标准状况下体积为()A.60L B.30L C.11.2L D.112LA【例题2】在标准状况下,测得1.92g某气体的体积为672mL。计算此气体的相对分子质量。12molO3和3molO2的质量之比为_;分子数之比为_;含氧原子的
18、数目之比为_;在相同条件下的体积比为_。24gH2与22.4L(标准状况)CO2相比,所含分子数目多的是_;各1.5mol上述两种气体相比较,质量大的是_。641:12:31:12:3H2CO23在相同的条件下,两种物质的量相同的气体在相同的条件下,两种物质的量相同的气体必然必然 A体积均为体积均为22.4L B具有相同的体积具有相同的体积C是双原子分子是双原子分子 D具有相同的原子数目具有相同的原子数目 4在相同条件下,下列气体中与在相同条件下,下列气体中与14gN2具有相具有相同分子数目的是同分子数目的是 A32gO2 B15g NOC34gNH3 D80gArBB5计算下列气体在标准状况下的体积。计算下列气体在标准状况下的体积。(1)2.8gCO (2)44gCO2(3)64gSO2 (4)34gNH36计算下列气体在标准状况下的密度。计算下列气体在标准状况下的密度。(1)H2 (2)O2(3)NH3 (4)CO2
- 温馨提示:
1: 本站所有资源如无特殊说明,都需要本地电脑安装OFFICE2007和PDF阅读器。图纸软件为CAD,CAXA,PROE,UG,SolidWorks等.压缩文件请下载最新的WinRAR软件解压。
2: 本站的文档不包含任何第三方提供的附件图纸等,如果需要附件,请联系上传者。文件的所有权益归上传用户所有。
3.本站RAR压缩包中若带图纸,网页内容里面会有图纸预览,若没有图纸预览就没有图纸。
4. 未经权益所有人同意不得将文件中的内容挪作商业或盈利用途。
5. 装配图网仅提供信息存储空间,仅对用户上传内容的表现方式做保护处理,对用户上传分享的文档内容本身不做任何修改或编辑,并不能对任何下载内容负责。
6. 下载文件中如有侵权或不适当内容,请与我们联系,我们立即纠正。
7. 本站不保证下载资源的准确性、安全性和完整性, 同时也不承担用户因使用这些下载资源对自己和他人造成任何形式的伤害或损失。
