 2014届高三12月考试
2014届高三12月考试


《2014届高三12月考试》由会员分享,可在线阅读,更多相关《2014届高三12月考试(5页珍藏版)》请在装配图网上搜索。
1、都江堰八一聚源高中2014届高中毕业班第一次诊断性模拟检测理综化学试题命题人:刘靖 审题人:袁贤俭可能要用到的相对原子质量:C-12 O-16 Si-28 Na-23 Fe-561.化学与生活密切相关,下列说法不正确的是A“地沟油”禁止食用,但可以用来制肥皂BPM2.5作为空气质量预报的一项重要指标,它是指空气中直径小于或等于2.5m的 颗粒物,该值越高,代表空气污染程度越严重C静电除尘治理悬浮颗粒污染,其依据是胶体的电泳原理D为消除碘缺乏症,卫生部规定食盐中必须加含碘物质,在食盐中所加含碘物质是KI2设NA为阿弗加德罗常数的数值,下列说法正确的是A8.2 g Na218O2与足量的CO2和H
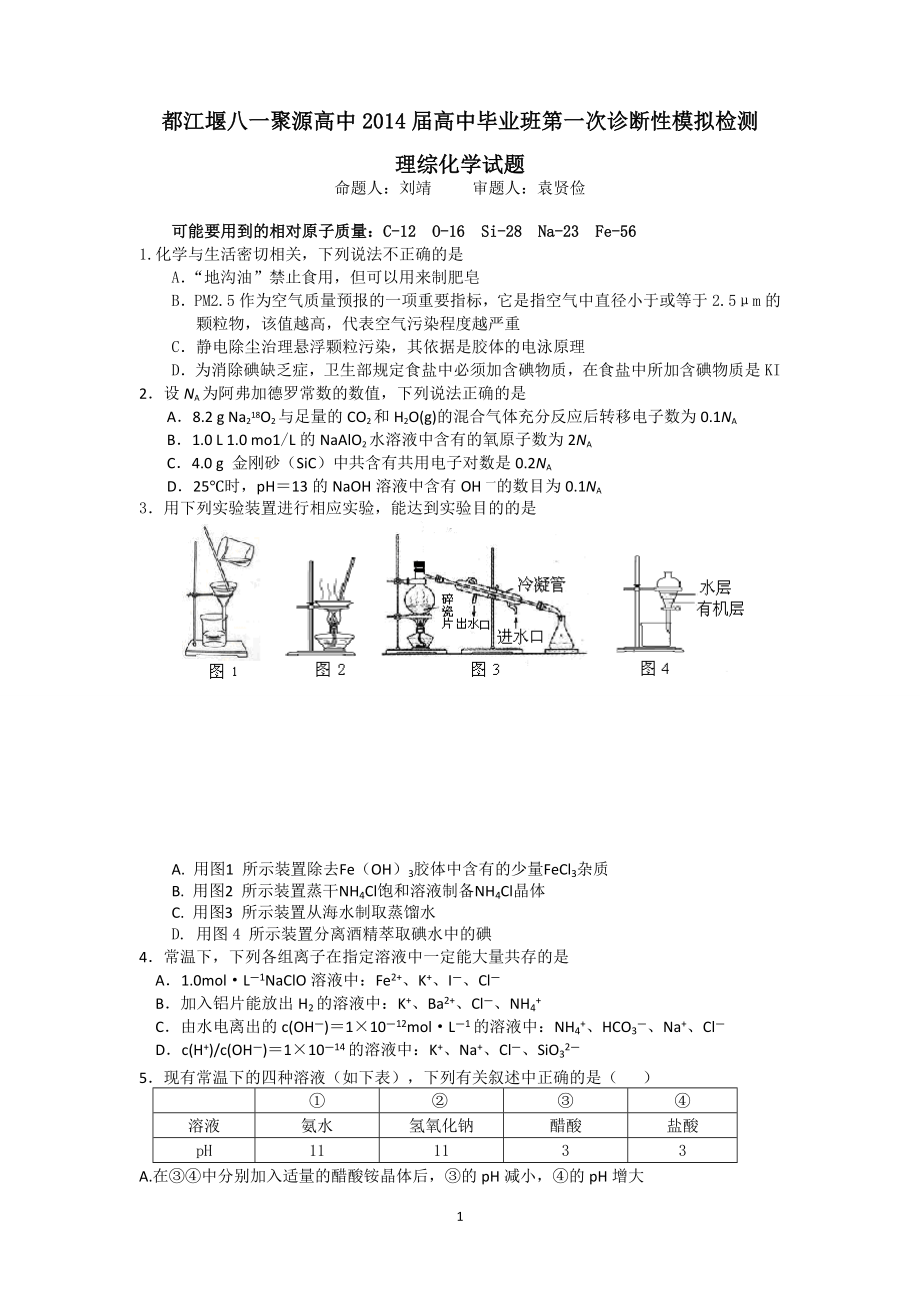
2、2O(g)的混合气体充分反应后转移电子数为0.1NAB1.0 L 1.0 mo1/L的NaAlO2水溶液中含有的氧原子数为2NAC4.0 g 金刚砂(SiC)中共含有共用电子对数是0.2NAD25时,pH13的NaOH溶液中含有OH一的数目为0.1NA3用下列实验装置进行相应实验,能达到实验目的的是A. 用图1 所示装置除去Fe(OH)3胶体中含有的少量FeCl3杂质B. 用图2 所示装置蒸干NH4Cl饱和溶液制备NH4Cl晶体C. 用图3 所示装置从海水制取蒸馏水D. 用图4 所示装置分离酒精萃取碘水中的碘4常温下,下列各组离子在指定溶液中一定能大量共存的是A1.0molL1NaClO溶液中
3、:Fe2+、K+、I、ClB加入铝片能放出H2的溶液中:K+、Ba2+、Cl、NH4+C由水电离出的c(OH)11012molL1的溶液中:NH4+、HCO3、Na+、ClDc(H+)/c(OH)11014的溶液中:K+、Na+、Cl、SiO325现有常温下的四种溶液(如下表),下列有关叙述中正确的是( )溶液氨水氢氧化钠醋酸盐酸pH111133A.在中分别加入适量的醋酸铵晶体后,的pH减小,的pH增大B.分别加水稀释10倍,四种溶液的pH为C.将两种溶液等体积混合,所得溶液中c(Na+)= c(CH3COO) + c(CH3COOH)D.将两种溶液等体积混合,所得溶液中c(Cl-)c(NH4
4、+)c(H+)c(OH-)6再生氢氧燃料电池(RFC)是一种将水电解技术与氢氧燃料电池技术相结合的可充电电 池。图为RFC工作原理示意图,下列有关说法正确的是图1 图2A图1把化学能转化为电能,图2把电能转化为化学能,水得到了循环使用Ba极上发生氧化反应,产生的气体X是H2C图2溶液中阳离子从B极流向A极Dc极上发生的电极反应是O2+2H2O+4e4OH7下列各表述与示意图一致的是A.图表示室温时,用0.1 mol/L盐酸滴定0.1 mol/LNaOH溶液过程中的pH变化B.T0C时,反应达到平衡时N02的体积分数 (N02) 随压强P的变 化如图所示,则A点的颜色深,B点的颜色浅 C.图表示
5、向绝热恒容密闭容器中通入A2和B2,一定条件下使反应达到平衡,正反应速率随时间变化的示意图。由图可得出的结论是:反应物的总能量低于生成物的总量 D.图在恒温恒容的密闭容器中,气体M存在如下关系,t1时刻,保持温度不变,再充入1 mol M,重新达到平衡时c(M)将增大8(16分)A、B、C、D、E五种短周期元素,F为第四周期过渡元素,核电荷数依次增加。元素有关性质及结构信息AA的一种原子内无中子BB原子的电子填充了4个原子轨道CC22离子与电负性最大的元素的单质互为等电子体DD是短周期金属性最强的元素EC与E同族F外围电子排布式为nd2n(n+1)s(n-1)(1) E2-基态核外电子排布式
6、;D2E的电子式为 ;B、C、D三种元素的第一电离能由大到小为 。(2)由A、B两种元素组成的非极性分子有多种,其中乙是一个分子含4个原子的的分子,乙的结构式是 。将1mol乙完全燃烧产生的气体慢慢通入含3molNaOH的溶液中,充分反应后,所得溶液中离子浓度由大到小为 。(3)甲是由A、B、C三种元素组成的相对分子质量最小的物质。甲的中心原子的杂化方式是 。(4)分别由A、C、D、E四种元素中的3种组成的两种物质丙和丁在溶液中反应生成气体和沉淀,该化学方程式是 。(5)C与D形成一种物质戊,将过量戊加入过量F与稀硫酸反应后的溶液,得到红褐色沉淀和气体,发生反应的离子方程式是 。9.(14分)
7、某酸性FeSO4溶液中含有少量的SnSO4,为得到纯净的FeSO47H2O晶体,可往溶液中通入H2S气体至饱和,然后用硫酸酸化至PH=2。过滤后,将所得滤液蒸发浓缩、冷却结晶、过滤洗涤,得到FeSO47H2O晶体。查询资料,得有关物质的数据如下表:250CPH250CPH饱和H2S溶液3.9FeS开始沉淀3.0SnS沉淀完全1.6FeS沉淀完全5.5(1) FeSO4溶液呈酸性的原因用离子方程式表示为 (2) 检验制得的绿矾晶体中是否含有Fe3+,可选用的试剂为 A.KSCN溶液 B.稀H2SO4 C.淀粉KI溶液 D.KMnO4溶液(3) 通入H2S至饱和的目的是 ;在溶液中用硫酸酸化至PH
8、=2的目的是 。(4) 某学习小组用“沉淀重量法”测定硫酸亚铁晶体中铁元素的含量。取17.0g样品溶于水,分别加入1mL稀H2SO4 、过量H2O2、NaOH溶液,过滤、洗涤、灼烧、冷却称量,得到固体4.8g。上述过程中的氧化剂除用H2O2外还可以用 代替。判断加入NaOH溶液是否过量的操作是 。假设实验无损耗,样品中铁元素的质量分数为 。10.(14分)生物质能是一种洁净、可再生能源。生物质气(主要成分为 CO、CO2、H2 等)与 H2 混合,催化合成甲醇和二甲醚(CH3OCH3)及许多烃类物质等,是生物质能利用的方法之一. (1)已知碳的气化反应在不同温度下平衡常数的对数值(lgK)如下
9、表:反应:CO(g)+H2O(g)CO2(g)+H2(g),该反应的H_0(选填:“”、“”、“”);在900K时,该反应平衡常数的对数值(lgK)=_.(2)甲醇是一种重要的能源和化工原料,工业上合成甲醇的反应为:CO+2H2CH3OH现已知:H2(g)、CO(g)、CH3OH(l)的燃烧热H分别为-285.8KJ/mol、-283.0KJ/mol和-726.5KJ/mol。则:CH3OH不完全燃烧生成CO和液态H2O的热化学反应方程式 .(3)在一定温度、压强和催化条件下,工业上用CO和H2反应生成二甲醚,同时产生一种参与大气循环的无机物。则该反应的化学反应方程式为: (4)下图左为绿色电
10、源“二甲醚燃料电池”的工作原理示意图a电极上发生反应的电极反应式为 .(5)连接下图右装置的电源为(4)问中的二甲醚燃料电池。接通电源一段时间后,观察到装置中电解质溶液颜色由无色变为蓝色,并逐渐加深。则该装置中的Cu电极应与二甲醚燃料电池中 电极(填a或b)相连。通电时发生反应的总的离子反应方程式为: . 11.(14分)I. 某校化学小组的同学进行以碳棒为电极电解氯化铜溶液时发现阴极碳棒上除了有红色物质析出外,还有少量白色物质析出。为探究阴极碳棒上的产物,设计了如下过程:、有关资料:铜的化合物颜色性质如下:物质颜色、性质物质颜色、性质氢氧化铜Cu(OH)2蓝色固体不溶于水硫酸铜(CuSO4)
11、溶液呈蓝色氧化亚铜(Cu2O)红色固体不溶于水氯化铜(CuCl2)溶液呈绿色,稀溶液呈蓝色氯化亚铜(CuCl)白色固体不溶于水碱式氯化铜绿色固体不溶于水、探究实验(1)提出假设:红色物质一定有铜,还可能有Cu2O;白色物质为铜的化合物,其化学式可能为CuCl(2)实验验证:取电解CuCl2溶液后的阴极碳棒,洗涤、干燥,连接下列装置进行实验,验证阴极产物实验结束后,碳棒上的白色物质变为红色,无水硫酸铜不变色。碳棒上的红色物质是否有Cu2O (填“是”或“否”),理由是 ;在c装置后将气体通入 中,若出现白色沉淀,可说明提出假设中的白色物质一定存在;写出装置b中发生反应的化学方程式: 。 II.(
12、1)用重铬酸钾法(一种氧化还原滴定法)可测得产物Fe3O4中二价铁含量。若需配制浓度为0.01000 mol/L的K2Cr2O7的标准溶液250 mL,应准确称取 g K2Cr2O7 (保留4位有效数字,已知M(K2Cr2O7)=294.0 g/mol)。配制该标准溶液时,下列仪器不必要用到的有 (用编号表示)。电子天平 烧杯 量筒 玻璃棒 容量瓶 胶头滴管 移液管 (2)滴定操作中,如果滴定前装有K2Cr2O7标准溶液的滴定管尖嘴部分有气泡,而滴定结束后气泡消失,则测定结果将 (填“偏大”、“偏小”或“不变”)。八一12月考试化学参考答案1D 2A 3C 4D 5B 6C 7D8.1s22s
13、22p63s23p6, H-CC-HSP2 Na2S2O3+H2SO4=S+SO2+Na2SO4+H2O 4Na2O2+4Fe2+6H2O=4Fe(OH)3+8Na+O29. (14分) (1)AC (2) 除去溶液中的Sn2+,并防止Fe2+被氧化; 使生成的FeS溶解并转化为FeSO4,减小Fe2+的损失(3) 氯水或其他合理的答案往上层清液中继续滴加NaOH溶液,若无沉淀生成,说明NaOH溶液已经过量。其他合理答案也可以。19.76%10.(14分,每空2分)(1); 0.36(2)CH3OH(l)+O2(g)=CO(g)+2H2O(l);H=-443.5KJ/mo(3):3CO+3H2 = (CH3)2O+CO2或者2CO+4H2 = (CH3)2O+ H2O,(4)(CH3)2O-12e-+3H2O=2CO2+12H+(5)b Cu+2H+=Cu2+H211. (14分,2分/空)I. 否 无水硫酸铜不变色,说明无水生成,红色物质不含有氧元素 硝酸银溶液2CuClH2 2Cu + 2HClII.(1)0.7350 (0.01000 mol/L0.250 L294.0 g/mol) (2)偏大5
- 温馨提示:
1: 本站所有资源如无特殊说明,都需要本地电脑安装OFFICE2007和PDF阅读器。图纸软件为CAD,CAXA,PROE,UG,SolidWorks等.压缩文件请下载最新的WinRAR软件解压。
2: 本站的文档不包含任何第三方提供的附件图纸等,如果需要附件,请联系上传者。文件的所有权益归上传用户所有。
3.本站RAR压缩包中若带图纸,网页内容里面会有图纸预览,若没有图纸预览就没有图纸。
4. 未经权益所有人同意不得将文件中的内容挪作商业或盈利用途。
5. 装配图网仅提供信息存储空间,仅对用户上传内容的表现方式做保护处理,对用户上传分享的文档内容本身不做任何修改或编辑,并不能对任何下载内容负责。
6. 下载文件中如有侵权或不适当内容,请与我们联系,我们立即纠正。
7. 本站不保证下载资源的准确性、安全性和完整性, 同时也不承担用户因使用这些下载资源对自己和他人造成任何形式的伤害或损失。
