 医疗器械使用质量管理自查表
医疗器械使用质量管理自查表


《医疗器械使用质量管理自查表》由会员分享,可在线阅读,更多相关《医疗器械使用质量管理自查表(10页珍藏版)》请在装配图网上搜索。
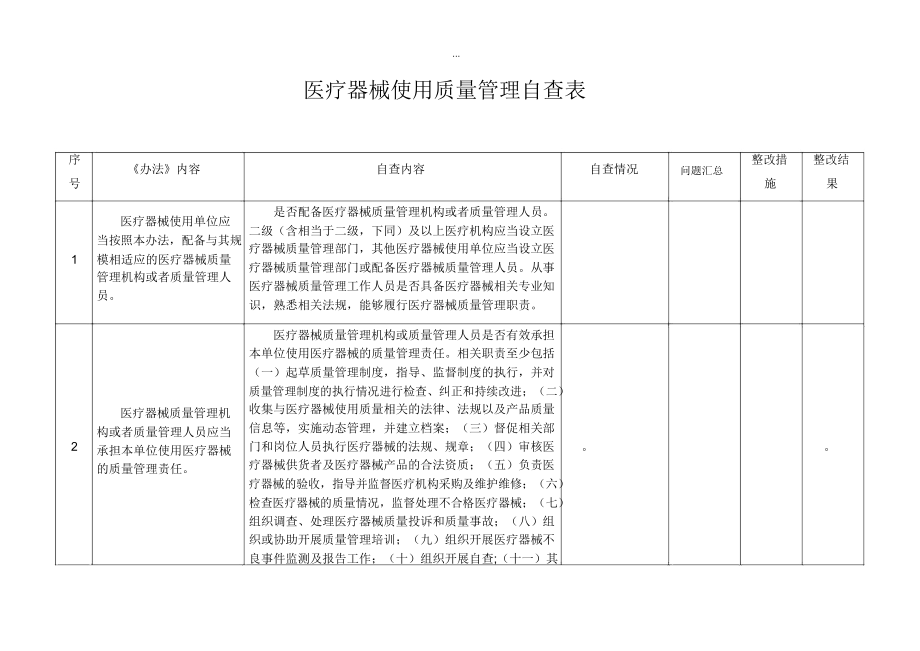
1、.医疗器械使用质量管理自查表序办法内容自查内容自查情况整改措整改结号问题汇总果施医疗器械使用单位应是否配备医疗器械质量管理机构或者质量管理人员。二级(含相当于二级,下同)及以上医疗机构应当设立医当按照本办法,配备与其规疗器械质量管理部门,其他医疗器械使用单位应当设立医1模相适应的医疗器械质量疗器械质量管理部门或配备医疗器械质量管理人员。从事管理机构或者质量管理人医疗器械质量管理工作人员是否具备医疗器械相关专业知员。识,熟悉相关法规,能够履行医疗器械质量管理职责。医疗器械质量管理机构或质量管理人员是否有效承担本单位使用医疗器械的质量管理责任。相关职责至少包括(一)起草质量管理制度,指导、监督制度
2、的执行,并对质量管理制度的执行情况进行检查、纠正和持续改进;(二)医疗器械质量管理机收集与医疗器械使用质量相关的法律、法规以及产品质量2构或者质量管理人员应当信息等,实施动态管理,并建立档案;(三)督促相关部。门和岗位人员执行医疗器械的法规、规章;(四)审核医承担本单位使用医疗器械疗器械供货者及医疗器械产品的合法资质;(五)负责医的质量管理责任。疗器械的验收,指导并监督医疗机构采购及维护维修;(六)检查医疗器械的质量情况,监督处理不合格医疗器械;(七)组织调查、处理医疗器械质量投诉和质量事故;(八)组织或协助开展质量管理培训;(九)组织开展医疗器械不良事件监测及报告工作;(十)组织开展自查;(
3、十一)其34.他应当由质量管理机构或者质量管理人员履行的职责。是否建立覆盖质量管理全过程的使用质量管理制度。相关质量管理制度至少包括:(一)质量管理机构或质量管理人员的职责;(二)供应商审核、采购、验收管理;医疗器械使用单位应 (三)库房储存管理、出入库管理;(四)维修、维护和当建立覆盖质量管理全过 保养;(五)使用前检查和植入类医疗器械使用记录管理;程的使用质量管理制度。 (六)转让与捐赠管理;(七)医疗器械追踪、溯源;(八)设施设备维护及验证和校准;(九)质量管理培训及考核;(十一)医疗器械不良事件监测及报告;(十二)质量管理自查;(十三)不合格品处置。医疗器械使用单位发现所使用的医疗器械
4、发生不良事件或者可疑不良事 是否建立不良事件监测报告制度,并按照医疗器械不件的,应当按照医疗器械不 良事件监测的有关规定报告和处理。良事件监测的有关规定报告并处理。56.医疗器械使用单位应当对医疗器械采购实行统一管理,由其指定的部门或 是否明确由专门机构或人员统一采购医疗器械。是否者人员统一采购医疗器械, 存在其他科室、部门或人员擅自采购的情形。其他部门或者人员不得自行采购。医疗器械使用单位应购进医疗器械时是否审查供货者资质、并至少索取留当从具有资质的医疗器械存以下证明文件:(一)营业执照复印件;(二)医疗器生产经营企业购进医疗器械注册证或者备案凭证复印件;(三)医疗器械生产、经械,索取、查验
5、供货者资质、营许可证和(或)备案凭证复印件;(四)销售人员的身医疗器械注册证或者备案份证明复印件和法人授权书原件;(五)进口医疗器械产凭证等证明文件。对购进的品通关文件;(六)标签和说明书样件复印件;(七)医医疗器械应当验明产品合疗器械相关票据原件。是否存在从未取得生产经营许可或格证明文件,并按规定进行者未办理备案的企业购进第二、三类医疗器械的情形。是验收。对有特殊储运要求的否对医疗器械逐批次进行验收,验明产品信息、产品合格医疗器械还应当核实储运证明文件、相关票据、储运条件和包装状况等。是否拒收条件是否符合产品说明书不符合验收要求的医疗器械。和标签标示的要求。789.医疗器械使用单位应是否建立
6、进货查验记录,其中进货查验记录内容应至当真实、完整、准确地记录少包括医疗器械的名称、型号、规格、数量、批号(生产进货查验情况。进货查验记批号、编号、序列号、灭菌批号等)、有效期、注册证号录应当保存至医疗器械规或备案凭证号、生产企业的名称、供货者的名称、联系方定使用期限届满后 2 年或式及相关许可证明文件编号、储运条件、到货日期、验收者使用终止后 2 年。大型医日期与结论并经验收人签字。查看相关记录,内容是否真疗器械进货查验记录应当实、完整、准确。需冷链管理的医疗器械的验收记录,是保存至医疗器械规定使用否记录运输方式、到货及在途温度、启运时间和到货时间期限届满后 5 年或者使用等信息;需进行安装
7、调试的医疗器械的验收记录,是否记终止后 5 年;植入性医疗器录安装调试合格的有关信息。进货查验记录的保存期限是械进货查验记录应当永久否满足要求。保存。医疗器械使用单位应是否妥善保存购入第三类医疗器械的原始资料,原始当妥善保存购入第三类医资料至少包括第三类医疗器械的供货者资质和产品注册证疗器械的原始资料,确保信合格证明、购进票据等原件或有效复印件。息具有可追溯性。医疗器械使用单位贮存医疗器械的场所、设施及 贮存医疗器械的场所、设施及条件是否与医疗器械品条件应当与医疗器械品种、 种、数量相适应,符合产品说明书、标签标示的要求,是数量相适应,符合产品说明 否具备防虫、防鼠、通风、照明等设施,对不合格
8、或待验书、标签标示的要求及使用 收的医疗器械等是否进行分区管理或张贴状态标识。对温安全、有效的需要;对温度、 度、湿度等环境条件有特殊要求的,是否配备温湿度监测、湿度等环境条件有特殊要 调节的设施,相关设施设备是否及时维护、校准并做好相求的,还应当监测和记录贮关记录,保证有效运行。存区域的温度、湿度等数.据。医疗器械使用单位应当按照贮存条件、医疗器械10是否定期检查医疗器械产品效期、外观、贮存设施设有效期限等要求对贮存的备情况等,并做好相关记录。医疗器械进行定期检查并记录。医疗器械使用单位不是否购进和使用未依法注册或者备案、无合格证明文得购进和使用未依法注册11件以及过期、失效、淘汰的医疗器械
9、。对发现的未依法注或者备案、无合格证明文件册或者备案、无合格证明文件以及过期、失效、淘汰的医以及过期、失效、淘汰的医疗器械是否采取处置措施。疗器械。医疗器械使用单位应当建立医疗器械使用前质量检查制度。在使用医疗器械前,应当按照产品说明书的有关要求进行检查。使用是否建立并执行医疗器械使用前质量检查制度。使用12 无菌医疗器械前,应当检查 医疗器械前是否按照产品说明书的有关要求进行检查,对直接接触医疗器械的包装 经检查不符合要求的医疗器械是否采取相关处置措施。及其有效期限。包装破损、标示不清、超过有效期限或者可能影响使用安全、有效的,不得使用。.医疗器械使用单位对 是否对植入和介入类医疗器械建立使
10、用记录并纳入信植入和介入类医疗器械应 息化管理系统,其中使用记录应至少包括以下内容:(一)当建立使用记录,植入性医 患者信息;(至少要明确患者姓名、住院号、手术信息)13 疗器械使用记录永久保存, (二)医疗器械的名称、型号、规格、数量、批号(生产相关资料应当纳入信息化 批号、序列号、灭菌批号等)、有效期、注册证号、生产管理系统,确保信息可追 企业的名称;(三)供货者的名称及相关许可证明文件编溯。 号;(四)其他必要的产品跟踪信息。医疗器械使用单位应当建立医疗器械维护维修管理制度。对需要定期检是否建立并执行医疗器械维护维修管理制度,明确人查、检验、校准、保养、维员对需要定期检查、检验、校准、保
11、养、维护的医疗器械,护的医疗器械,应当按照产14按照产品说明书的要求进行检查、检验、校准、保养、维品说明书的要求进行检查、护并记录,及时进行分析、评估,确保医疗器械处于良好检验、校准、保养、维护并状态。记录,及时进行分析、评估,确保医疗器械处于良好状态。对使用期限长的大型医疗器械,应当逐台建立使用档案,记录其使用、维护对使用期限长的大型医疗器械,是否逐台建立使用档15 等情况。记录保存期限不得案,记录保存期限是否符合要求。少于医疗器械规定使用期限届满后 5 年或者使用终止后5年。.医疗器械使用单位可以按照合同的约定要求医疗器械生产经营企业提供医疗器械维护维修服务,也可以委托有条件和能力的维修服
12、务机构进行医疗器械维护维修,或者自行对在医疗器械使用单位委托维修服务机构或者自行对在用用医疗器械进行维护维修。医疗器械进行维护维修的,相关合同是否约定了提供维护16医疗器械使用单位委托维手册、维修手册、软件备份、故障代码表、备件清单、零修服务机构或者自行对在部件、维修密码等维护维修必需的材料和信息。用医疗器械进行维护维修的,医疗器械生产经营企业应当按照合同的约定提供维护手册、维修手册、软件备份、故障代码表、备件清单、零部件、维修密码等维护维修必需的材料和信息。由医疗器械生产经营企业或者维修服务机构对 由医疗器械生产经营企业或者维修服务机构对医疗器医疗器械进行维护维修的, 械进行维护维修的,合同
13、是否约定明确的质量要求、维修应当在合同中约定明确的 要求等相关事项,查看相应的维修记录是否真实、完整。17 质量要求、维修要求等相关 医疗器械使用单位自行对医疗器械进行维护维修的,是否事项,医疗器械使用单位应 对从事医疗器械维护维修的技术人员开展培训考核,建立当在每次维护维修后索取 培训档案,并保存相关培训考核记录。并保存相关记录;医疗器械使用单位自行对医疗器械.进行维护维修的,应当加强对从事医疗器械维护维修的技术人员的培训考核,并建立培训档案。医疗器械使用单位发现使用的医疗器械存在安全隐患的,应当立即停止使查看相关制度文件是否明确对存在安全隐患的医疗器18 用,通知检修;经检修仍不 械排查与
14、处理的要求。查看有关记录,是否及时按照有关能达到使用安全标准的,不 规定处置。得继续使用,并按照有关规定处置。医疗器械使用单位之间转让在用医疗器械,转让方应当确保所转让的医疗器械安全、有效,并提供产 存在医疗器械使用单位之间转让在用医疗器械的,查品合法证明文件。转让双方 看转让医疗器械的合格证明文件与检验报告是否合法、有19 应当签订协议,移交产品说 效,查看相关文件,判断是否按照转让协议移交产品说明明书、使用和维修记录档案 书、使用和维修记录档案复印件等资料。对受让方,还应复印件等资料,并经有资质 查看是否按照进货查验的规定进行查验。的检验机构检验合格后方可转让。受让方应当参照本办法第八条关
15、于进货查验的规定进行查验,符合要求.后方可使用。不得转让未依法注册或者备案、无合格证明文件或者检验不合格,以及过期、失效、淘汰的医疗器械。医疗器械使用单位接受医疗器械生产经营企业或者其他机构、个人捐赠医疗器械的,捐赠方应当提供医疗器械的相关合法证明文件,受赠方应当参照本办法第八条关于进货查验的存在接受捐赠医疗器械的,捐赠医疗器械的合格证明规定进行查验,符合要求后20文件与检验报告是否合法、有效。是否按照进货查验的规方可使用。不得捐赠未依法定进行查验。注册或者备案、无合格证明文件或者检验不合格,以及过期、失效、淘汰的医疗器械。医疗器械使用单位之间捐赠在用医疗器械的,参照本办法第二十条关于转让在用医疗器械的规定办理。.(注:表格素材和资料部分来自网络,供参考。只是收取少量整理收集费用,请预览后才下载,期待你的好评与关注)
- 温馨提示:
1: 本站所有资源如无特殊说明,都需要本地电脑安装OFFICE2007和PDF阅读器。图纸软件为CAD,CAXA,PROE,UG,SolidWorks等.压缩文件请下载最新的WinRAR软件解压。
2: 本站的文档不包含任何第三方提供的附件图纸等,如果需要附件,请联系上传者。文件的所有权益归上传用户所有。
3.本站RAR压缩包中若带图纸,网页内容里面会有图纸预览,若没有图纸预览就没有图纸。
4. 未经权益所有人同意不得将文件中的内容挪作商业或盈利用途。
5. 装配图网仅提供信息存储空间,仅对用户上传内容的表现方式做保护处理,对用户上传分享的文档内容本身不做任何修改或编辑,并不能对任何下载内容负责。
6. 下载文件中如有侵权或不适当内容,请与我们联系,我们立即纠正。
7. 本站不保证下载资源的准确性、安全性和完整性, 同时也不承担用户因使用这些下载资源对自己和他人造成任何形式的伤害或损失。
最新文档
- 嵌入式系统概论-以S3C2440核心为架构课件
- 地理事象的季节变化课件
- 地理中外著名旅游景观欣赏课件
- 地理中图版选修5第一章第二节主要自然灾害及其分布课件
- 地理中考复习-地图课件
- 北师大版历史八年级下册第17课《筑起钢铁长城》课件1
- 北师大版历史八下《祖国统一的历史大潮》课件5
- 北师大版历史八下《欣欣向荣的科教文体事业》3课件
- 北师大版历史八下《蓝色的地中海文明》课件
- 北师大版历史九年级下册第10课“冷战”与“热战”丁飞鹤T-课件
- 北师大版历史八下第17课《大河流域的文明曙光》课件
- 北师大版历史九上1718课课件
- 高中化学热力学复习10多重平衡与化学计算ppt课件
- 高中化学第1章化学反应与能量转化第3节化学能转化为电能电池ppt课件1鲁科版选修
- 高中化学第三节玻璃、陶瓷和水泥公开课课件
