 第四单元物质构成的奥秘
第四单元物质构成的奥秘


《第四单元物质构成的奥秘》由会员分享,可在线阅读,更多相关《第四单元物质构成的奥秘(22页珍藏版)》请在装配图网上搜索。
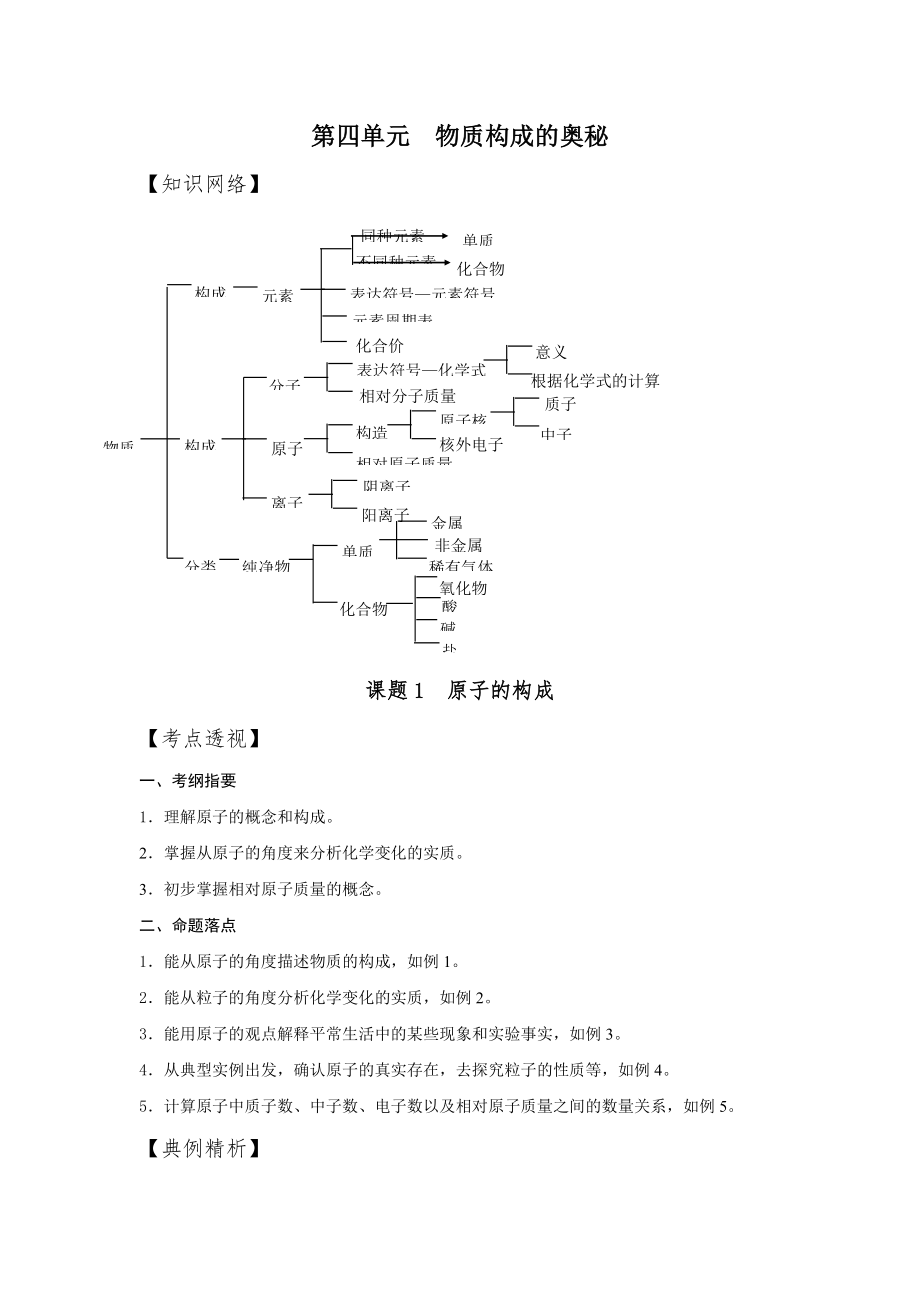
1、第四单元 物质构成的奥秘【知识网络】 单质 同种元素 不同种元素 化合物 表达符号元素符号元素周期表 化合价元素 构成表达符号化学式 相对分子质量 分子 原子 构造 原子核 核外电子 质子 中子 相对原子质量 离子 阴离子 阳离子 构成 意义 根据化学式的计算 单质 金属 非金属 稀有气体 纯净物 分类 化合物 氧化物 碱 酸 盐 物质 课题1 原子的构成【考点透视】一、考纲指要1理解原子的概念和构成。2掌握从原子的角度来分析化学变化的实质。3初步掌握相对原子质量的概念。二、命题落点1能从原子的角度描述物质的构成,如例1。2能从粒子的角度分析化学变化的实质,如例2。3能用原子的观点解释平常生活
2、中的某些现象和实验事实,如例3。4从典型实例出发,确认原子的真实存在,去探究粒子的性质等,如例4。5计算原子中质子数、中子数、电子数以及相对原子质量之间的数量关系,如例5。【典例精析】例1:(河南省)下列说法不对的的是( )A原子能构成分子 B原子能直接构成物质C原子是在不断运动的 D原子在化学变化中可以再分解析 分子可以构成物质,原子也可以直接构成物质,如铁是由铁原子直接构成的,故A、B都对的;原子和分子同样也是在不断运动的,C的说法也是对的的;根据原子的概念:“原子是化学变化中的最小粒子”可知,在化学变化中原子是不能再分的。答案:D例2:(南通市课改区)如下图是水分子在一定条件下分解的示意
3、图,从中获得的信息中不对的的是( )A一种水分子由二个氢原子和一种氧原子构成B水分解后生成氢气和氧气的分子个数比为21 C水分解过程中,分子的种类不变D水分解过程中,原子的数目不变解析 本题通过水电解的微观示意图,让学生归纳可以获得的信息,本是一道开放性试题,但由于是选择题,限定了几种答案,只要能判断正误就可以了。从反映的微观示意图中可以分析出水分子的构成,反映生成物的分子个数比,反映前后的原子个数不变,但分子个数不一定不变,分子种类一定变化。答案:C例3:(南京市)在2400近年前,古希腊哲学家德谟克利特在一首诗中体现了物质不灭的观点:“无中不能生有,任何存在的东西也不会消灭。看起来万物是死
4、了,但是实则犹生:正如一场春雨落地,霎时失去踪影;可是草木把它吸取,长成花叶果实,仍然欣欣向荣。请你从分子和原子的观点,阐明物质不灭的因素。解析 从分子和原子的观点解释物质不灭,核心要指出在物理变化中微粒种类不变,质量不变;在化学变化中,分子要分解成原子,原子不能再分,构成新的分子,元素的种类、各原子个数、原子的质量都没有发生变化。答案:物质是由原子、分子等粒子构成的,分子是由原子构成的。在物理变化中,构成物质的原子、分子自身不变。在化学变化中,反映物的原子重新组合生成新物质,原子的种类、数目和质量都不变化。因此物质不灭。例4:(烟台课改区)科学家设想宇宙中也许存在完全由反粒子构成的物质反物质
5、;物质反物质相遇会释放出巨大的能量,在能源研究领域中前景可观,正电子、负质子等都是反粒子,它们跟一般所说的电子、质子相比较,质量相等但电性相反,请您推测,反氢原子的构造也许是( )A由1个带正电荷的质子和1个带负电荷的电子构成。B由1个带负电荷的质子和1个带正电荷的电子构成。C由1个带正电荷的质子和1个带正电荷的电子构成。D由1个带负电荷的质子和1个带负电荷的电子构成。解析 该题是信息题,应抓住题中“反物质”的概念,懂得什么是“反粒子”,采用逆向思维,氢原子是由一种带正电的质子和一种带负电的电子构成,那么反氢原子的构造一定是由一种带负电的质子和一种带正电的电子构成,因此A、C、D错误。答案:B
6、例5:(河北省)国内“嫦娥工程”探月筹划的一种重要目的是开发月球新能源“氦3”,10吨氦3就能满足国内一年所有的能源需求。有关氦原子的说法对的的是( )A质子数为3,电子数为3 B质子数为2,电子数为2 C质子数为2,电子数为3 D质子数为3,电子数为2解析 要懂得原子的构造中各粒子数目间的关系以及符号的意义。“He3”是指相对原子质量为3,质子数为2的氦原子。根据在原子中“核电荷数=质子数=核外电子数;相对原子质量=质子数+中子数”这两个关系式可知,电子数应为2,中子数为1。答案:B【常用误区】1不能抓住原子概念的本质特性。在化学变化中,原子不能再分了,是指原子核没有变化,核外电子还是有变化
7、的。化学变化的实质是分子分解为原子,原子再重新组合成新的分子,但在此变化中,原子的种类、数目和质量都没有发生变化。如例1中的D选项和例2中的D选项以及例3。2原子不仅可构成分子,也可直接构成物质,并且能保持所构物质的化学性质;原子同其她的粒子同样都具有不断运动,体积小、质量轻,粒子间均有一定的间隙等性质。如例1。3原子的种类是由原子核内的质子数决定的,一当质子数变化,其原子的种类随之变化,且此变化不是化学变化。4原子中“核电荷数=质子数=电子数;相对原子质量=质子数+中子数”这两个关系式掌握的不牢。如例5。【基本演习】一、选择题1氩气是一种惰性气体,若以表达氩原子,则氩气是如下列何种形式存在?
8、( )A B C D2下列符号中,表达一种原子,又表达一种元素,还表达一种物质的是( )AC60 B2H C2N2 DFe3国内出名科学家、中国科学院院士张青莲专家主持测定了铟、铱、锗、铕、镝等元素相对原子质量的新值。其中,核电荷数为63的铕元素的相对原子质量为152。该元素原子的中子数为( )A89 B26 C126 D634下列符号中,表达2个氢原子的是( )AH2 B2H CH2O D2H2 51999年度诺贝尔化学奖获得者艾哈迈德泽维尔,开创了“飞秒化学”的新领域,使运用激光光谱技术观测化学反映时分子中原子的运动成为也许。你觉得该技术不能观测到的是( )A化学反映中反映物分子的分解 B
9、反映中原子的运动C化学变化中生成物分子的形成 D原子核的内部构造6科学技术的发展,使人们操纵单个原子和分子成为也许,从而可以直接用原子来制造分子。若能用这种措施制造葡萄糖(C6H12O6),下列原子中不需要的是( )A碳原子 B氢原子 C氮原子 D氧原子二、填空题氧分子 氢分子 水分子7下图中,表达氧原子,表达氢原子。根据此图,试分别从物质构成、分子构成的角度各说出一种观点:a ;b 。根据此图,阐明化学反映的本质: 。8原子是由原子核和电子构成的。原子核在原子中所占体积极小,其半径在约为原子半径的十万分之一,因此,相对而言,原子里有很大空间,粒子是带两个单位正电荷的氦原子。19,科学家用一束
10、平行高速运动的粒子轰击金箔时(金原子的核电核数为79,相对原子质量为197),发现三种实验现象:(1)有一小部分粒子变化了本来的运动途径。因素是粒子路过原子核附近时,受到斥力而稍微变化了运动方向。(2)大多数粒子不变化本来的运动方向,因素是_。(3)很少数粒子被弹了回来,因素是_。(4)19物理学家卢瑟福用氦原子核轰击氮原子核,成果得到氧、氢两种原子。某些同窗因此断定说:“这是生成新物质的变化化学变化,元素可以通过化学变化来制取。”你觉得这些同窗的说法与否对的?为什么?课题2 元素【考点透视】一、考纲指要1理解元素的概念,对的理解物质的宏观构成和微观构造。2理解元素符号所示的意义,学会元素符号
11、的对的写法。3初步结识元素周期表,懂得它是学习和研究化学的工具,能根据原子序数,在元素周期表中找到指定元素和理解该元素的有关信息。4理解物质的简朴分类。二、命题落点1运用元素这一宏观概念,去对的描述物质的构成或成分,如例1。2考察元素符号所示的意义,如例2。3命题时往往给出元素周期表或部分内容,规定根据元素周期表中的递变规律,去推测某些未知元素的构造和性质,或发现某些规律,如例3。4一般给出常用物质名称、俗名、图形或其她信息,根据构成物质中元素的种类,来判断物质所属的类别,如例4。【典例精析】例1:(黑龙江课改区)“三氯生”是一种高效广谱抗茵剂,广泛应用于牙膏、药皂、洗面奶、空气清新剂等。下面
12、有关三氯生(C12H7Cl3O2)的说法中错误的是( )A三氯生中具有氧气分子 B三氯生由碳、氢、氯、氧四种元素构成C三氯生是一种有机物 D一种三氯生分子中共具有24个原子解析 本题是有关物质的元素构成的考察,波及到化学式的其她方面,属于综合题。三氯生是纯净物,其中不也许具有氧分子,因此A是错误的。答案:A例2:(黄冈市) 下列符号中,既表达一种原子,又表达一种元素,还表达一种物质的是( )AC60 BO2 CH DAu解析 C60 和O2 分别是足球烯和氧气的化学式,可表达物质或该物质的一种分子,但不能表达一种元素或一种原子了;H可表达氢元素或一种氢原子,但不能表达氢气单质,氢气的化学式为H
13、2;只有Au既表达一种原子,又表达一种元素,还表达一种物质,由于金是由原子直接构成的。答案:D例3:(南通课改区)我们周边的物质世界是由100多种元素构成的,为了便于研究元素的性质,常常需要寻找它们之间的内在规律。下表列出的是118号元素的部分最高正化合价和最低负化合价。请你阅读后,回答问题:(1)11号元素属于_元素(填“金属”或“非金属”),它在化学反映中形成的粒子与_(写元素符号)原子具有相似的核外电子排布。(2)16号元素的原子核外电子数为_,推测该元素最低负化合价为_,最高正化合价的氧化物的化学式为_。(3)从化合价角度分析,我们可以发现某些规律。请写出其中的一种:_。解析 元素周期
14、表中每一种周期都从金属元素开始,到稀有气体元素结束(第一周期从非金属元素氢开始)。原子序数和核电荷数(质子数)相等,即可知16号元素原子的核外电子数。分析表中信息可推测出S元素的最低负化合价、最高正化合价,进而拟定化学式。根据图表找规律的一般措施是对比分析法,即将表中所给的信息,从横向和纵向及整体进行对比,找出其相似点和不同点,综合提炼出新的信息也就是其中隐含的规律。从化合价的角度横向对比,不难看出:同一横行(周期)从左到右元素的最高正化合价逐渐升高;从纵向对比可以看出:同一纵行元素的最高正化合价(或最低负化合价)相等等规律。答案:(1)金属 Ne (2)16 2 SO3 (3)同一横行(周期
15、)从左到右元素的最高正化合价逐渐升高例4:(四川省)已知“O”、“”表达质子数不同的原子。 (1)下列表达的气体物质中,属于化合物的是 。 (2)下列表达的气体物质中,属于混合物的是 。解析 图A中的分子是由同一种原子构成的,故为单质分子;图B中的分子是由两种原子构成的同种分子,应为化合物;图C和D中都具有两种不同的分子,故为混合物。答案:B;C D【常用误区】1对物质的宏观和微观描述混淆不清。如元素只能讲种类,不能讲个数;粒子既可讲种类,又可讲个数。2元素的种类是由质子数决定的;在化学变化中,元素的种类和质量也不变化;元素的化学性质与其原子最外层上的电子数密切有关。3缺少摸索和发现能力的训练
16、。如在元素周期表中,随原子序数的递增,原子构造中电子层数、最外层电子数发生规律性的变化,元素的种类(金属、非金属、稀有气体)和元素性质,也发生规律性的变化。如例3。【基本演习】一、选择题1如图和分别表达两种不同质子数的原子,其中表达化合物的是( ) A B C D2经测定一瓶气体中具有C、H两种元素,这瓶气体不也许是( )A一种化合物 B一种单质和一种化合物的混合物C两种化合物 D两种单质3下列物质中属于有机物的是( )A干冰 B蒸馏水 C小苏打 D酒精4国外医学界研究表白,如果人体不缺少微量元素而随意过量补充,不仅对健康无益,反而有害。下列元素属于人体中微量元素的是( )A碳 B.氢 C.氧
17、 D. 铁二、填空题5. 某学生用A、B、C、D四种元素构成的化合物AD、BAC、BCD通过一系列十分复杂的化学反映,制造出人类目前尚未知的物质X。该学生在科技新闻发布会上说:“我制造出一种新元素X。”该学生的话是 (填“对的的”或“错误的”),由于 。6请从H、C、O、K中选择合适的元素,按照规定写出化学式(各写一例): 酸性氧化物 有三种元素构成的酸 可以溶于水的碱 有三种元素构成的盐 7物质之间既互相联系,又存在规律,这是我们学好化学应当掌握的一种基本措施。请你仿照下表中的示便。找出O2,CH4、CO2、NH3 C2H4(乙稀)五种气体之间的存在的此外两个规律,并排列出顺序,将答案填在下
18、表中的空格内。规律排列顺序示例:原则状况下,密度由小到大CH4、NH3、C2H4、O2、CO28元素周期表是学习和研究化学的重要工具。下图是元素周期表的一部分。(1)诸多科学家对元素周期表的发现和完善做出了重大奉献,请写出其中一位科学家的名字_。(2)查出碳的相对原子质量:_,写出16号元素的元素符号:_。(3)表中不同种元素最本质的区别是_(填序号)。 A质子数不同 B中子数不同 C相对原子质量不同 D电子数不同(4)运用元素周期表,人们对元素的结识进入全新的奔腾时期。近日,俄罗斯科学家宣布她们将人将人工合成第118号元素,则此元素的核电荷数为_。课题3 离子【考点透视】一、考纲指要1初步理
19、解原子核外的电子是分层排布的。2理解原子构造的表达措施。3理解原子构造与元素化学性质的关系。4理解离子的形成过程,结识离子是构成物质的一种粒子。二、命题落点1运用粒子中质子数、电子数的关系去判断粒子种类,如例1。2根据原子的构造来判断或推测元素有关的化学性质,如例2。3能从离子的角度描述物质的构成,能用粒子的观点解释某些现象和实验事实,如例3。【典例精析】例1:(威海市)在宏观物质、微观粒子和化学符号之间建立联系,是化学科学特有的思维方式。已知氢、碳、氧、钠、氯五种元素的核电荷数分别为:1、6、8、11、17。试按下列规定,写出微观粒子的化学符号,以及由这种粒子构成的或具有这种粒子的一种物质的
20、名称(微观粒子和物质所波及的元素限定在上述5种元素内)需满足的条件粒子的化学符号相应的物质的名称(1)质子数为11的同种元素的原子和离子 (2)质子数均为10的两种不同的分子(3)质子数为1的阳离子和质子数为9的阴离子解析 同元素的原子和离子指核电荷数相似,核外电子数不同的微粒。由于质子数为11,因此应是钠原子和钠离子;质子数均为10的不同的分子有NH3、H2O、HF、CH4等。质子数为1的阳离子是H+,质子数为9的阴离子有F-或者OH-。再找到具有这些离子的物质就可以了。答案:粒子的化学符号相应物质名称Na金属钠Na+氯化钠(氢氧化钠等)H2O水CH4(HF、NH3)甲烷(氟化氢,氨气等)H
21、+盐酸(硫酸)OH-(F-)氢氧化钠(氟化氢)例2:(宜昌市)下图示表达非金属元素的是 ;化学性质相似的是 ;具有稳定电子层构造的是 ;属于离子的是 ;表达同种元素的是 。286+16281+1168+82+112A B C D 解析 在原子构造示意图中,最外层电子数一般少于4个,为金属元素(H、He、B除外),多于或等于4个为非金属元素,等于8个为稀有气体元素(He为2个),上图中B、D最外层电子数不小于4个,应为非金属元素;在原子构造示意图中,核内质子数等于核外电子数的为原子,不相等的则为离子,故A为离子;核内质子数相等的粒子为同种元素,最外层电子数相等的原子,化学性质也相似。答案:表达非
22、金属元素的是B、D、;化学性质相似的是B、D;具有稳定电子层构造的是B;属于离子的是A;表达同种元素的是A、C。例3:(四川自贡课改区)下面这幅卡通画形象地呈现了钠与氯气反映形成氯化钠的微观过程,在此过程中,钠原子变成了钠离子。 钠与氯气反映形成氯化钠(钠原子和氯原子的构造示意图分别为: (1)钠元素处在元素周期表中的第_周期;(2)氯是非金属元素,它的原子在化学反映中一般比较容易_电子;(3)请你比较分析钠原子和钠离子的微粒构造的异同:相似之处:_;不同之处:_。解析 根据题目所给信息及所学知识:原子的电子层数即为该元素在元素周期表中的周期数、元素的化学性质与原子最外层电子数的关系,(1)(
23、2)两问较为简朴。第(3)问重要结合离子形成的过程,从质子数、电子灵数、电子层数等方面入手,分析问题要全面、细致。答案:(1)三(2)得到(3)核电荷数或质子数相似,第一、二层电子数相似,核外电子数、电子层数、最外层电子数不同。【常用误区】1对原子、阳离子、阴离子的构成及其区别与联系,缺少整体把握,导致错误。在原子中:核电荷数=质子数=电子数;在阳离子中:核电荷数=质子数电子数;在阴离子中:核电荷数=质子数电子数。如例2。2对构造与性质之间的关系结识不清。构造决定了性质,反过来,性质又反映出构造。如例3。【基本演习】1现榨的苹果汁在空气中会由淡绿色变为棕黄色。你猜想其因素也许是( )A苹果汁中
24、的Fe2+变成Fe3+ B苹果汁中具有Cu2C苹果汁中具有OH D苹果汁中具有K21个氢原子是由一种质子和一种电子构成,不含中子。当1个氢原子失去1个电子后,它不会变成( )A质子B原子核 C阳离子 D带负电荷的离子3根据粒子构造示意图给出的信息,下列说法对的的是( )A表达的是三个原子 B表达的元素是非金属元素C表达的是阳离子 D表达的元素化学性质相似二、填空题4下图为四种粒子的构造示意图,请用相应的序号填空:(1)属于同种元素的粒子是_;(2)具有相对稳定构造的粒子是_;(3)某元素R形成碱的化学式为R(OH)3,则R元素相应的原子构造示意图也许是_。5下图是118号元素原子最外层电子数与
25、原子核电荷数的关系图。试回答:(1)一种水分子共有_个原子核、_个质子。(2)一种Mg2+核外共有_个电子;Cl-的最外层电子数和_原子的最外层电子数相似。(3)通过上图你能发现哪此规律?请写出其中一种:_。6明矾(化学式为KAl(SO4)212H2O)是农村常用的一种净水剂,它在水中离解出K+、Al3+和SO42-。甲同窗为了探究明矾中每种粒子与否有净水作用,进行了如下实验,请填写表中空白。 实验操作 实验现象 结论在一杯浑浊的水中加少量KCl,静置烧杯中的水仍浑浊在一杯浑浊的水中加少量Al2(SO4)3,静置烧杯中的水变澄清乙同窗看到甲的方案后,觉得该方案不完善,她对甲同窗的方案进行了补充
26、完善。请你把乙同窗补充方案中要达到的目的和所使用的试剂填入下表。 实验目的 使用的试剂7氧化铜是一种黑色固体,可溶于稀硫酸。某同窗想懂得是稀硫酸中的哪种粒子(H2O、H+、SO42-)能使氧化铜溶解。请你和她一起通过图中I、三个实验完毕这次探究活动。(1)你提出的假设是_。(2)通过实验I可证明_。(3)要证明此外两种粒子能否溶解氧化铜,还需要进行实验和,在中应当加入_。(4)探究成果为_。你觉得除实验和所用试剂外,还可以溶解氧化铜的一种常用物质是_。课题4 化学式与化合价【考点透视】一、考纲指要1理解化学式的涵义。能用化学式表达物质的构成2熟记常用元素及原子团的化合价,并能运用化合价推求化学
27、式。3理解相对分子质量的涵义,并能运用相对原子质量和相对分子质量计算。二、命题落点1命题时常给出化合价写出相应的化学式,如例1。2给出物质的化学式,要能懂得化学式所示的意义,如例2。3能根据物质的化学式,寻找物质间的内在规律,如3。4一般考察根据指定规定,用化学符号表达粒子、粒子的个数,以及化学符号周边数字的意义等,如例4。5根据给出化学式去求某一种元素的化合价,如例5。6有关化学式的计算的重要考察,如例6。【典例精析】例1:(湖北黄冈市)已知,碘(I)元素有1、1、3、5、7等多种化合价,碘酸碘是由带正电荷的碘离子和碘酸根(IO3)离子构成。你觉得它的化学式也许是下列中的( )。AI2O5
28、BI2O7 CI4O5 DI4O9解析 此题所予以的信息是根据化合价规则拟定物质的化学式。解题的核心在于拟定碘酸根的数目。由题意,碘酸碘是由带正电荷的碘离子和碘酸根(IO3)离子构成的,根据碘酸根离子中所含氧原子数拟定碘酸碘中含碘酸根离子的数目,再由化合价规则拟定该碘离子的数目并加以验证。I4O9具有含3个碘酸根离子,可写成3 1I(IO3)3形式。答案: D例2:(南京市)lO月15日,中国“神州五号”飞船载人航天获得成功。偏二甲肼是火箭推动器的常用燃料。根据偏二甲肼的化学式C2H6N2,你懂得哪些信息?(即化学式表达的意义,回答不规定波及相对原子质量。)请写出三点:(1) ,(2) ,(3
29、) 。解析 本题考核对化学式所示意义的理解限度,规定从宏观与微观、构成与构成等方面去理解化学式表达的意义,有时也许从化学式所示的构造特性推断也许具有的化学性质。答案:(1)偏二甲肼由碳、氢、氮三种元素构成(2)每个偏二甲肼分子由2个碳原子、8个氢原子、2个氮原子构成(3)偏二甲肼属于化合物 (其她合理答案给分)例3:(大连市)物质之间既互相联系,又存在规律,这是我们学好化学应当掌握的一种基本措施。请你仿照下表中的示便。找出O2,CH4、CO2、NH3 C2H4(乙稀)五种气体之间的存在的此外两个规律,并排列出顺序,将答案填在下表中的空格内。规律排列顺序示例:原则状况下,密度由小到大CH4、NH
30、3、C2H4、O2、CO2解析 分析五种气体,从化学式表达的意义出发,按构成、构造、性质寻找它们内在联系进行排序。如从构成、构造出发,每个分子中具有的原子个数多少、相对分子质量的大小、等质量的物质含分子数的多少;从性质思考,密度的大小等。答案:(1)分子中所含的原子总数:O2、CO2 NH3、 CH4、C2H4(2)相对分子质量的大小:CH4、NH3、C2H4、O2、CO2例4:(山西省)用化学符号表达:3个氮原子 ,+3价的铝元素 ,n个水分子 ,2个铁离子 。解析 元素符号既可表达该种元素,又能表达该种元素的一种原子;化学式既能表达该种物质,又能表达该种物质的一种分子;化合价一般表达在元素
31、(或原子团)的正上方,符号在前,数字在后;离子一般表达在元素(或原子团)的右上角,数字在前,符号在后。 +3答案:3N Al nH2O 2Fe3+例5:(菏泽市)下列物质中均具有氯元素,它们按下列顺序排列:KCl Cl2 HClO X NaClO4。根据这种排列规律,X不也许是( )AAgCl BKClO3 CHClO2 D。Cl2O5解析 从题中提供的几种物质的排列顺序,我们不难发现它们是按氯元素化合价由低到高的顺序排列,可推知X也应具有氯元素,且氯元素的化合价应在+1到+7之间都可以,而AgCl 中氯元素化合价为1,故不行。答案:A例6:(无锡市)下图为哈药集团制药六厂生产的“新盖中盖牌”
32、高钙片标签上的部分文字,请仔细阅读后回答问题。重要原料碳酸钙、维生素D功能成分补钙每片中含:钙(以Ca计)500 mg维生素D 100 IU食用措施 每日1次,每次1片规 格 2.5g/片(1)维生索D种类较多,其中维生素D2的化学式为C28H44O,试计算维生素D2的相对分子质量为 ;维生素D2中碳、氢、氧三种元素的质量比为 。(2)计算高钙片中碳酸钙的质量分数 。(3)根据你对补钙产品的调查和已有的化学知识,判断下列物质可作为补钙品直接服用的是 (填字母)。A氧化钙 B氢氧化钙 C葡萄糖酸钙(4)目前市场上的补钙产品诸多,请你再举出一种补钙产品的名称 (不能使用本题中已浮现过的名称)。解析
33、 这道题直接运用化学式中有关量的关系进行计算,即答案:(1)396 84114 (2)50% (3)C (4)盖天力(或巨能钙、盖种盖等)【常用误区】1元素的化合价是元素的一种性质,一种元素也许有几种化合价。如Fe有+2和+3价。但在某一具体的物质中,元素的化合价是拟定的,也许只体现出一种或几种。如在FeSO4 中Fe只能为+2价;在NH4NO3 中N体现为3和+5两种价态。2微粒名称、符号、构造示意图的书写或匹配错误。如例6中铝元素的化 3+合价不能表达为Al+3,铁离子不能表达为Fe+3、Fe或Fe2+等。3化合价与化学式的算错或写错。如例4。4混合物中元素的质量或质量分数的计算容易错,如
34、例7。【基本演习】一、选择题1微型化录音的高性能磁带中的磁粉重要材料之一是化学构成相称于CoFe2O4的化合物,又知钴(Co)和铁都也许有+2、+3价,且在上述化合物中每种元素只有一种化合价,则钴和铁的化合价分别为( )A+2,+3 B+2,+2 C+3,+3 D+3,+22,合肥、芜湖等都市已开始使用西气东输工程送来的天然气,天然气重要成分是CH4,下列四位同窗在讨论化学式CH4的意义,其中错误的是( )3既有H2S、S、M、SO3四种物质,是按硫元素的化合价由低到高排列的,其中M这种物质的化学式可以是( )AH2SO3 BH2SO4 CNa2S DNa2SO44X元素原子的最外层有6个电子
35、,Y元素的原子最外层上有2个电子,X、Y元素化合形成的离子化合物的化学式为( )AYX BY2X CYX2 DXY二、填空题5葡萄糖在人体组织中缓慢氧化放出热量,这是人类生命活动所需能量的重要来源之一。葡萄糖的化学式为C6H12O6,从葡萄糖的化学式你能总结出哪些信息(请写出两条)?(1)_;(2)_。6由(NH4)2S 、(NH4)2SO4 、(NH4)2HPO4 构成的混合物中,已知氮元素的质量分数为28%,则混合物中氧元素的质量分数为 。三、计算 7右图是市售某品牌牙膏包装盒上的部分阐明。其重要活性成分单氟磷酸钠(Na2PO3F)是牙膏的常用添加剂之一,实验表白牙膏中单氟磷酸钠的质量分数
36、达到0.76%0.80%时,防龋齿的效果较好。(计算成果保存小数点后二位)(1)求单氟磷酸钠中F元素的质量分数。(2)通过计算判断,该牙膏与否有较好的防龋齿效果。 单元测试题一、选择题(下列各题只有一种对的选项,每题2分,合计20分)1小华用凉开水养鱼,不久鱼儿全死了。下列解释合理的是( )A凉开水中几乎不含氧元素 B凉开水中几乎不含氧原子C凉开水中几乎不含水分子 D凉开水中几乎不含氧气2下列符号只具有微观意义的是( )AH2 BH2SO4 C2H2O DC2H23(03上海市)氮化硅是一种新型陶瓷材料的重要成分,能承受高温,可用于制造业、航天业等领域。已知氮、硅的原子构造示意图分别如下图。请
37、推测氮化硅的化学式为( ) ASi3N4 BSi4N3 CSi3N7 DSi7N3 4下列有关Fe、Fe2+、Fe3+的说法中,对的的是( )A它们结合其她原子的个数相似 B它们的质子数不同C它们的最外层电子数相似 D它们的核外电子数不同5国内在1993年成功制取了一种由相对原子质量为18、核电荷数为8的氧原子构成的双原子分子气体,下列说法对的的是( )A种气体的相对分子质量是32B这种氧原子和氢原子构成的水分子,其相对分子质量为20C这种氧原子的核内质子数为10 D这种氧原子的核外电子数为106测得某溶液中仅具有Na、Mg2、SO42、Cl四种离子,其中离子个数比为NaMg2Cl = 458
38、,若设Na为4n个,则SO42的离子数为( )A2n B3n C6n D8n7如上图,这四位同窗描述的也许是下面的同一种化学符号 ( )AHClO BO3 C.NO2- DH2O8下列各组原子构造示意图中,所示的两种元素具有相似化学性质的是 ( )A B.CD9188O(质子数为8,相对原子质量为18)是一种与一般氧原子有相似的核内质子数的原子,它与一般氧原子的化学性质相似,在有机化学反映中被用作示踪原子。188O与一般氧原子属于( )A相似分子 B相似原子 C相似元素 D相似单质10下图是表达物质分子的示意图。图中“”和“”分别表达两种具有不同质子数的原子,则图中表达单质的是( ) 二、选择
39、题(如下每题也许有12个符合规定的答案。错选、多选不给分。有二个答案的,只选一种且对的,给2分。每题3分,合计15分)11科学家已研究出高能微粒N5+,有关它的说法对的的是( )AN5+是有5个氮原子构成的单质 BN5+中只有质子没有中子和电子C每个N5+中具有35个质子和34个电子D每个N5+中具有35个质子和35个电子12十九世纪初,意大利科学家阿伏加德罗在总结前人工作的基本上,提出了分子的概念,觉得:一切物质都是由分子构成的;分子由原子构成;原子不能独立存在;分子是保持物质化学性质的最小粒子;分子的质量等于构成它的原子的质量之和;分子在不断地运动。从你所学的知识看,上述观点中存在明显局限
40、性的是( )A B C D13由碳、氧元素构成的气体中,碳与氧的质量比为3:5,则该气体也许是( )A由CO2 或CO单独构成的纯净物 B由CO和CO2 共同构成的混合物C由CO和O2 共同构成的混合物 D由O2和CO2 共同构成的混合物14核外电子数相似,核内质子数不同的两种粒子,它们也许是( )A一种元素的原子和另一种元素的离子 B同种元素的原子和离子C两种不同元素的原子 D两种不同元素的离子15.由如下粒子构造示意图得出的结论中,错误的是( )A、分别与、反映均能形成与电子层构造相似的粒子B上述粒子间能形成AB型、AB2型、A2B型化合物C上述粒子形成化合物前后,质子总数、电子总数均发生
41、变化,而质量不变D上述粒子形成化合物前后,在化合物中均能显示可变化合价三、简答题空气热 火 干 土 冷水 湿 16(3分)古希腊出名学者亚里士多德曾提出过“四元素说”,觉得火、空气、土、水是构成世界万物的基本元素,它们两两作用产生物质的基本性质热、冷、干、湿,如图所示。你觉得“空气”和“水”是元素吗?为什么?17(3分)对“原子在化学反映中不可再分”这一句话,在学完了原子构造和核外电子排布知识后,你是如何理解的?四、填空题18(5分)用化学符号表达:3个氮原子_,+3价的铝元素_,n个水分子_,2个铁离子_,2个铵根离子 。19(8分)(1)欢迎参与我们的化学俱乐部,请你写出符合与下列特性提示
42、有关的物质名称提示1提示2提示3物质名称物质1液体银白色温度计物质2碳元素很硬昂贵物质3空气植物根系保护气物质4无色光合伙用人工降雨(2)化学与我们的生活密切有关,平常生活中的化学知识有诸多。想想看,你懂得生活中常用的如下物质分别具有什么化学成分?“干冰”常用于人工降雨,干冰中的“冰”是指_;(填化学式)管道煤气中具有使人中毒的成分,该有毒气体是指_;(填化学式)碘酒是生活中常用的皮肤消毒剂,碘酒中的“酒”是指_;(填名称)天然气是常用的气体燃料,天然气中的“气”重要是指_;(填化学式)氧气氮气20(8分)下图是从空气中分离氧气的示意图:请你写出从图中所获得的有关物质构成、构造、性质、变化等信
43、息各一条: 构成: 构造: 性质: 变化: 21(8分)右面是四种粒子的构造示意图:序号填空:(1)电子层排布相似的是 ;(2)属于同种元素的是 ;(3)表达阳离子的是 ; (4)属于非金属元素原子的是 。 22(6分)科学家发现,细胞膜中存在着某种只容许水分子出入的通道-水通道。右图是诺贝尔化学奖获得者彼得阿格雷发布的世界上第一张水通道蛋白的示意图。(1)右图水通道中的每个“”表达: ; 。(2)根据示意图,由于水通道中间的正电荷对H+离子有 作用,因此,H+离子不能通过该水通道。23(8分)俄国化学家门捷列夫在总结前人经验的基本上,通过艰苦的努力,终于提出了现代元素周期表的雏形。下表为元素
44、周期表的部分示意图,表中数字为各元素原子的质子数,运用下表回答有关问题:H1He2Li3Be4B5C6N7O8F9Ne10Na11Mg12Al13Si14P15S16Cl17Ar18(1)用符号表达:带两个单位负电荷且质子数为8的离子 (写一种)。AB2型化合物 、 (写两种)。(2)去年终重庆开县发生天然气“井喷”事件。喷出的气体中有一种有毒的具有18个质子的A2B型气体,其水溶液是一种无氧酸,请用符号和数字表达:3个A2B分子 。(3)研究表中各元素原子的质子数,可发现元素从左向右的排列规律是 ,请预测质子数为20的元素在表中的位置 (填、)。该元素离子的构造示意图是 。(填“甲”或“乙”)(4)已知元素周期表中原子序数等于质子数。请从元素种类、质子数分析第二、第三周期的元素分布,有什么规律? 。五、实验与探究题24(6分) NaOH溶液可使无色酚酞变红。我们懂得NaOH溶液中具有Na+离子、OH-离子、H2O分子,如要探究是哪种微粒使酚酞变红,请填写下表内容:实验环节现象分析推理过程结论六、计算题25(6分)自然界生命体的有机物构成除C、H、O外尚有其她元素,如藻类物质(化学式可表达为C106H263O110N16P)的构成中就具有N和P。丙氨酸是构成人体蛋白质的氨基酸之一,其分子构造如图所示:(1)写出丙氨酸的化学式。(2)丙氨酸中氮元素的质量分数是多少?
- 温馨提示:
1: 本站所有资源如无特殊说明,都需要本地电脑安装OFFICE2007和PDF阅读器。图纸软件为CAD,CAXA,PROE,UG,SolidWorks等.压缩文件请下载最新的WinRAR软件解压。
2: 本站的文档不包含任何第三方提供的附件图纸等,如果需要附件,请联系上传者。文件的所有权益归上传用户所有。
3.本站RAR压缩包中若带图纸,网页内容里面会有图纸预览,若没有图纸预览就没有图纸。
4. 未经权益所有人同意不得将文件中的内容挪作商业或盈利用途。
5. 装配图网仅提供信息存储空间,仅对用户上传内容的表现方式做保护处理,对用户上传分享的文档内容本身不做任何修改或编辑,并不能对任何下载内容负责。
6. 下载文件中如有侵权或不适当内容,请与我们联系,我们立即纠正。
7. 本站不保证下载资源的准确性、安全性和完整性, 同时也不承担用户因使用这些下载资源对自己和他人造成任何形式的伤害或损失。
